[导读] 一个偶然的机会在“中美加宫颈病理学交流群”中听闻一位华人病理学家提及了《Robbins Basic Pathology》这本书,出于对“Basic”的兴趣(想必也是最基础、最基本的知识以及各个器官系统的常见病、多发病),在华夏病理学网下载第9版进行了学习,现将“女性生殖系统”的部分内容编译如下,不当之处恳请批评指正……
▌译者:王巍伟 山东省诸城市妇幼保健院病理科
大多数子宫颈病变为相对无关紧要的炎症性病变(子宫颈炎),但是子宫颈也是世界范围内癌症最常见的发生部位。
一、子宫颈炎(CERVICITIS)
子宫颈炎症性病变非常常见,与阴道脓性分泌物相关。子宫颈炎分为感染性和非感染性两类,但是由于正常阴道菌群(包括:偶尔出现的阴道需氧菌和厌氧菌、链球菌、葡萄球菌、肠球菌和大肠杆菌)的存在而很难将两者进行区分。
比较重要的病原体包括沙眼衣原体、解脲支原体、阴道毛滴虫、念珠菌、淋球菌、HSV-2(生殖器疱疹病原体)以及一些类型的HPV,上述病原体通常由性接触传播。沙眼衣原体是目前最常见的致病菌,性传播疾病(STD)门诊多达40%的子宫颈炎病例均为其感染所致。虽然疱疹病毒性子宫颈炎比较少见,但也值得注意,因为在分娩过程中可以发生母婴垂直传播,并且可能导致新生儿发生严重、有时可以致命的系统性疱疹病毒感染。
非特殊类型子宫颈炎可以为急性或慢性。相对少见的急性子宫颈炎局限于产后期女性,通常由葡萄球菌或链球菌感染引起。慢性子宫颈炎由炎症和再生性上皮细胞两部分组成,所有生育期女性均可见一定程度的慢性子宫颈炎。子宫颈鳞状和柱状黏膜上皮均可呈增生性和反应性改变。最终,柱状上皮发生鳞状上皮化生。
子宫颈炎通常为常规检查或者由于白带过多而发现。分泌物培养必须谨慎判读,因为里面几乎总是存在共生性微生物(如前所述)。只有确定已知的致病微生物后才会有所帮助。
二、子宫颈肿瘤(NEOPLASIA OF THE CERVIX)
大多数子宫颈肿瘤为上皮源性,并且由致癌性人乳头瘤病毒(HPV)感染引起。在女性发育过程中,子宫颈管柱状、黏液分泌性上皮细胞和子宫颈外口覆盖的鳞状上皮细胞同时发生改变。青春期,鳞柱交界区发生外翻,从子宫颈外口就可以看到柱状上皮。然而,暴露的柱状上皮细胞最终发生鳞状上皮化生,所形成的区域称之为“移行区”(图1)。
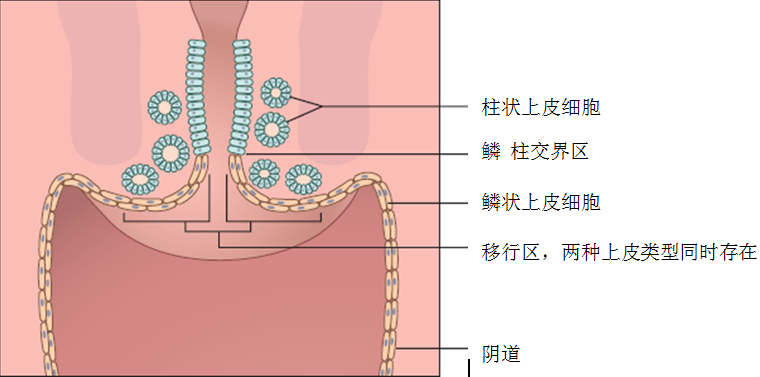
图1 子宫颈移行区形成过程
HPV是子宫颈肿瘤的致病病毒,其倾向于感染移行区非成熟鳞状上皮细胞。大多数的HPV感染为短暂性,通过急性和慢性炎症反应于数月内将其清除。仅有一小部分HPV感染持续存在,其中一些可以进展为子宫颈鳞状上皮内病变(CIN);这是一种癌前病变,大多数浸润性子宫颈癌都是由其进展而来。
几乎所有CIN和子宫颈癌病例都可以通过分子方法检测到HPV的存在。因此,发生CIN和浸润性癌的重要风险因素与HPV暴露直接相关,包括:
● 初次性交年龄较早;
● 多个性伴侣;
● 男性伴侣先前有多个性伴侣;
● 高危型HPV感染持续存在。
虽然HPV感染发生于最不成熟的基底层鳞状上皮细胞,但是HPV DNA复制则发生于其上部相对有所分化的鳞状上皮细胞。正常情况下,成熟阶段鳞状上皮细胞不会复制DNA,但是HPV感染的鳞状上皮细胞可以,结果表达了HPV基因组E6和E7两种有效的癌基因蛋白。E6和E7蛋白分别与两种关键的肿瘤抑制因子p53和Rb结合并使其失活,通过这一作用促进细胞增殖并增加其对附带突变的敏感性,最终导致子宫颈癌的发生。
根据HPV诱导癌变的能力,血清学HPV检测可以将其分为高危型和低危型两类。高危型HPV感染是子宫颈正常上皮发展为CIN和子宫颈癌最重要的风险因子。HPV16和HPV18是两种高危型HPV,大约70%的CIN和子宫颈癌病例都有这两型HPV的感染。一般而言,血清型高危型HPV感染更倾向为持续性感染,其是进展为宫颈癌的一个风险因素。这些HPV亚型也显示有整合到宿主细胞基因组的倾向,这是与疾病进展相关的一个分子事件。从另一方面讲,低危型HPV(例如:HPV6和HPV11)与下生殖道湿疣的发生发展相关(图2),并且不会整合到宿主细胞基因组,而是仍然以游离病毒DNA的形式存在。虽然HPV感染与子宫颈癌具有较强的相关性,但是HPV并不足以掌控肿瘤形成的整个过程。如下所述,一些具有HPV感染的高级别前驱性病变并没有进展为浸润性癌。在子宫颈鳞状上皮异型增生进展为浸润性癌的这一过程中,各种各样的因素都发挥了作用,例如:免疫和激素状态、与其他性传播疾病的共同感染等。最近研究发现,20%以上的子宫颈癌存在肿瘤抑制基因LKB1的体细胞获得性突变。P-J综合征是一种常染色体显性遗传病,特征为胃肠道错构瘤性息肉及不同解剖部位(包括子宫颈)上皮性恶性肿瘤的发生风险显著增加,而LKB1则是P-J综合征中发现的第一个存在突变的基因。LKB1在肺癌中通常也是处于失活状态。LKB1蛋白是一种丝氨酸-苏氨酸激酶,其发生磷酸化并激活AMPK(一种代谢感受器)。反过来,AMPK通过mTOR复合体调控细胞生长。
(1)子宫颈上皮内瘤变
HPV相关性肿瘤的形成从癌前上皮性病变(称之为CIN)开始,到进展为明显的癌症通常需要数年甚至数十年。与此观念一致,CIN的发病高峰为30岁左右,而浸润性子宫颈癌的发病高峰为45岁左右。
CIN通常起始于低度异型增生(CIN1),随着时间的推移进展为中度异型增生(CIN2)及重度异型增生(CIN3);但是,也有一些例外的病例报道,一些患者首次诊断时即为CIN3。一般来说,CIN的级别越高,进展为癌可能性就越大;但值得注意的是,一些病例即使是高级别病变也不会进展为癌,甚至可以发生退变。由于患者的治疗决策是双层式(即临床观察和外科手术),所以这种三层式分级系统最近被简化为双层式分级系统,CIN1命名为低级别鳞状上皮内病变(LSIL),CIN2和CIN3归为一类命名为高级别鳞状上皮内病变(HSIL)。如表1所示,HSIL外科治疗和LSIL临床观察的诊疗决策是基于这两组病变自然病史的差异而定。
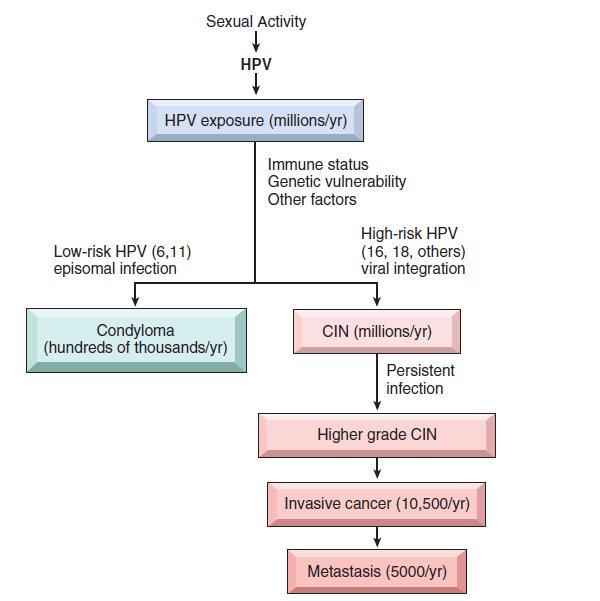
图2 人乳头瘤病毒(HPV)感染所致可能结果。进展与病毒整合以及文中所述的获得性突变相关;CIN,子宫颈上皮内瘤变。

注:LSIL,低级别鳞状上皮内病变;HSIL,高级别鳞状上皮内病变;*10年内进展
子宫颈癌前病变与宫颈细胞学检查(Pap涂片)异常相关,大体检查出现任何异常之前很长的一段时间之内都可以检测到子宫颈细胞学异常。宫颈细胞学检测的理论基础就是对早期异型细胞的检测,在移行区刮取细胞后显微镜下观察。到目前为止,子宫颈细胞学检测仍然是有史以来最成功的癌症筛查方法。在美国,子宫颈细胞学筛查显著的降低了浸润性子宫颈肿瘤的发病率,当前每年新发病例约12000例、死亡病例约4000例;实际上,子宫颈癌已经不再位于美国女性癌症死亡原因前10位。矛盾的是,CIN的发病率已经增加到每年50000例之多,显然是由于宫颈细胞学检测的不断增加所导致。
最近引进的四价HPV疫苗(包括HPV6、11、16、18)对于预防HPV感染非常有效,预期可以大大的降低与这些HPV亚型相关的生殖道湿疣和宫颈癌的发病率。虽然疫苗非常有效,但是其并不能取代常规子宫颈癌筛查,因为许多高危女性已经感染,并且其只能预防诸多致癌性HPV亚型中的一部分。
图3显示了CIN的三个阶段。CIN1的特征为异型性改变位于鳞状上皮下1/3层,挖空细胞样改变位于鳞状上皮表层。CIN2,异型细胞延伸至鳞状上皮中1/3层,并且表现为角质细胞成熟延迟。其也与细胞及细胞核大小变化、细胞核染色质异质性、基底细胞层之上的核分裂象延伸至上皮下中1/3层相关。表层细胞显示有一定程度的分化,偶尔呈挖空细胞样改变。CIN3是子宫颈上皮内病变的下一阶段,显著特征为成熟现象几乎完全缺失、细胞和细胞核大小变化较大、染色质具有异质性、细胞极性紊乱、并可见正常或异常核分裂象,上述变化几乎累及上皮所有层次。通常无挖空细胞样改变。这些组织学特征相对应的细胞学改变如图4所示。如前所述,临床对于CIN的意图就是将其分为LSIL(CIN1)和HSIL(CIN2和CIN3)。
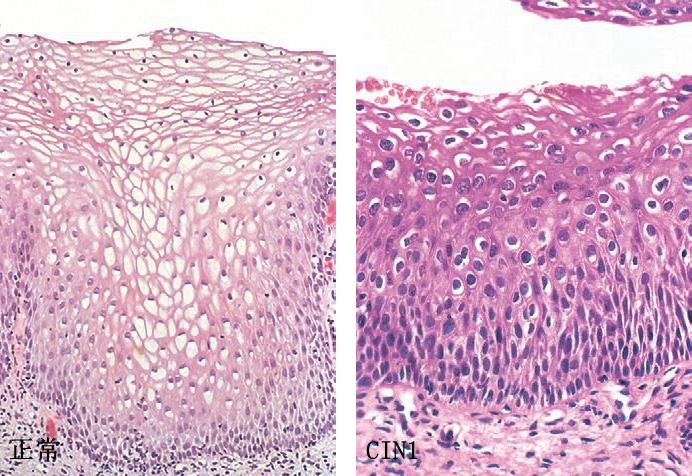

图3 子宫颈上皮内瘤变(CIN)发展谱系(正常鳞状上皮作为对照):CIN1,伴有挖空细胞的异型性改变;CIN2,上皮各层异型性增加;CIN3(原位癌),弥漫性异型及成熟现象缺失。
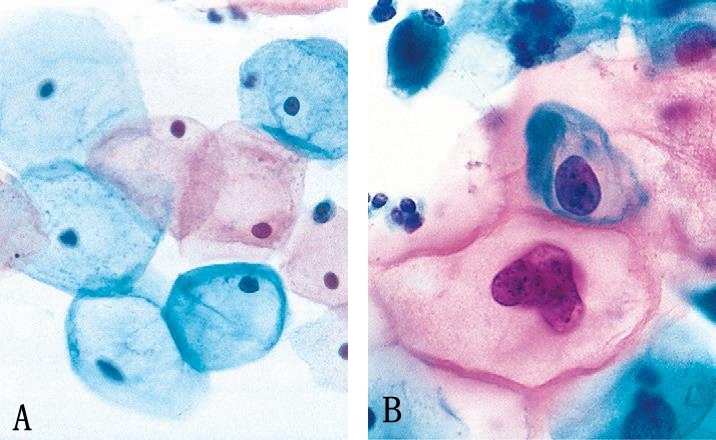
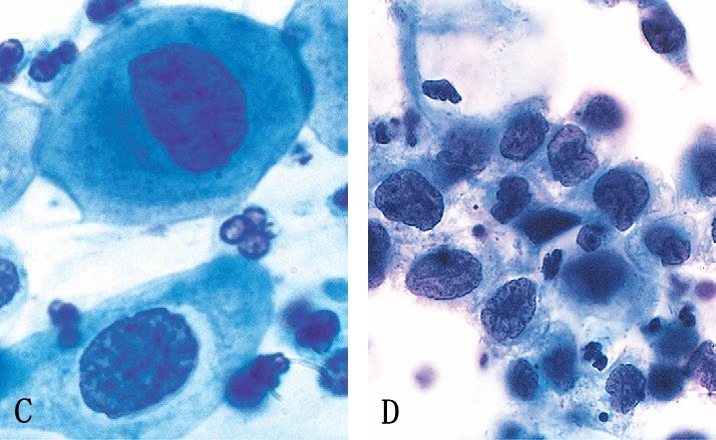
图4 子宫颈细胞学检查子宫颈上皮内瘤变(CIN)的细胞学特征。表层鳞状上皮细胞可以呈红色或蓝色。A:正常脱落表层鳞状上皮细胞;B:CIN1,低级别鳞状上皮内病变(LSIL);C和D:分别为CIN2和CIN3,均为高级别鳞状上皮内病变(HSIL)。随着病变级别的增加,注意胞浆的减少和核浆比的增加。这一现象反应了子宫颈病变表面脱落细胞细胞分化的进行性缺失(图18-6)。(Courtesy of Dr. Edmund S. Cibas, Brigham and Women’s Hospital, Boston, Massachusetts)
CIN无任何症状,只有宫颈细胞学检查结果异常时才会引起临床注意。这些患者随后进行阴道镜检查,检查过程中使用醋酸突显病变部位以及活检区域。活检证实为LSIL的女性可以进行保守性密切随诊,而HSIL需要进行外科切除治疗(锥切活检)。HSIL患者终生需要进行子宫颈细胞学和临床检查随访,因为这些患者仍然具有HPV相关性宫颈癌、外阴癌及阴道癌的发病风险。
2、浸润性子宫颈癌(Invasive Carcinoma of the Cervix)
鳞状细胞癌是最常见的子宫颈癌(75%),腺癌和混合性腺鳞癌(20%)、小细胞神经内分泌癌(<5%)紧随其后。所有这些类型的癌均由HPV感染引起。有趣的是,最近数十年腺癌的相对比例有所增加,这是由于鳞状细胞癌发病率下降以及子宫颈细胞学检查对腺性病变检查并不理想所致。
鳞状细胞癌的发病高峰约为45岁,为发现癌前病变(CIN)后10-15年。如前所述,CIN发展为浸润性癌这一过程多变且不可预测,需要发生HPV感染及有关基因突变(例如:LKB)。病变进展的风险因素包括吸烟和人类免疫缺陷病毒(HIV)感染,对后者的发现提示免疫监视在人体本身控制CIN方面具有一定作用。虽然风险因素对可能由CIN进展为癌的患者分层有所帮助,但是监视疾病进程仅有的、可靠的途径就是常规体检并对疑似病变进行活检。
浸润性子宫颈癌发生于移行区,大小从显微镜下所见的局灶性浸润至大体上明显的外生性肿物(图5)。肿瘤环绕子宫颈且浸润至下方间质而形成桶状子宫颈,这样直接触诊就能发现。延伸至子宫旁软组织可以导致子宫与周围盆腔结构粘连。盆腔淋巴结转移的可能性与肿瘤浸润深度和肿瘤细胞血管转移相关。转移风险从<1%(浸润深度<3mm)增长到>10%(浸润深度>3mm)。除了一些表现为神经内分泌分化的罕见肿瘤外(同样具有侵袭性生物学行为),子宫颈癌都是根据其鳞状分化程度进行分级。
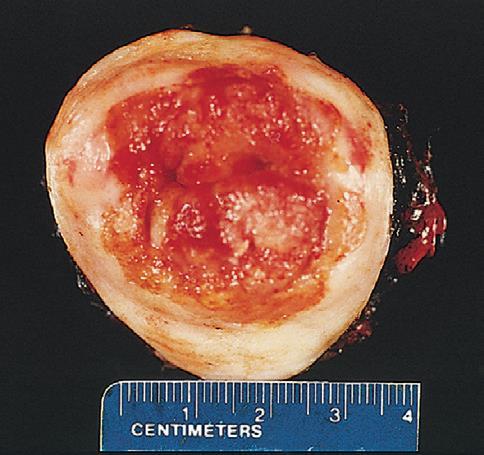
图5 子宫颈口周围浸润性、外生性子宫颈癌
浸润性子宫颈癌最常见于从未进行或许多年未进行宫颈细胞学检查的女性。这些病例中,子宫颈癌患者就诊时通常会出现意外阴道出血、白带过多、性交痛(性交困难)以及排尿困难等症状。治疗方法采用外科子宫切除和淋巴结清扫手术,小的微小浸润性癌的治疗方法可以采用锥形切除。死亡率与肿瘤分期和细胞类型(就“神经内分泌癌”而言)具有显著相关性。大多数癌症晚期患者死于局部浸润(而不是远处转移),特别是膀胱和输尿管梗阻所导致的肾功能衰竭是常见的死亡原因。
● 子宫颈癌风险因素与HPV暴露相关,例如:初次性交年龄较早、多个性伴侣、以及吸烟、免疫缺陷等其他因素。
● 几乎所有子宫颈癌均由HPV感染引起,特别是高危型HPV(HPV16、18、31、33);HPV疫苗对于预防HPV16、18感染有效。
● HPV表达E6和E7蛋白,两者分别能够引起p53和Rb肿瘤抑制基因失活,最终导致细胞增生的增加和DNA损伤诱导细胞凋亡的抑制。
● 子宫颈高级别鳞状上皮内病变(CIN2和CIN3)中,HPV整合到了宿主细胞基因组中。
● 并非所有HPV感染都会进展为CIN3或浸润性癌。从HPV感染发展为浸润性病变这一时间过程通常需要10年或更长时间。一般来说,进展风险与异型程度成正比。
● 子宫颈细胞学检查是子宫颈异型增生和癌的检测方法中非常有效的筛查工具,显著降低了子宫颈癌的发病率。
3、子宫颈息肉(Endocervical Polyp)
子宫颈息肉是一种良性的、子宫颈内黏膜(有时为子宫颈外黏膜)突出的息肉状肿物。它们可以有数厘米大小,质地柔软且易触摸到,表面光滑、有光泽,下方为囊性扩张、充满黏液性分泌物的腔隙。表面上皮及其下方囊腔所衬覆上皮均由与宫颈管相同的黏液分泌性柱状上皮细胞组成。间质水肿,可见散在单核细胞。叠加慢性炎症可以导致所衬覆上皮和溃疡的鳞状上皮化生。这些病变可以引起出血,因此会引起注意,但是它们没有恶性潜能。
参考文献:
Vinay Kumar, Abul K. Abbas, Jon C. Aster. Robbins Basic Pathology(第9版),681-685.
推荐阅读:
连载 | (一)外阴和阴道肿瘤及非肿瘤性病变





















共0条评论