[导读] 作者:赵东晖
病史:
患者,男,42岁,发现左颈部肿物1年余,大小约4×3×3cm,无其他不适。临床考虑:颈部淋巴结炎?转移癌?
影像检查:
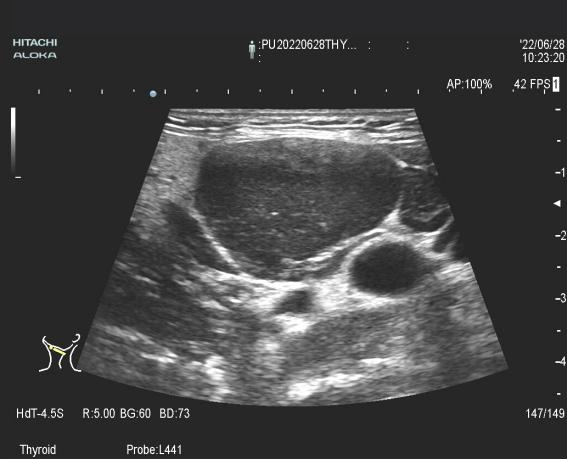
双侧颈部淋巴结肿大,内可见数个低回声团,其中两个较大淋巴结分别为36×26×8mm、30×26×9mm,椭圆形,边界清,部分淋巴门消失。

病理检查:
大体:穿刺活检组织4条,长约2cm,全取。
镜下:
HE:淋巴结穿刺活检组织:
1.低倍镜下看到模糊的结节轮廓,结节偏大一些,似滤泡性淋巴瘤的结节,小淋巴细胞,主要是套细胞进入结节里面,符合生发中心进行性转化;
2.本来结节里生发中心都应该是中心母细胞、中心细胞,现被这些小淋巴细胞所代替,且在小淋巴细胞的背景中可以看到“爆米花”细胞,是形态学特征;
3.背景细胞单一,浆细胞、嗜酸性粒细胞及中性粒细胞无或少见,见组织细胞,上皮样,伴血管增生及纤维化。
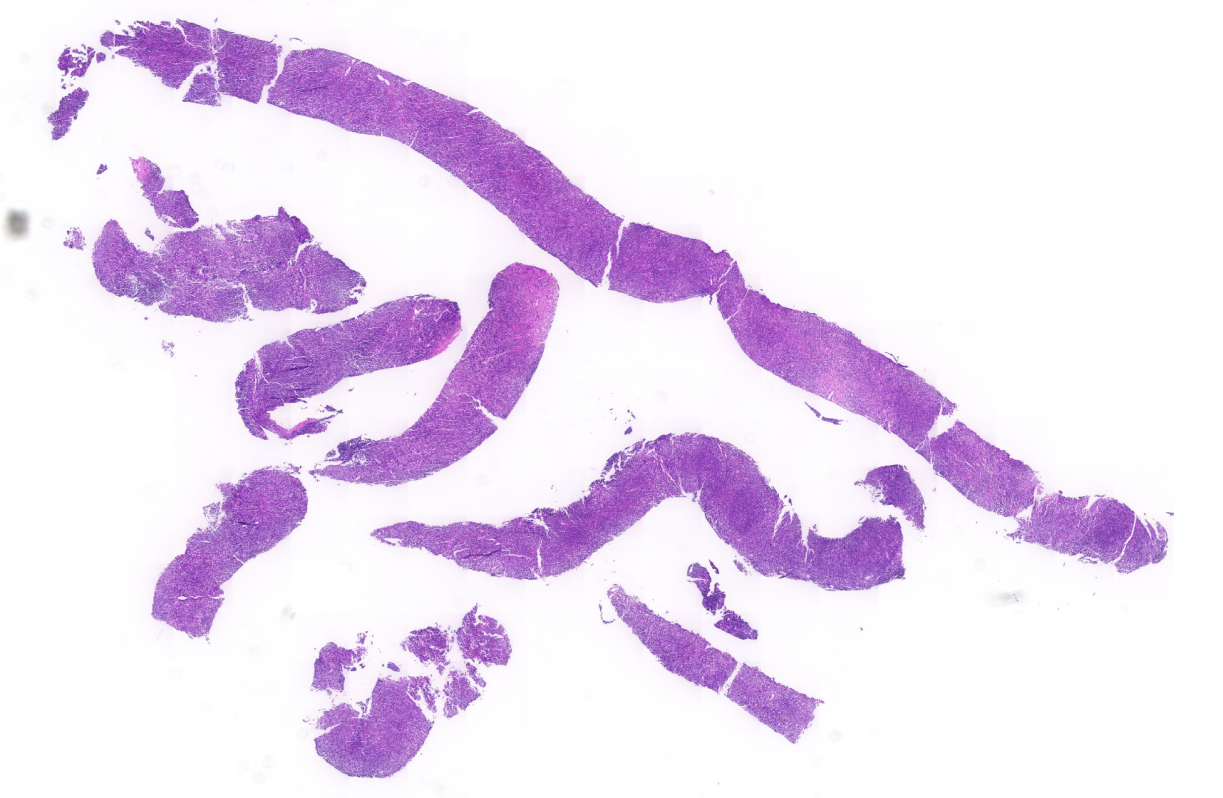
淋巴结穿刺活检组织多条,破碎,淋巴结结构不完整
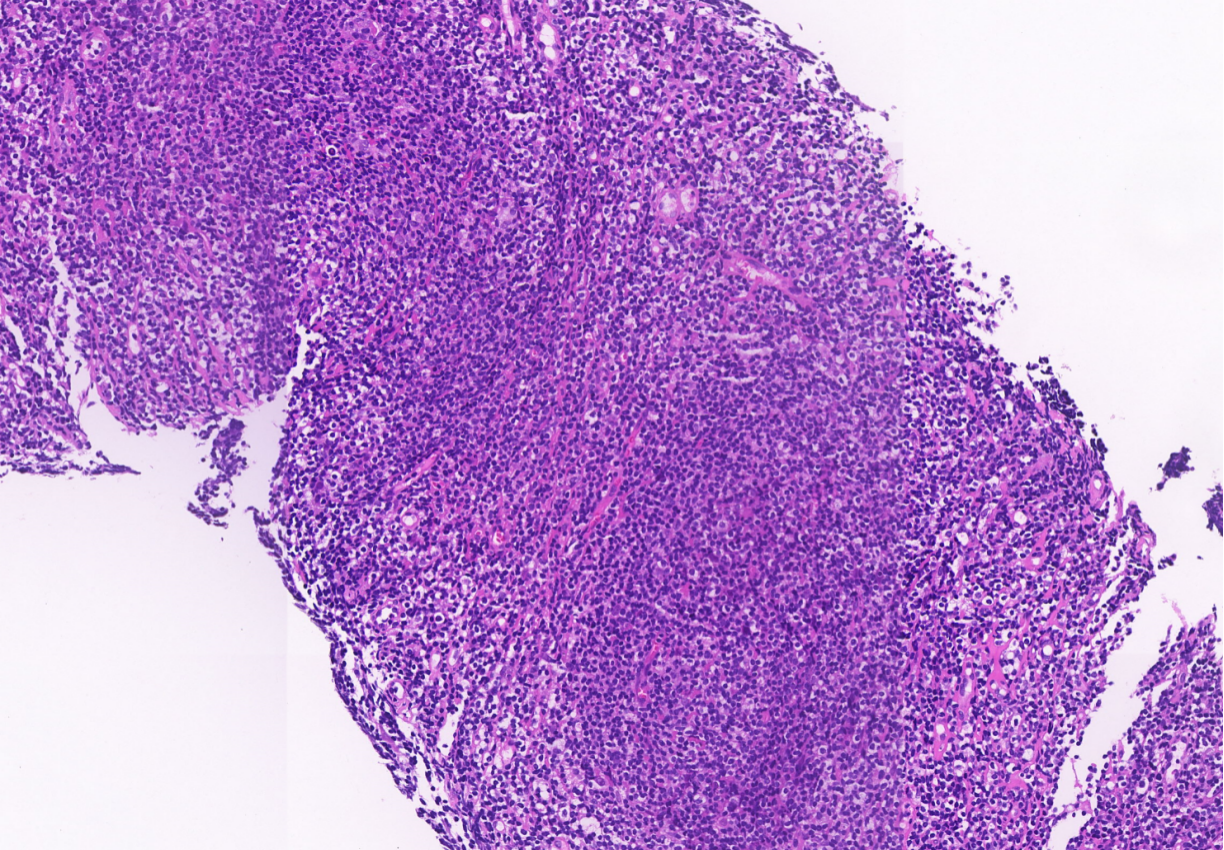
可以看到模糊的结节轮廓,较大,似滤泡性淋巴瘤的结节,外面有好多小淋巴细胞都进入结节里面,呈生发中心进行性转化改变
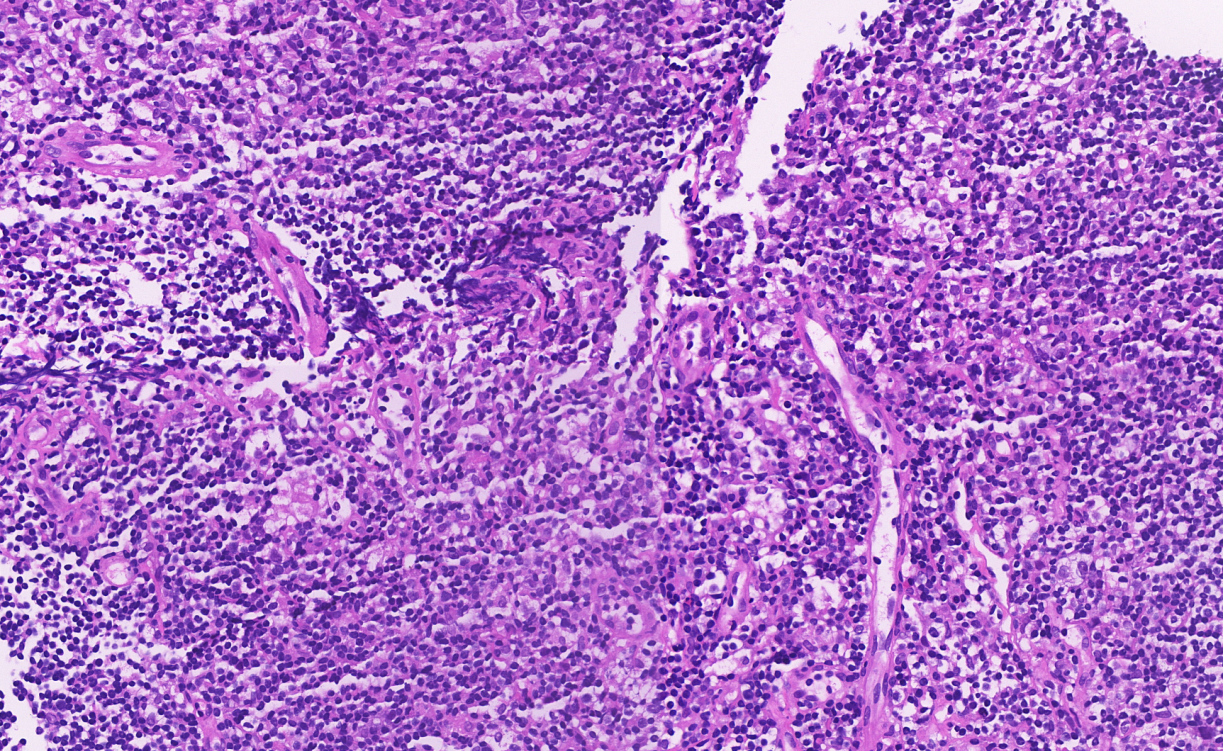
伴血管增生
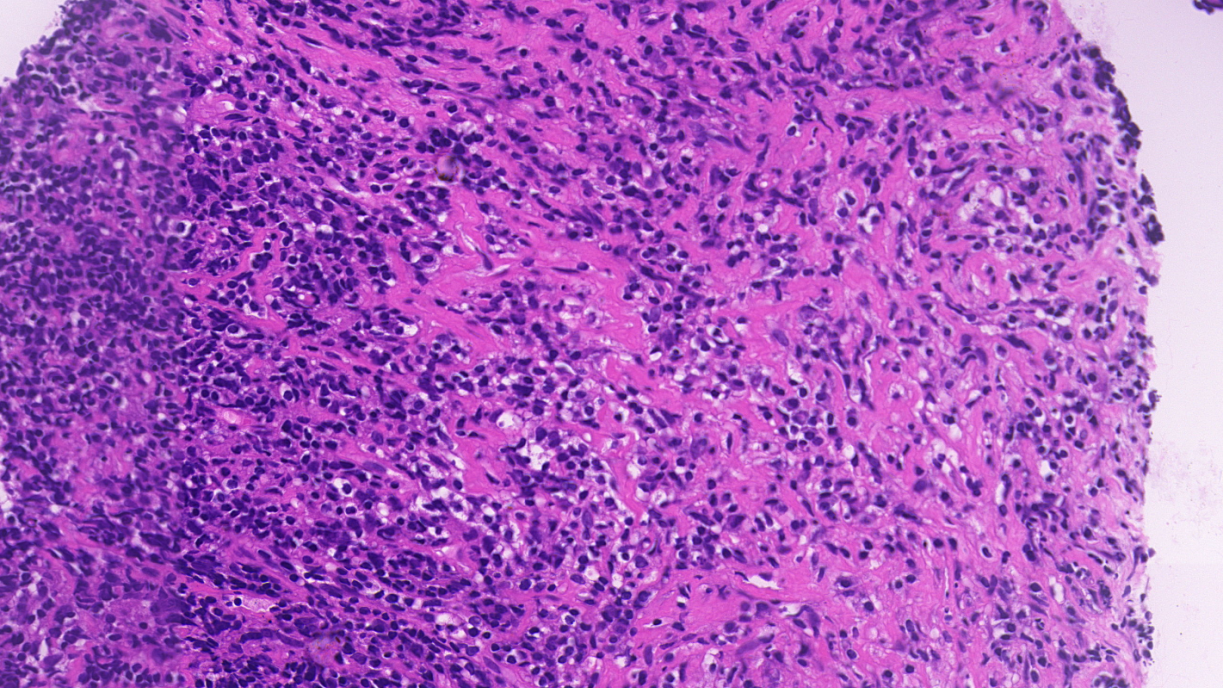
伴纤维化
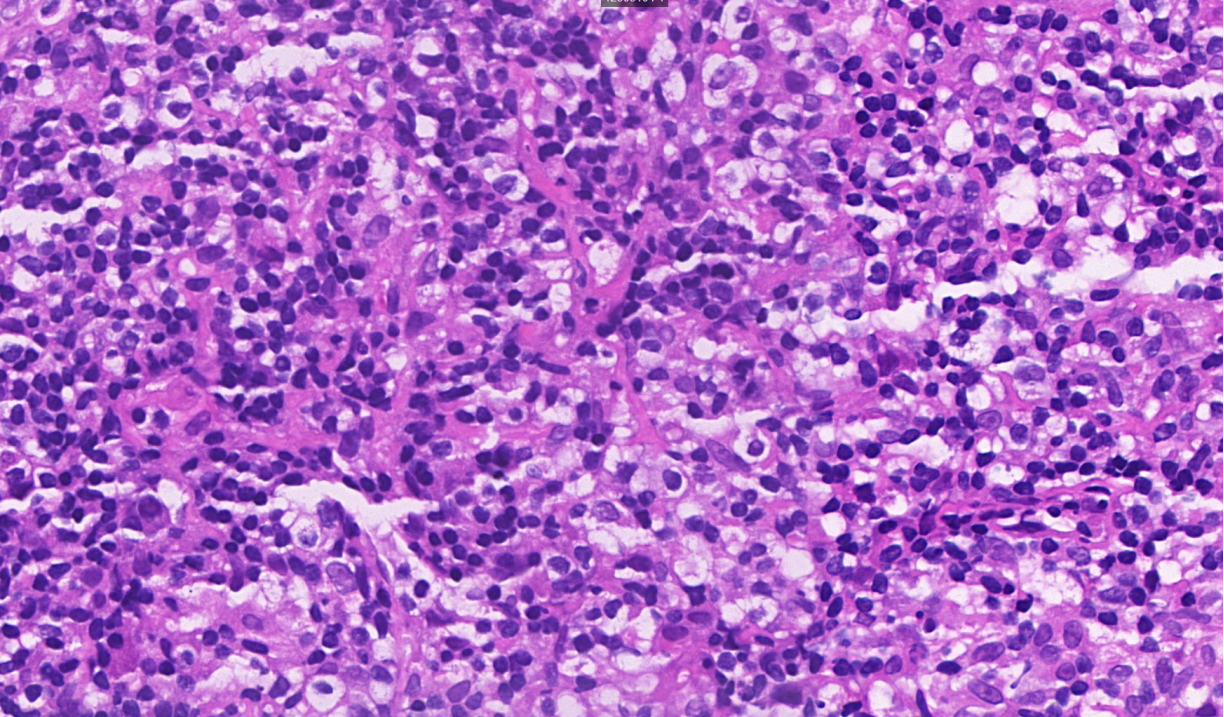
背景见上皮样组织细胞
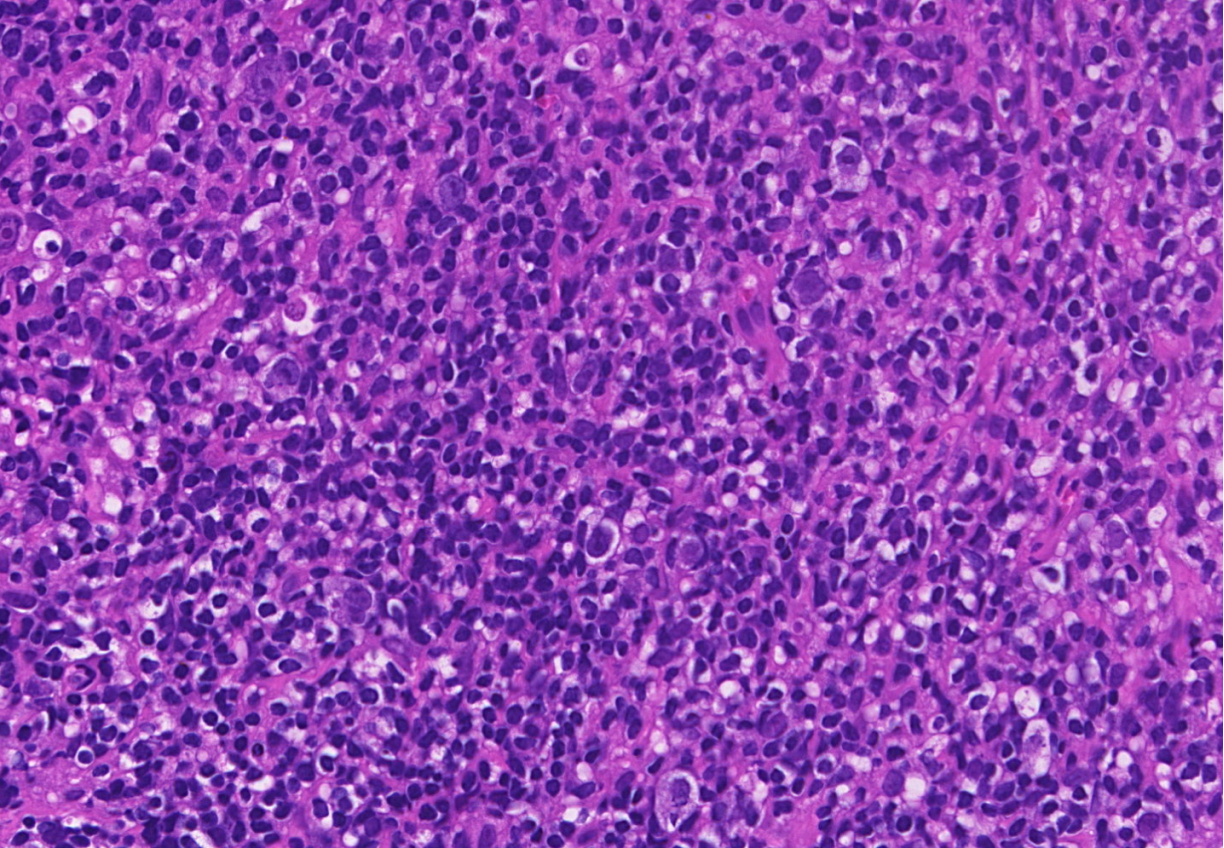
本来结节内生发中心应该是中心母细胞、中心细胞,现被这些小淋巴细胞所代替,在小淋巴细胞的背景中可以看到“爆米花”细胞,是特征性形态学改变,“爆米花”细胞(LP细胞)周围见小淋巴细胞围绕
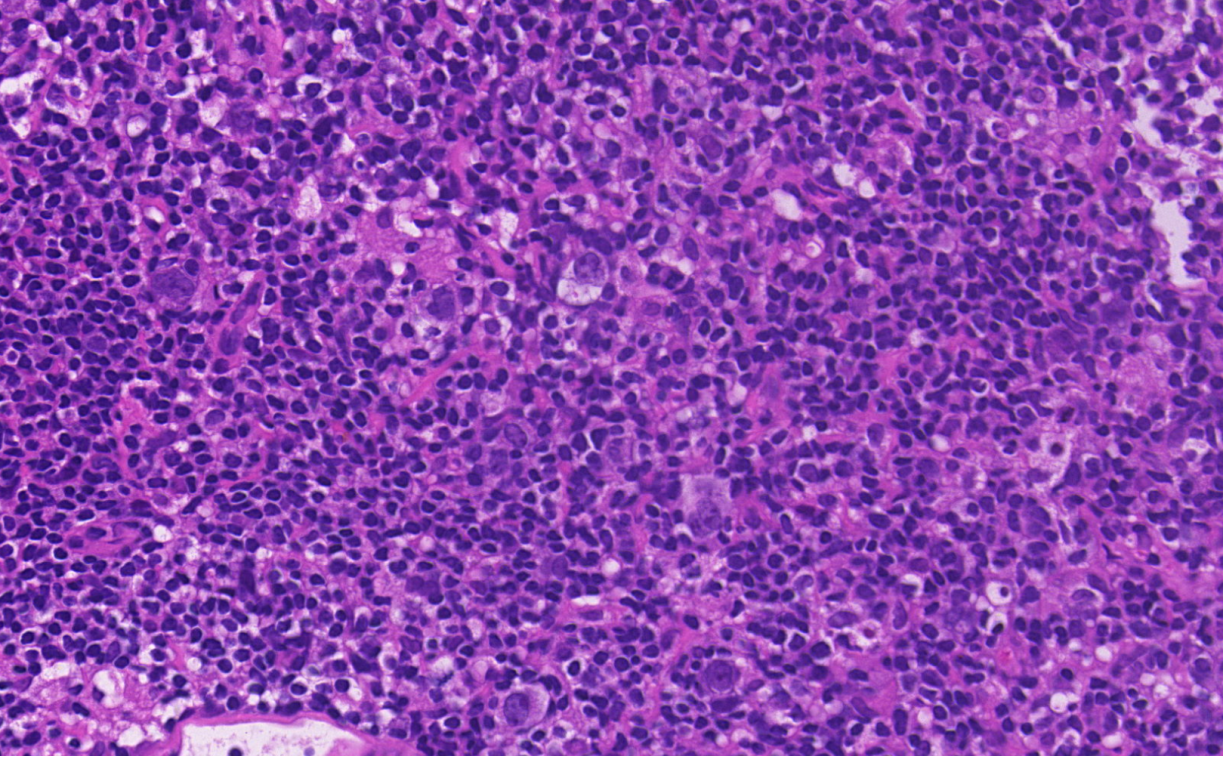
LP细胞:体积大,通常有一个大核、细胞质少,核常重叠或分叶,呈爆米花样,也可以见多个核仁,嗜碱性
IHC结果:
1.CK(AE1/AE3)(-),CD15(-);
2.CD20(+),CD79a(+),Bcl-2(+),Bcl-6(+),Bob.1(+),Pax-5(+),CD30少量弱(+),Ki67约20%(+),CD45(+),EMA少量弱(+);CD3和CD5在大细胞周围形成T花环;CD21显示FDC网松解;
3.原位杂交结果:EBER(-)。
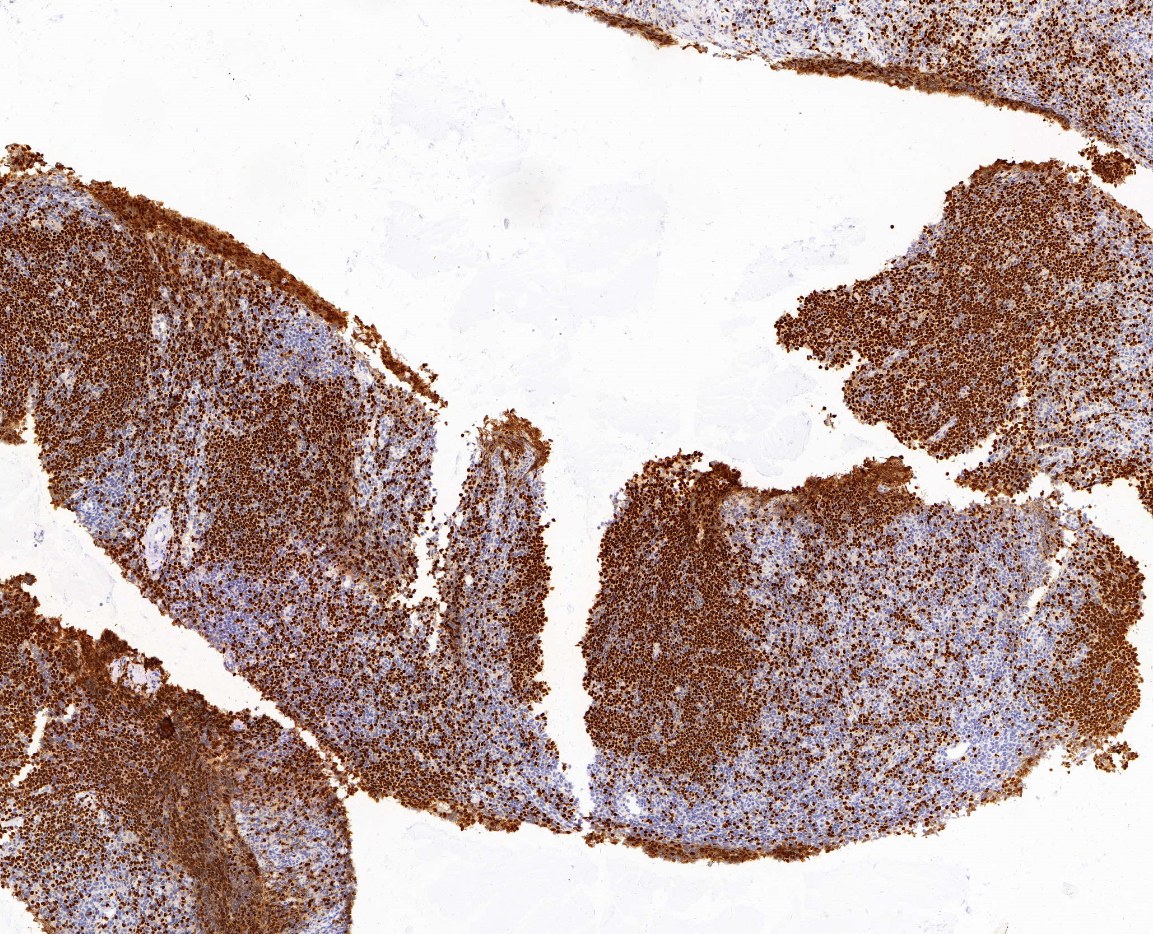
Pax-5勾勒出增大滤泡样结节
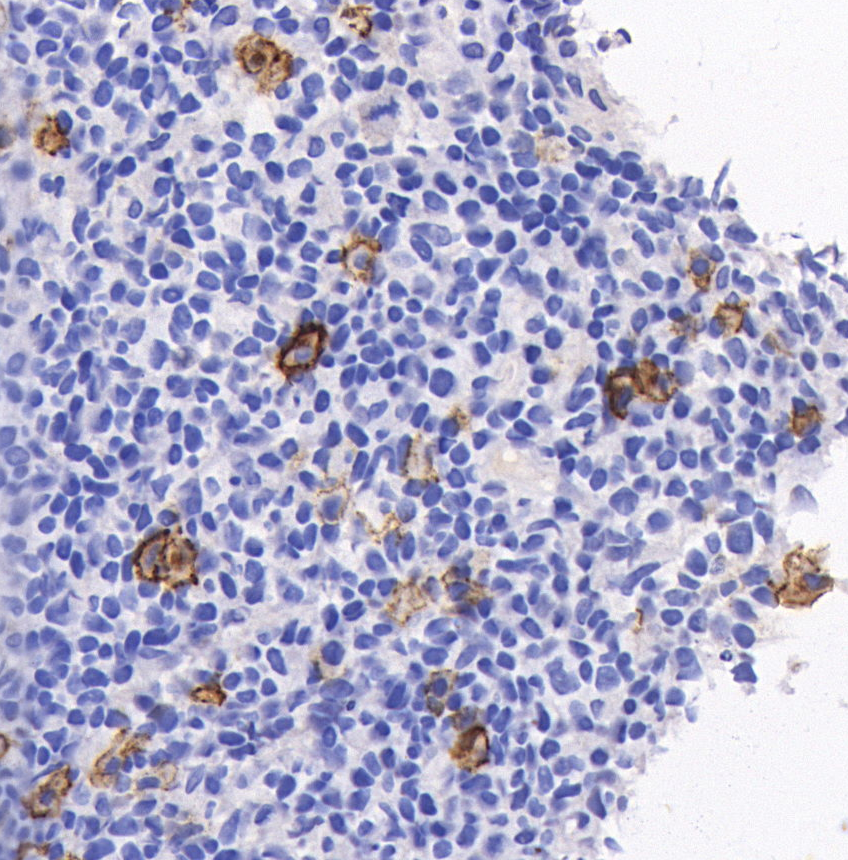
EMA(爆米花细胞+)
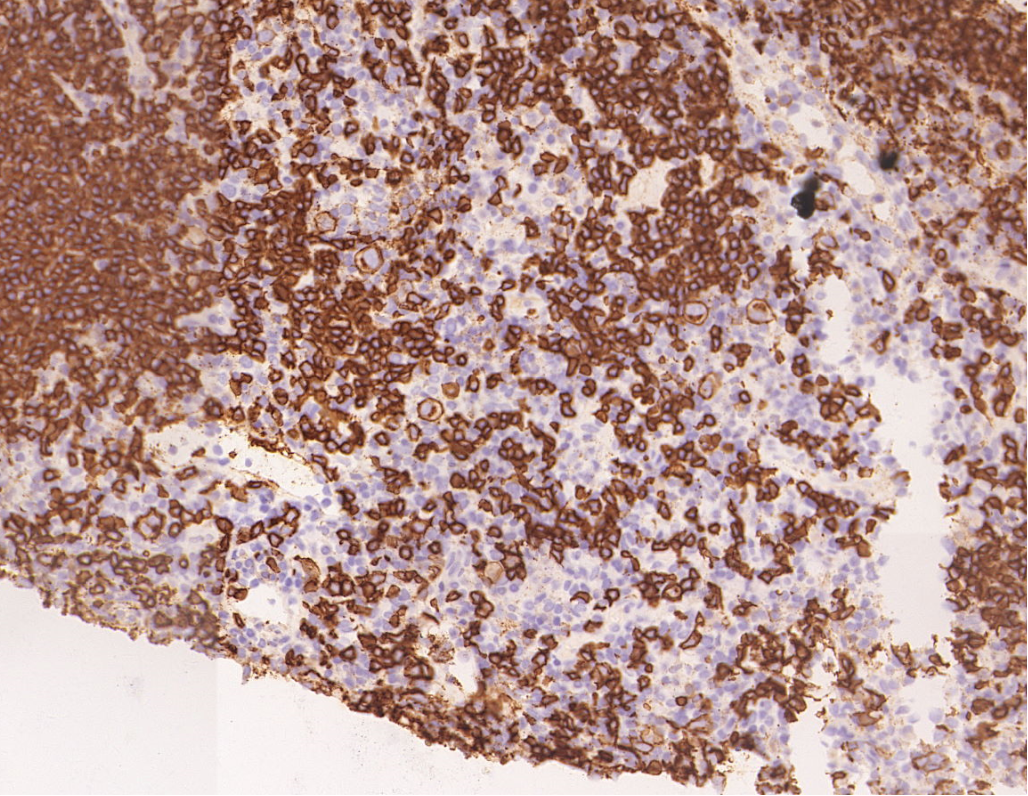 CD20(爆米花细胞+)
CD20(爆米花细胞+)
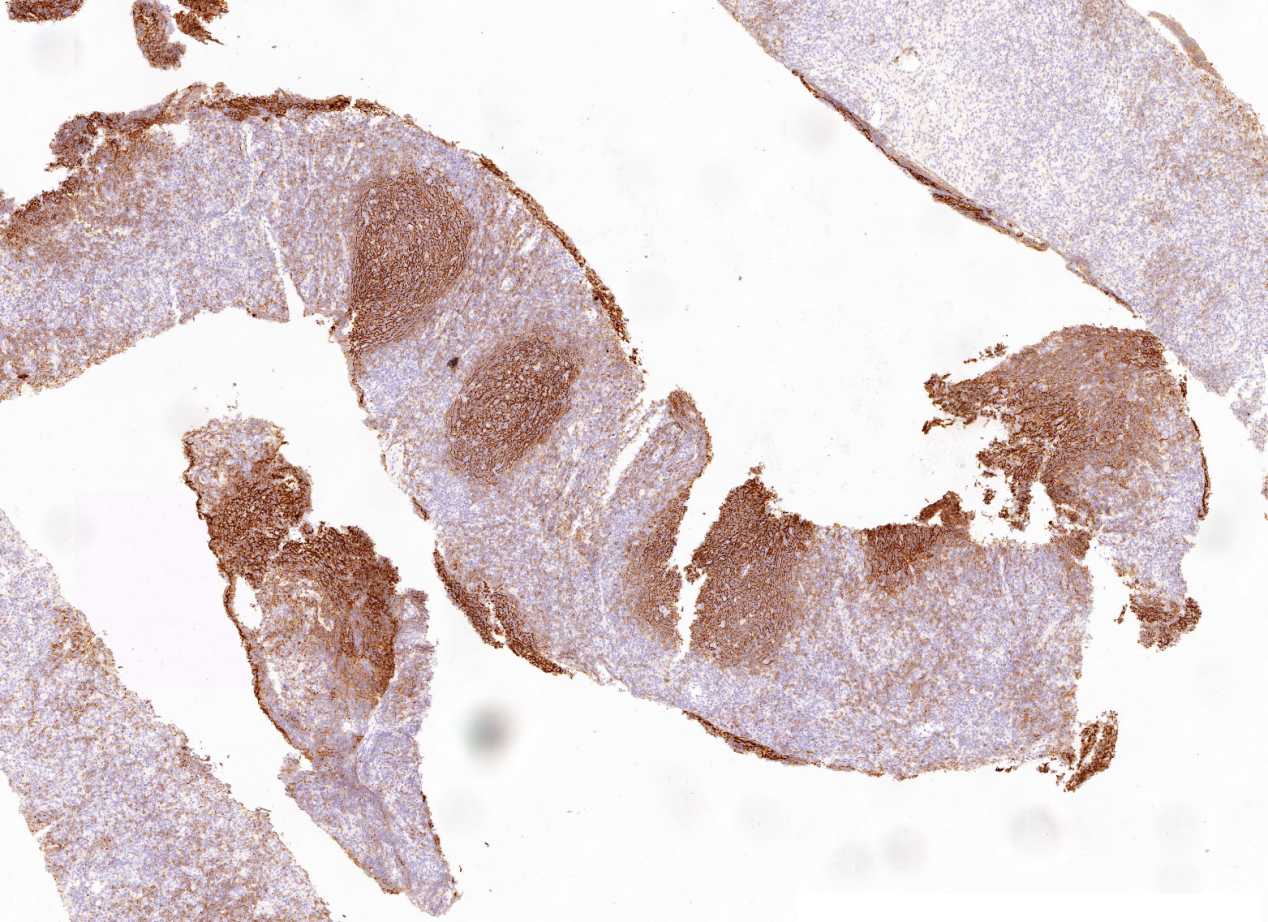
CD21(滤泡样结节内FDC+)
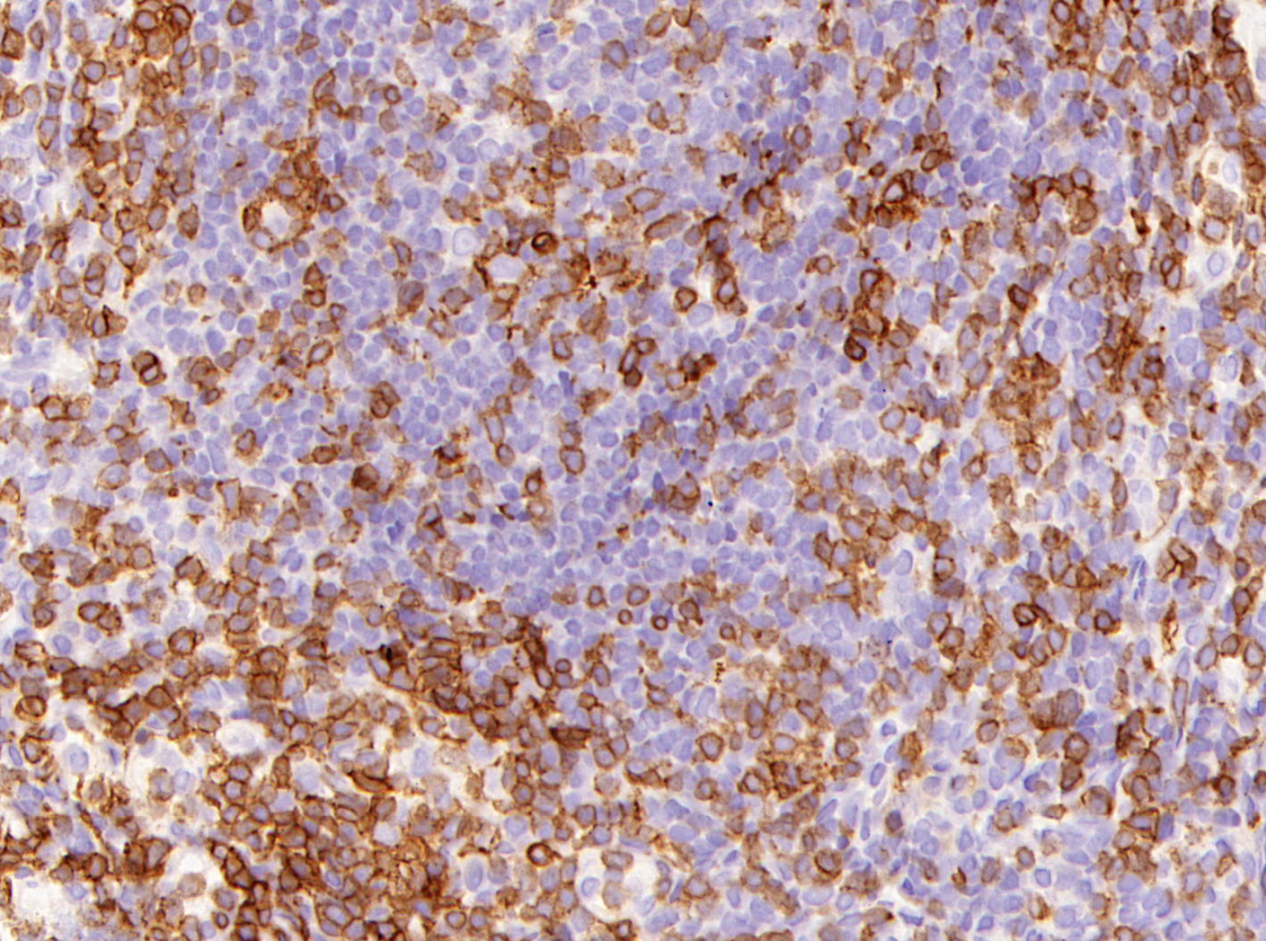
CD3(爆米花细胞周围T花环)
病理诊断:
结合免疫组化结果,(左侧颈部II区淋巴结,穿刺组织)符合结节性淋巴细胞为主型霍奇金淋巴瘤(非经典型霍奇金淋巴瘤),活检组织量少,建议完整切除淋巴结综合诊断。
讨论:
1.结节性淋巴细胞为主型霍奇金淋巴瘤(nodular lymphocyte predominant Hodgkin lymphoma, NLPHL )约占所有HL的5%,可发生于各年龄组,最常累及年轻成人(30-50岁,平均40岁),男性多见,M:F=3:1;常累及颈、腋下或腹股沟淋巴结,纵隔、脾、骨髓受累少见,多数表现为局部淋巴结肿大,除非转化DLBCL后常有B症状,如发热、体重减轻和盗汗等;临床呈惰性经过,预后好。
2.NLPHL淋巴结结构部分或完全破坏,其浸润方式呈多种形成良好的结节状表现,以至其低倍镜下表现与滤泡性淋巴瘤相似。但结节在大小和染色上不一致,并且由于其淋巴细胞和上皮样细胞混合存在,使其呈现斑驳状外观。NLPHL的结节周边见进行性转化的生发中心。嗜酸性粒细胞、浆细胞和纤维化病灶少见或缺如。结节里生发中心被这些小淋巴细胞所代替,在小淋巴细胞的背景中看到瘤细胞。
3.优势细胞为不规则的、中等大小的B淋巴细胞(也就是LP细胞,LH或“爆米花”细胞),伴有或不伴有形态良性的组织细胞,高内皮毛细血管后微静脉可能很显著。LP细胞体积大,通常有一个大核、细胞质少,核常重叠或分叶,呈爆米花样,也可多个核仁,嗜碱性,较典型HRS细胞核仁小。
4.LP细胞最常见于结节内,伴有扩大的滤泡树突状细胞网,但也可向结节间区溢出。LP细胞偶尔以结节边缘分布为主,它们也可表现为大片聚集,形似DLBCL。
5.如果要确认并与其他淋巴瘤区分开,加做IHC,确定“爆米花”细胞是B细胞,CD20、CD79a、CD45(LCA)、PAX5、OCT2均阳性基本上都是阳性;常表达上皮膜抗原(EMA),但一般缺乏CD30和CD15表达。结节内LP细胞常被滤泡辅助T(TFH)细胞菊形团样环绕,这些细胞表达CD3、PD1、BCL6 和CD57。而经典Hodgkin淋巴瘤只有少数病例是CD20阳性。
6.背景中CD57染色显示阳性T细胞比反应性淋巴滤泡里要多得多,可以看到CD57阳性细胞围绕这些大细胞现象,具特征性。
7.NLPHL应与经典型霍奇金淋巴瘤明确区分开,偶尔可同时存在。
NLPHL多种生长模式概括:
可基于这些生长模式概括,进行鉴别诊断。
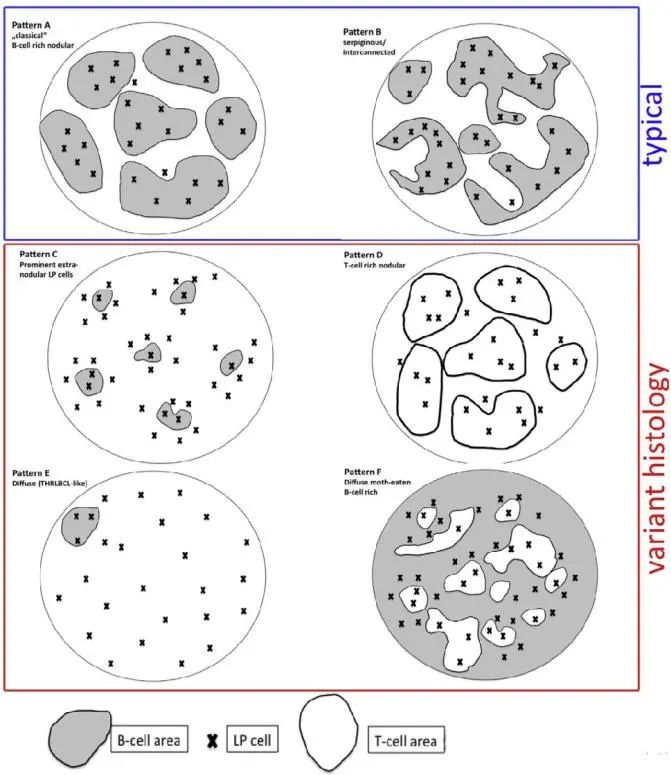
模式A:最常见,经典的结节状结构(富含B细胞)
模式B:匍行样/互连结节
模式C:结节外大量LP细胞
模式D:富于T细胞的结节
模式E:富于T细胞/组织细胞的大B细胞淋巴瘤(THRLBCL)样型
模式F:弥漫性,富于B细胞,伴有虫蚀样外观
治疗:
1.无临床不良预后因素的I-IIA期患者首选单纯放疗(30Gy)。
2.IB-IIB期或有临床不良预后因素的I-IIA期患者可采用化疗±利妥昔单抗±放疗。
3.III-IV期根据临床判断采用化疗±利妥昔单抗±放疗或利妥昔单抗,化疗方案可选择 ABVD、CHOP、CVP方案。
4.治疗采用PET-CT评估,如缓解且无症状则观察,以前未行RT(放疗)可考虑RT,如疾病稳定或进展则需进行活检,活检结果阴性且无症状可继续观察,活检结果阳性则参考以下复发难治患者治疗方案。
5.NLPHL复发难治性患者:对疑似复发者推荐重复PET/CT或诊断性CT评估,再重新进行活检以排除转化为侵袭性B细胞淋巴瘤的可能。复发时病变局限者可应用利妥昔单抗单药治疗,病灶广泛者可选择利妥昔单抗联合二线挽救方案治疗。
分子遗传学:
显微切割分析显示,NLPHL的肿瘤(L&H/LP)细胞有免疫球蛋白基因克隆性重排,并显示为高频突变和进行性突变。
参考书籍及文献:
1.《罗塞和阿克曼外科病理学》第11版,下卷。主译:回允中。副主译:李挺,柳剑英,沈丹华,石雪迎,薛卫成。北京大学出版社。
2.《中国霍奇金淋巴瘤的诊断与治疗指南》(2022年版),中国抗癌协会血液肿瘤专业委员会,中华医学会血液学分会,中国霍奇金淋巴瘤工作组。




























共0条评论