[导读] 作者:游乐园
1、病例资料:患者男性,69岁。患者2周前因乏力就诊当地医院,腹部CT提示肝右叶占位,恶性可能。患者自诉偶有肝区疼痛,可忍受。查体:神志清楚,全身皮肤黏膜及巩膜无黄染,右上腹轻压痛,余腹无压痛及反跳痛,双下肢无水肿。检验项目:ALT 42.4U/L,AST 45.1U/L,GGT 281.0U/L。上腹部MRI:平扫肝右叶实质内见类圆形T1WI及T2WI混杂信号囊性灶,边缘清楚,大小约128.4x150.6mm,内部见多发絮片状T1WI高信号影,T2WI示灶内多发分隔样改变,临近局部肝内胆管受压轻度扩张。行肝右叶切除术以明确诊断。显微镜下见肿瘤由形态多样的未分化间叶细胞及疏松黏液样基质构成,瘤细胞排列成片状或束状,细胞异型明显,核分裂象易见,局部见瘤巨细胞,在瘤细胞的胞质内或胞质外基质中可见嗜伊红小体,局部见纤维性假包膜、出血及坏死。免疫组化:Vimentin、Desmin阳性,CK、Glypican-3局灶阳性,余HepPar1、AFP、SMA、S-100、CD68、CD56、Myogenin、Syn、LCA、CK7、CD117、HMB-45和CD34均阴性。病理诊断:(肝右叶)胚胎性肉瘤。
2、讨论:肝脏胚胎性肉瘤(embryonal sarcoma of the liver,ESL)是一种少见的间叶组织来源的高度侵袭性恶性肿瘤。1978年首次报道并命名为未分化(胚胎性)肉瘤,WHO2019第五版消化系统肿瘤分类不再使用这一名词,改用胚胎性肉瘤这一术语。ESL好发于儿童,在各种类型的儿童肝脏肿瘤中占9%-13%,发生率仅次于肝母细胞瘤和肝细胞癌,居儿童恶性肿瘤的第3位。ESL好发年龄为5-15岁,成人ESL罕见,在成人原发性肝肿瘤中占比不足1%。本病无种族差异,在儿童中无明显性别差异,在成人中女性略占优势。
组织起源:ESL的病因和发病机制尚不完全清楚。有研究表明ESL与肝间叶性错构瘤(MH)恶变具有相似的细胞遗传学异常,即19q13.4的染色体重排,提示ESL可能来源于间叶性错构瘤的恶性演变。当ESL组织学特征存在MH样区域以及MH样区域与典型ESL区域之间的过渡区,间叶细胞恶性转化的过程提示ESL起源于MH。因此,在临床实践中需对MH的不同部分进行取材,以排除恶性转化的区域。ESL可伴有1q、5p、6q、8p、11p、14p和12q染色体的扩增或缺失。拷贝数改变在ESL中很常见,但无特定的拷贝数变化,猜测可能与肿瘤的异质性相关。6、11、12、14和x染色体的畸变和TP53基因突变也有少数报道,TP53基因突变的位点包括K120M、V216M等,这可能成为ESL潜在的治疗靶点。患者一般无乙肝、肝硬化等肝病背景,少数成人患者可合并系统性硬化症、恶性肿瘤化疗史等。既往有文献报道部分ESL患者有肝炎病史,故本病的发生与肝炎的关联有待于进一步探讨。
临床表现:ESL的临床表现隐匿,缺乏特异性,容易误诊。临床表现通常为上腹不适、腹部包块、腹胀腹痛、腹泻便秘、恶心、呕吐、厌食、消化不良、黄疸,在某些情况下还伴有发热、体重减轻及嗜睡等全身症状,其中腹痛和发热可能由瘤体出血、坏死引起。有少数患者在诊断时无症状或因瘤体自发破裂出血表现为急腹症而就诊。5%-15%的患者可出现肝外转移,常见的转移部位包括肺、膈肌、心脏和腹膜,成人患者较儿童患者更易发生远处转移。实验室检查无特异性,肝酶和血清肿瘤标志物一般正常,少数病例可表现为白细胞、谷氨酰胺转肽酶、乳酸脱氢酶、AFP、CA125、CA199升高、低白蛋白和贫血。
影像学检查:儿童ESL多表现为巨大囊实性肿块,囊性为主,边界较清,增强后实性成分及分隔轻中度强化,具有一定的特异性表 现,而成人ESL多表现为实性或实性为主的囊实性肿块,边界不清,浸润性强,可多发,可伴出血,也可发生转移,增强呈花环状或环形强化,此类征象均指向恶性肿瘤,与肝细胞肝癌的典型影像学表现不同,但与胆管细胞癌、转移瘤等其他恶性肿瘤鉴别困难。ESL的形态、密度、血供和强化模式复杂多变,其发病机制尚不清晰,可能涉及多种因素,包括基因突变、胚胎发育异常和分化异常等。ESL复杂多变的影像学表现可能与其组织细胞学特性及不同的生长方式有关。ESL影像学表现可能的病理生理机制包括: (1)ESL的细胞学特点是呈未分化状态,由于肿瘤细胞缺乏正常肝细胞的分化特性,这可能导致肿瘤在影像学上可以呈现出实性的密度或信号。(2)ESL内部存在坏死和囊变区域为黏液样基质,这些区域在影像上呈现出低密度或囊性信号,与实性成分形成对比,坏死区域通常与肿瘤的快速增殖和供血不足有关。
组织病理学:肿瘤由未分化的间充质细胞和疏松的黏液样基质组成,伴出血和坏死。肿瘤细胞具有明显异型性和多形性,多呈梭形、卵圆形或星芒状,可见散在少量分布的瘤巨细胞和核深染的奇异细胞。核分裂象多见,肿瘤细胞胞质内和细胞外基质中可见嗜酸性小体,PAS染色阳性。肿瘤细胞分布疏密不均,致密区可排列成恶性纤维组织细胞样、纤维肉瘤样、血管内皮瘤样或横纹肌肉瘤样,疏松区则细胞稀少。瘤细胞以膨胀性生长为主,在肿瘤与邻近肝实质的交界处可形成纤维性假包膜。多发性血管浸润和局部纤维包膜浸润到肝包膜往往提示预后不良。少数病例可见小圆细胞和髓外造血。ESL的大多数超微结构研究显示其成纤维细胞或纤维组织细胞分化,电镜下可见粗面内质网扩张和电子致密物沉积,这些电子致密物对应组织学上的嗜酸性小体。也有研究描述了ESL脂肪源性和肌源性的分化。
ESL无特异性的免疫组化标记,联合检测免疫组化标记是非常必要的,排除其他肿瘤的同时提高 ESL的诊断准确性。大多数ESL表达Vimentin、Desmin、α1-AT、BCL2、CDl0、CD56、CD68,局灶性或点状表达CK,通常不表达HepPar1、AFP、SMA、S-100、ALK、 Myogenin、Syn、CD117、HMB-45和CD34,但这些标志物可用于与其它肿瘤的鉴别。Glypican-3在部分病例中表达,因此无法鉴别ESL与肝母细胞瘤和肝细胞癌。
鉴别诊断:(1)肝细胞癌:多数具有肝炎病史,并伴有不同程度的肝硬化。当肝细胞癌分化较低或呈肉瘤样形态时,需与ESL鉴别。肝细胞癌免疫组化染色表达HepPar1、AFP、Glypican-3。(2)肝母细胞瘤:3岁以下儿童多见,由胚胎或胎儿肝细胞及原始间叶细胞构成,在临床上表现为肝脏迅速增大的肿块,且均以肝右叶多见,伴有AFP升高。与ESL不同的是,大体上常表现为实性肿块,组织学主要表现为不同分化阶段的肝组织,同时表达AFP、HepPar1、GPC3等标志物。(3)间叶性错构瘤:好发于2岁以下的儿童,临床上表现为肝脏迅速增大的囊性包块,肿瘤由上皮及间叶两种成分构成。上皮成分主要由肝细胞团和大小不等的胆管及簇状小管构成,间叶成分主要由疏松结缔组织、小血管和炎细胞组成,间质水肿或黏液样变,细胞异型性不明显。(4)胚胎性横纹肌肉瘤:5岁以下儿童多见,临床上通常表现为梗阻性黄疸,镜下原始间叶性细胞具有不同程度的横纹肌母细胞分化,肿瘤细胞呈梭形或星形,散在分布于粘液样基质中,胞质少,核小而深染,免疫组化表达MyoD1和Myogenin。(5)黑色素瘤:是一种形态异质性的肿瘤,有时仅从组织学上与ESL鉴别困难,但黑色素的存在和黑色素细胞标志物(包括SOXl0、HMB45、Melan-A和S-100)的表达有助于鉴别诊断。(6)胃肠道间质瘤(GIST):肝脏是GIST的好发转移部位,肝脏转移性GIST根据临床病史或原位肿瘤情况鉴别诊断较容易。原发于肝的GIST罕见,肿瘤细胞间变性较少,免疫组化表达DOG-1、CDll7和CD34。(7)其它高级别肉瘤:未分化多形性肉瘤、黏液样脂肪肉瘤、平滑肌肉瘤、血管肉瘤,可根据特异性细胞谱系分化的组织学或免疫组化证据进行鉴别。
治疗:由于ESL侵袭性强,大多数患者在就诊时肿瘤体积已巨大,易出现复发或远处转移,总体治疗效果不佳,预后较差。目前普遍认为,以完整切除肿瘤为基础的综合治疗是肿瘤长期生存的关键。ESL多不伴发肝硬化等肝病,且多为单发,有完整包膜。因此,即使肿瘤过大,只要肝功能正常,就应尽早手术切除。但是,术中常因肿瘤体积大,切除范围并不能达到无瘤标准,因此手术前后常联合辅助或新辅助化疗来改善患者预后。对于体积巨大的肿瘤,术前辅助化疗能使肿瘤缩小,从而提高手术切除率。有研究回顾性分析了67例ESL患者的治疗效果,术后1、2年生存率分别为61%、55%,中位生存期为29个月(1-204 个月),肿瘤完整切除后行辅助化疗较单纯手术切除能显著延长患者生存期(P=0.002),前者的中位生存期达27.5个月,而后者在平均随访8个月后迅速出现肿瘤复发,肿瘤切除不完整与不良预后明显相关。但成人患者接受化疗的频率较儿童低,成人患者的死亡风险明显高于儿童患者。成人患者的预后较差,也可能反映了疾病生物学的差异。由于ESL瘤体血供较少且体积大,单纯肝脏射频消融术或TACE治疗常不能取得理想效果。术前经导管动脉化疗栓塞(TACE)和全身化疗等新辅助治疗(NAT)可有效缩小肿瘤体积,清除肿瘤边缘,提高根治性切除率,延长术后生存期。另外,对于肿瘤完整切除术后复发、既往化疗耐药后不无法手术切除、无肝外转移的患者,肝移植是一种合理的替代治疗方法。然而,由于ESL的发病率较低,目前病例数仍较少,各种综合治疗的标准和效果尚需进一步验证。
病例图片:
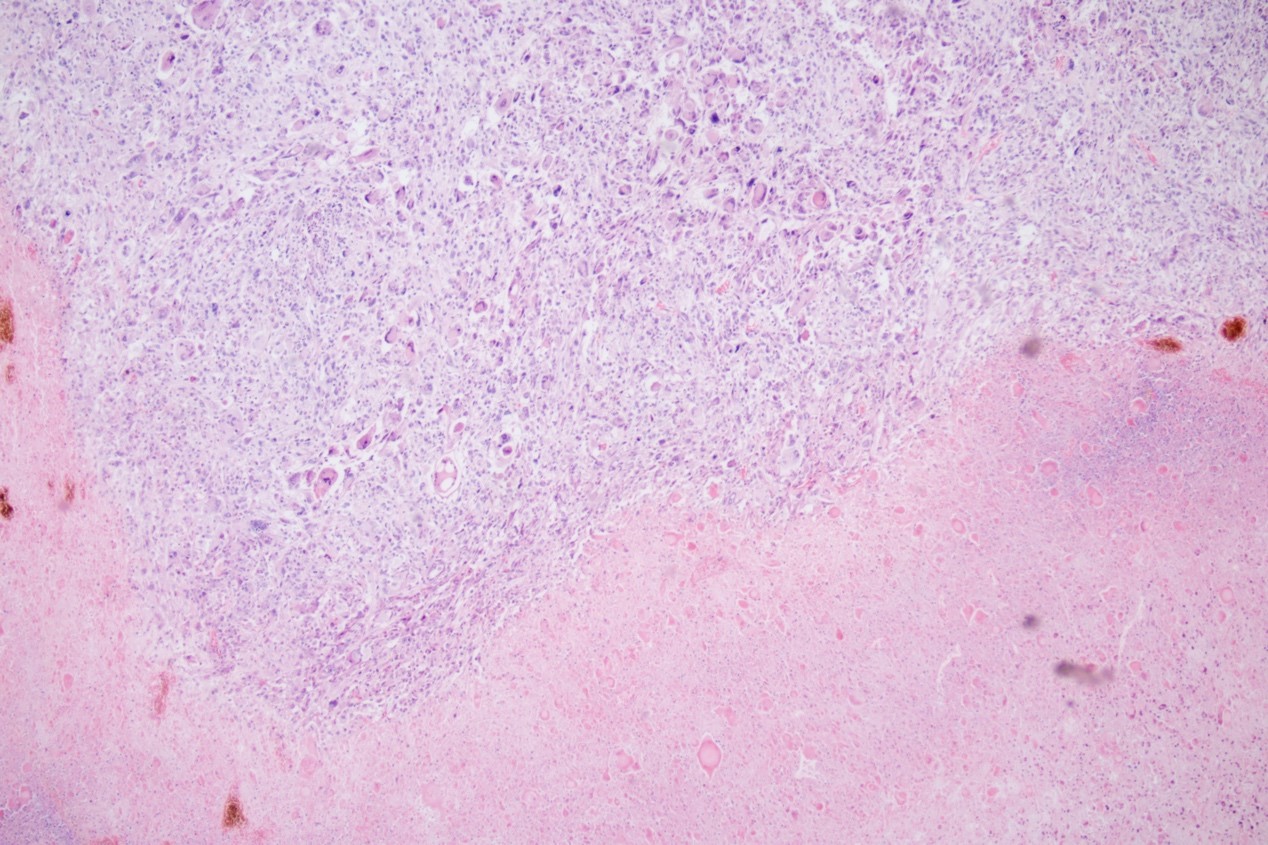 低倍
低倍
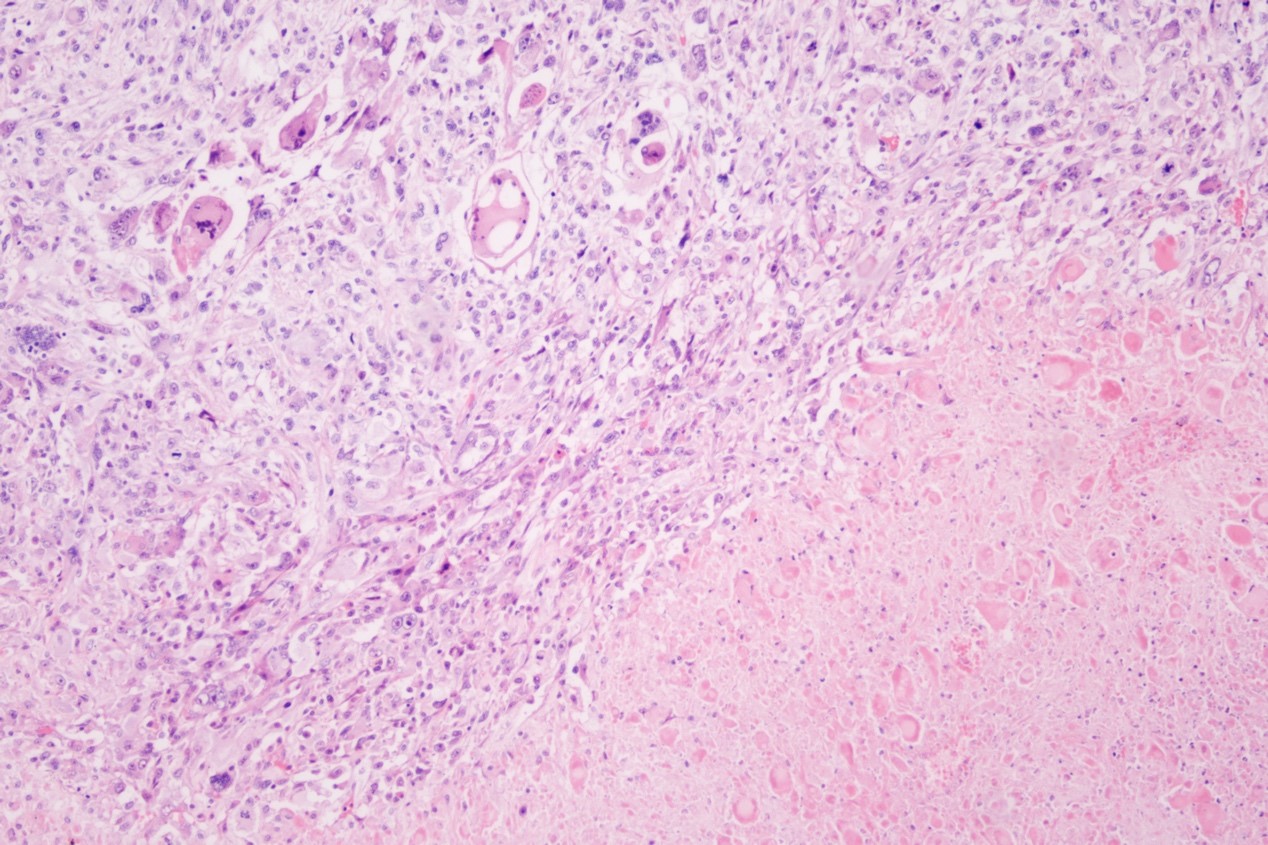 中倍
中倍
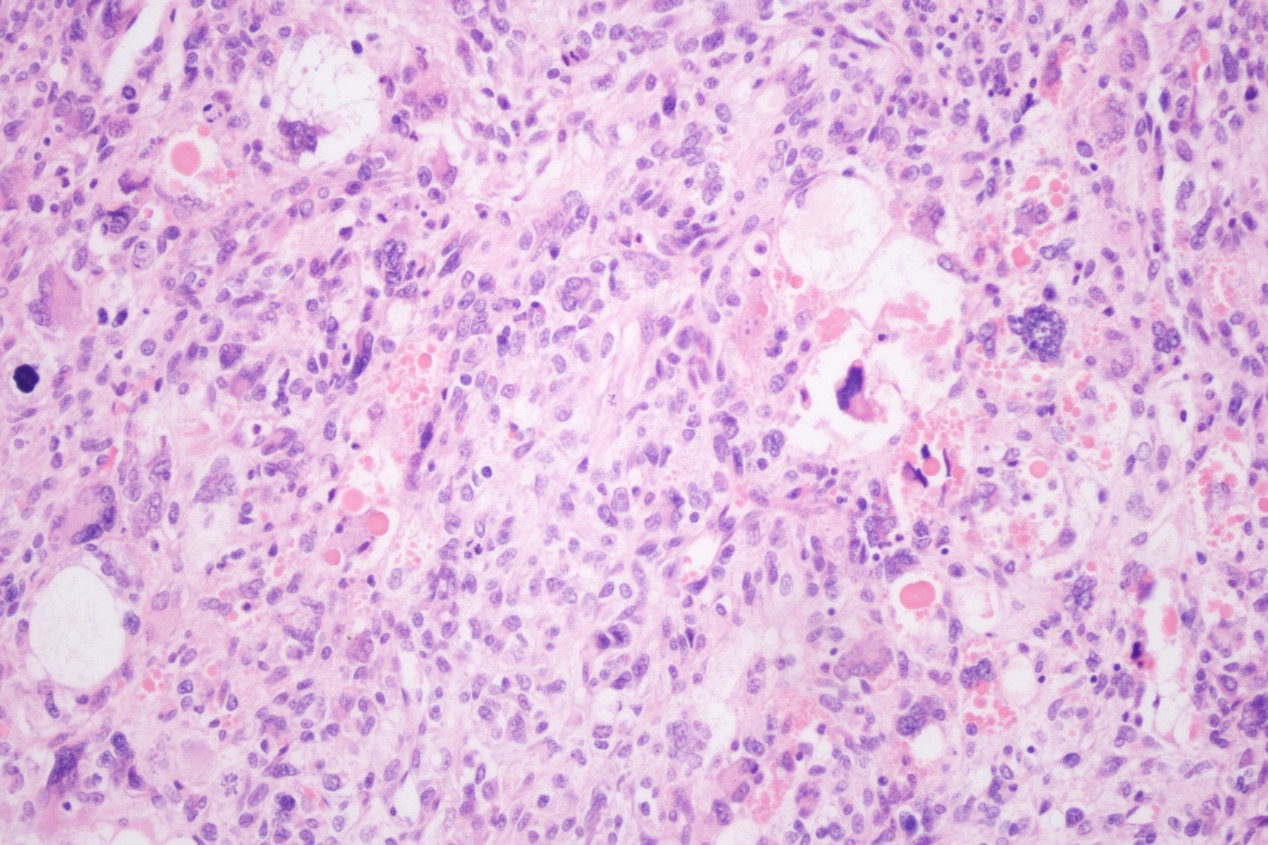 嗜酸性小体和奇异形细胞
嗜酸性小体和奇异形细胞
 肿瘤巨细胞和奇异形细胞
肿瘤巨细胞和奇异形细胞
 纤维性假包膜
纤维性假包膜
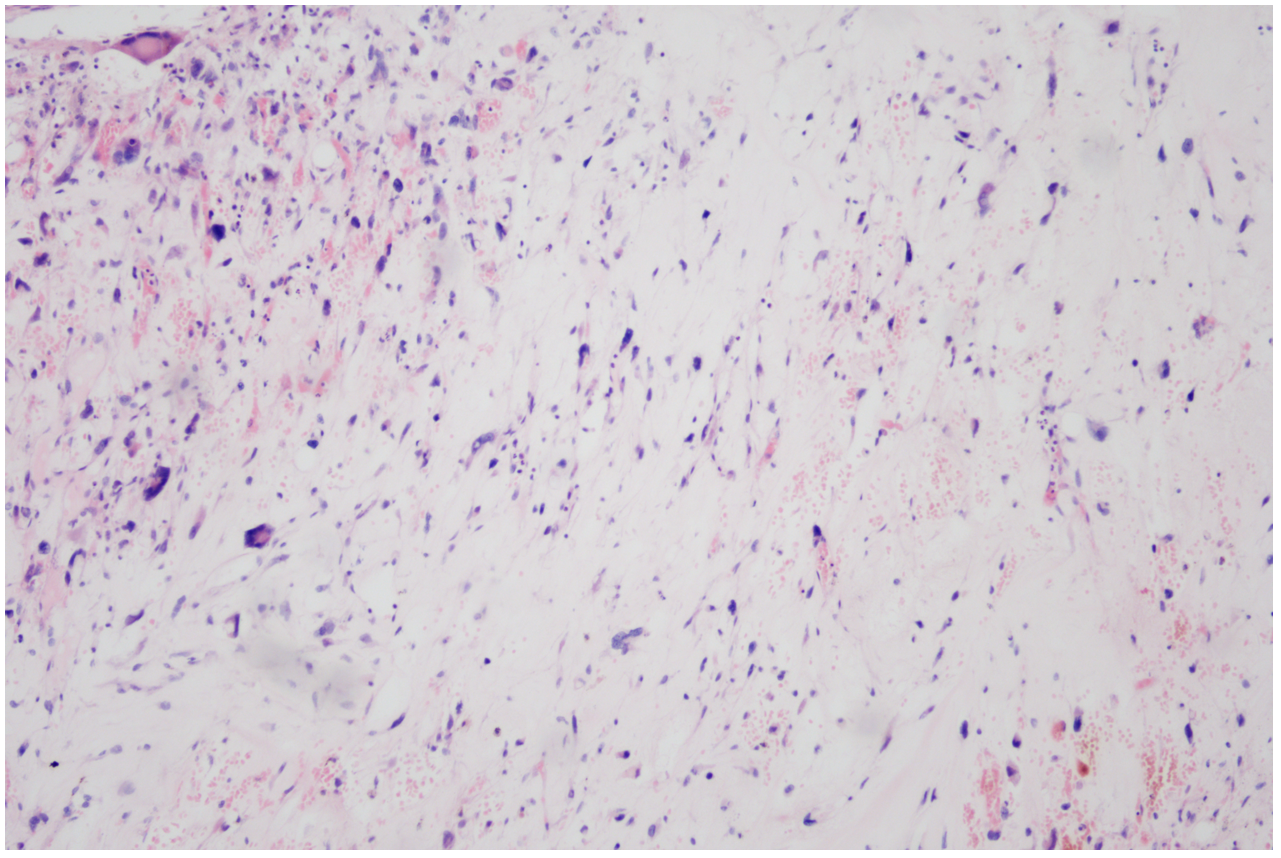 黏液样区域
黏液样区域
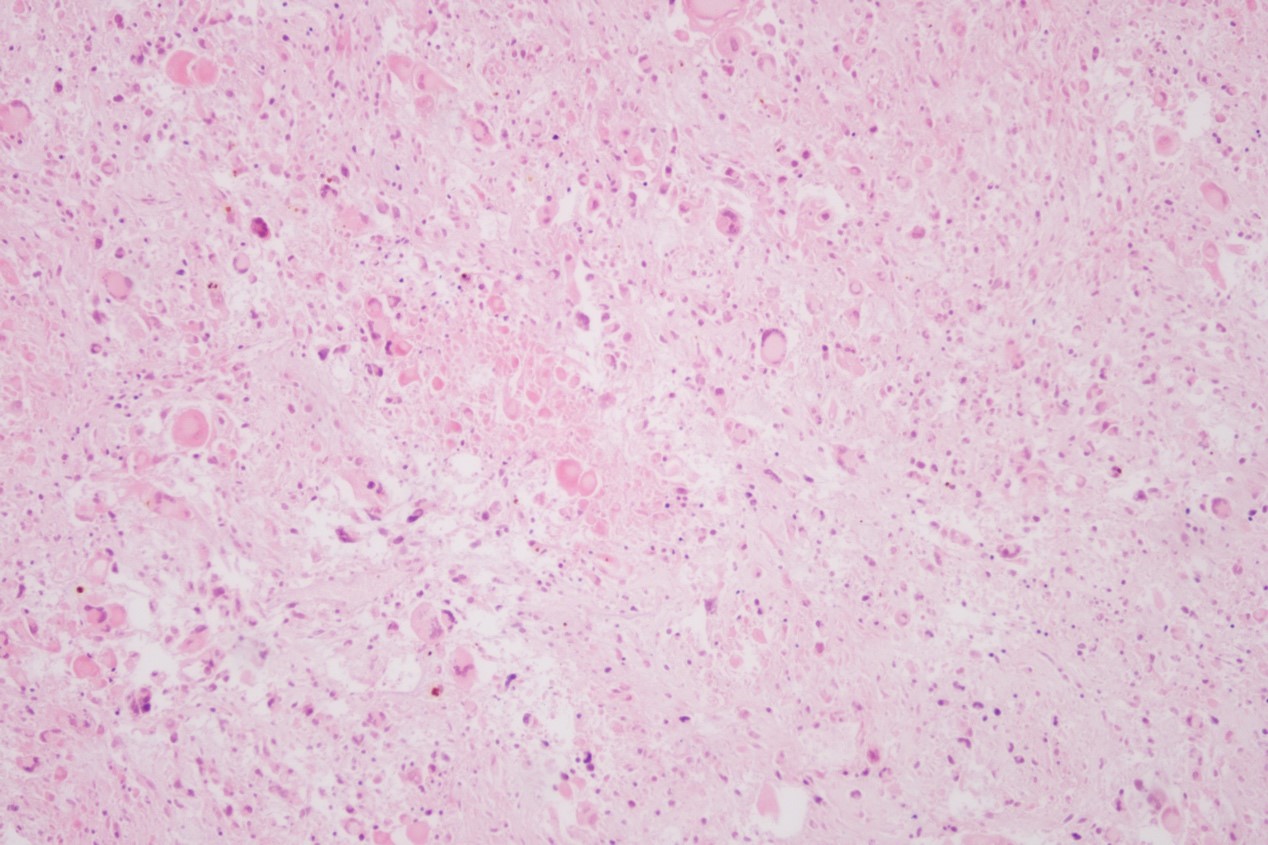 坏死区域
坏死区域
 免疫组化:CK(局灶+)
免疫组化:CK(局灶+)
 免疫组化:Desmin(+)
免疫组化:Desmin(+)
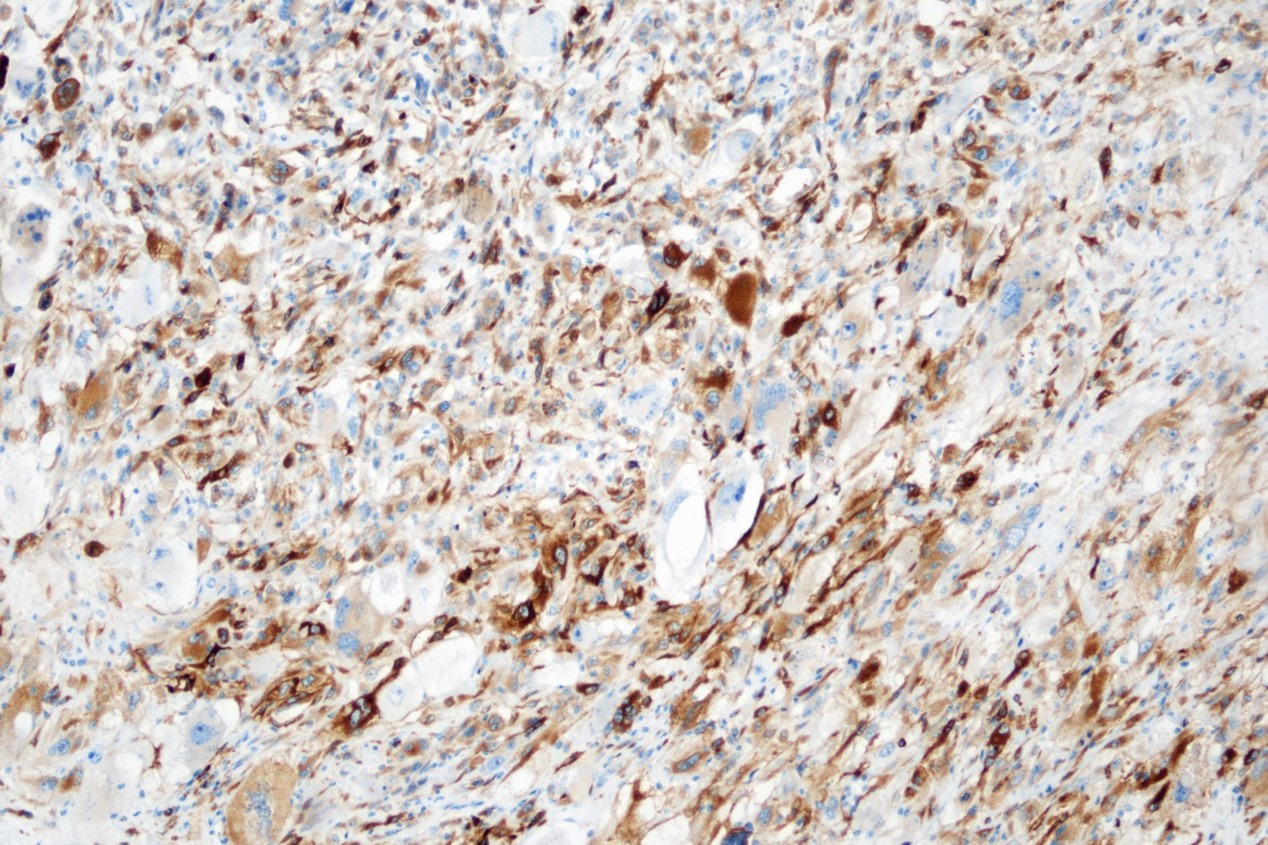 免疫组化:GPC-3(局灶+)
免疫组化:GPC-3(局灶+)
 免疫组化:Vimentin(+)
免疫组化:Vimentin(+)
 免疫组化:Ki-67(约70%+)
免疫组化:Ki-67(约70%+)
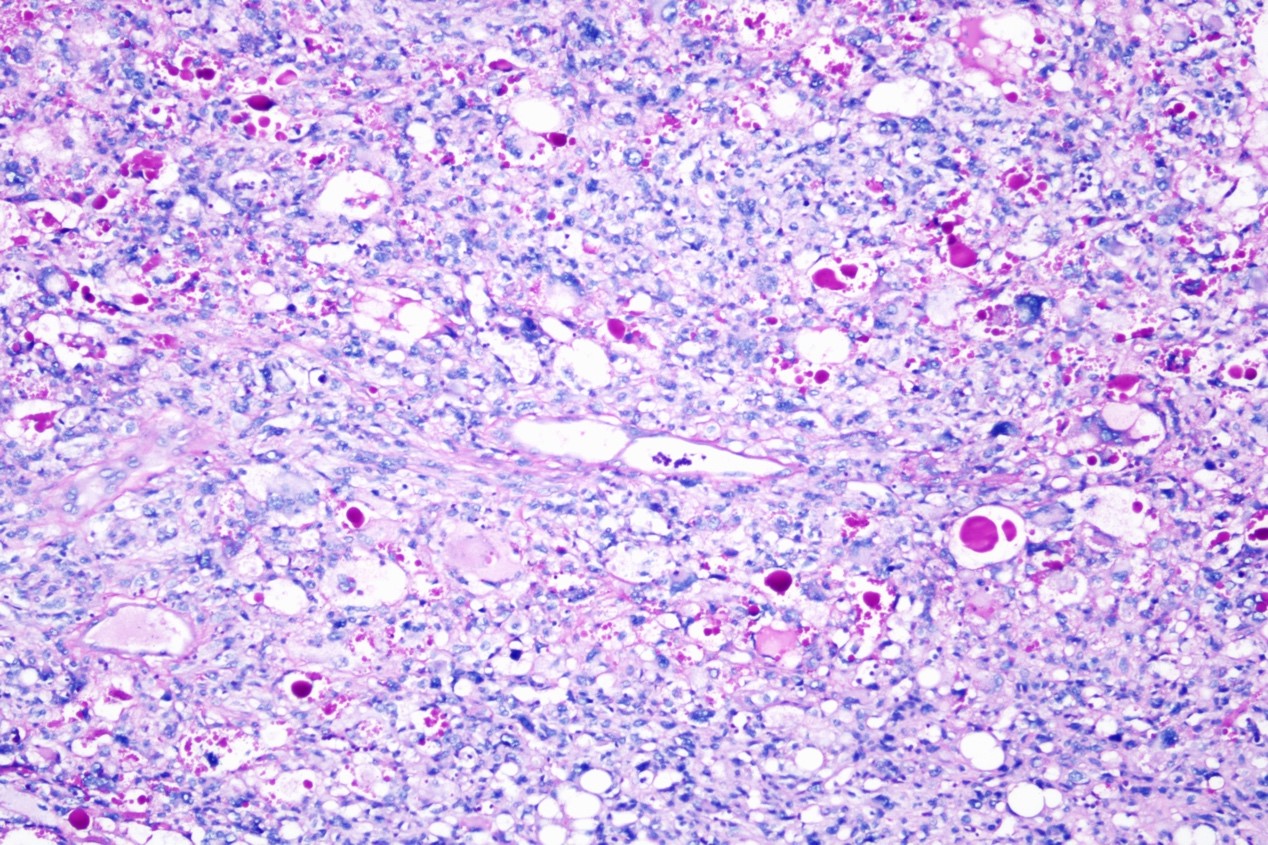 特殊染色:PAS(+)
特殊染色:PAS(+)


























共0条评论