[导读] 本文作者:徐福炉
乳腺的微腺腺病(MA)是一种良性的腺体增生,大约在35年前首次被描述。“病变由大小相同的小腺体组成。腺体内衬一层立方上皮细胞,被基底膜包围但没有肌上皮成分。细胞对低分子角蛋白和S-100蛋白呈阳性,对雌激素受体(ER)、孕激素受体(PR)和HER-2呈阴性。”
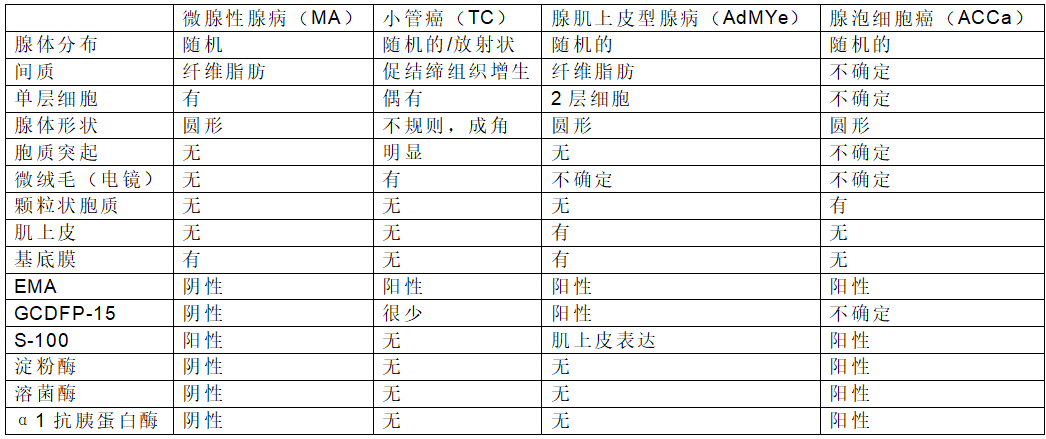
微腺腺病(MA)主要由良性的大小相同的增生性腺体组成,界限不清,腺体散乱的分布在乳腺间质和脂肪组织内。这种病变特别的地方在于其打破了乳腺良性病变2层细胞的结构,即缺乏周围围绕的肌上皮成分。有多篇文献曾报道了MA的恶性特征,但是大多数报道的MA病例并没有之前所描述的典型特征。它们在细胞学组成和免疫组化上都有不同的特点。本文主要探讨了MA的诊断及具有MA相似结构的病变的鉴别诊断。
临床特征:MA仅在女性患者中被描述过。患者年龄从28岁到82岁,平均60岁。
大体观察:病变从直径0.5至8cm,可单灶、多灶分布。
组织学特点:
MA的特征是离散的单层小管状腺体增生。病变界限不清,增生的腺体结构渗入周围的正常乳腺组织。腺体分布不规则,先前存在的导管和小叶似乎被包围,但没有被增生腺体所挤压的改变(图1A)。

图1A增生的小而均匀的腺体分布于乳腺实质和脂肪组织内,但不破坏正常腺体
小管大小一致,与正常乳腺小叶腺泡相似。腺管呈圆形,有一个开放的明显的管腔。很少出现封闭的管状结构。腺腔各个切面几乎都是一致的圆形,说明腺体结构是小球状的(图1B)。管腔内通常含有无定形的嗜酸性物质,并且是acid-Schiff阳性和淀粉酶阴性。偶尔阿辛蓝(pH2.5)可染管腔内物质。管腔内很少见到层状砂粒体。

图1B高倍镜下,MA腺体圆形,规则,内衬单层立方细胞,无异型性。腺体缺乏微绒毛,腔内有分泌物
小管内衬上皮一般为单层立方细胞,偶尔可以变平坦。特征性的变化是外层肌上皮的缺失。此外,围绕腺体结构的薄至偶尔厚的基底膜偶可辨别。小管上皮细胞的细胞质通常是透明的,偶尔显示糖原的细颗粒状。尽管有明显的管腔内分泌物,但细胞质的管腔边缘被截断,没有明显的顶浆分泌的特点(图1C)。这些特征在其他显示管腔分泌的上皮中是没有的。细胞核形态温和,呈圆形或卵圆形,核仁缺失,偶尔可见模糊的小核仁,核分裂罕见,ki67指数较低。

图1CMA腺体呈圆形,位于纤维组织内。细胞质透明,细颗粒状。核呈圆形至多边形。可见基底膜环绕腺体。
腺体某些情况下可能排列紧密,但大多数时候是由少细胞的胶原性间质或脂肪间隔开的。没有促结缔组织增生性间质反应或血管及神经侵犯。
MA可与其他良性病变伴随,如囊肿、硬化性腺病、导管扩张和导管上皮增生。有研究报道MA出现在纤维腺瘤中。
超微结构:
管腔表面没有微绒毛,腔内为均匀的电子致密分泌物,胞质内为电子致密颗粒,几乎不含细胞器,可有溶酶体,没有发现分泌颗粒。
免疫组化:
低分子角蛋白(几乎全部为阳性),平滑肌肌动蛋白示肌上皮缺乏,IV型胶原和层粘连蛋白提示基底膜存在。雌激素受体(ER)、孕激素受体(PR)和HER-2一直呈阴性。S-100蛋白对上皮细胞的强烈且一致的阳性,上皮细胞膜抗原(EMA)和GCDFP-15完全阴性。淀粉酶、溶菌酶和α1抗胰蛋白酶MA阴性(图2)。

图2A:S100阳性 B:EMA阴性 C:IV型胶原示基底膜 D:肌上皮标记失表达
鉴别诊断:
硬化性腺病:有小叶中心性的腺体增生,周围有明显的肌上皮细胞。
小管癌(tubular carcinoma (TC)):腺体呈放射状增生,间质有间质反应,腺体有棱角,细胞核大而不规则,管腔细胞显示胞质突起,在免疫组织化学和电子显微镜(EM)水平上看不到基底膜。电镜下可见微绒毛。免疫组化显示:低分子角蛋白、EMA、ER和PR持续阳性。GCDFP-15可能为阳性,而S-100蛋白、HER-2、基底膜和肌上皮染色为阴性。
腺肌上皮型腺病:有明显的两层细胞,肌上皮存在,免疫组化EMA,GFDFP-15阳性表达
腺泡细胞癌(Acinic cell carcinoma (ACCa)):腺体大小、形状不同,腺腔内衬一至几层非典型细胞(图3A,B)。腺体缺乏基底膜和肌上皮,腔内有亲两性分泌物,肿瘤细胞胞质丰富,多角形,胞质呈透明状,内含颗粒。结构上显示强的嗜碱性,大小不一,核位于中央,可见粗糙的染色质和明显的核仁(图3C,D)。核分裂多见。免疫组化:ER/PR/HER2阴性,EMA、低分子角蛋白、α抗胰蛋白酶和淀粉酶阳性,超微结构显示致密的粗胞质颗粒。

图3
图4显示微腺体结构病变的鉴别诊断要点
参考文献:
[1]Foschini MP, Eusebi V.Microglandular adenosis of the breast: a deceptive and still mysterious benign lesion. Hum Pathol.2018 Dec;82:1-9.



















共0条评论