[导读] 译者:慧海拾穗
儿童型弥漫性低级别胶质瘤主要包括(1)弥漫性星形细胞瘤,MYB或MYBL1变异型;(2)血管中心性胶质瘤;(3)年轻人多形性低级别神经上皮性肿瘤;(4)弥漫性低级别胶质瘤,MAPK通路变异型。
(1)弥漫性星形细胞瘤,MYB或MYBL1变异型
【定义】MYB或MYBL1变异型弥漫性星形细胞瘤是一种伴MYB或MYBL1基因改变的由单一形细胞形态组成的弥漫性浸润性星形胶质瘤,WHO分级为I级。
【ICD-0编码】9421/1
【ICD-11编码】2A00.0Y和XH6PH6其他特定的脑胶质瘤和星形细胞瘤,NOS
【相关术语】不推荐:同形态(isomorphic)星形细胞瘤变异型;同形态弥漫性胶质瘤
【亚型】弥漫性星形细胞瘤,MYB变异型;弥漫性星形细胞瘤,MYBL1变异型
【部位】是最常见的是具有皮质和皮质下成分的脑肿瘤,依次为颞、前额、枕部、顶叶。脑干罕见。
【临床特征】MYB或MYBL1变异型弥漫性星形细胞瘤患者通常表现为抗药性癫痫发作(drug-resistant epileptic seizures),通常自儿童时期起出现。因此,该肿瘤属于长期癫痫相关(epilepsy–associated)肿瘤范畴。文献报道,癫痫发作的中位年龄为10岁(范围1~35岁)。然而,只有23%的患者在儿童时期接受过手术,手术的中位年龄为29岁,癫痫发作后手术的中位时间为15年。
【影像学】MYB或MYBL1变异型弥漫性星形细胞瘤T1典型低信号,T2-FLAIR显示混合信号或高信号,无增强,不显示局限性扩散。肿瘤大多界限清楚,但它们可能表现出弥漫性生长模式,至少局部是这样。偶尔可见大囊肿。
【流行病学】MYB或MYBL1变异型弥漫性星形细胞瘤罕见或少见,约占儿童低级别胶质瘤的2%,占所有脑肿瘤的<0.5%。无性别差异(也有文献报道男女比例为3﹕1)。
【病因学】未知。
【大体表现】MYB或MYBL1变异型弥漫性星形细胞瘤通常为无包膜、软至易碎的灰白色肿块。
【组织病理学】MYB或MYBL1变异型弥漫性星形细胞瘤特征性具有相对单一形态的胶质细胞增生,其细胞核温和、圆形至卵圆形或纺锤状,弥漫分布于纤维基质中或渗透神经纤维。模糊的血管中心极性可能在部分区域上很明显,尤其是在MYB改变的亚型中。内陷的神经元通常证明这些星形细胞瘤具有浸润性。核分裂象通常缺失或较低,未见微血管增生和坏死。偶尔会观察到更多形性细胞核、轻度增生的病例,尤其是在儿童病例中。
【免疫表型】典型MYB或MYBL1变异型弥漫性星形细胞瘤病例为GFAP阳性和低Ki-67标记指数。一项研究报告,MAP2的表达仅限于残余神经元和神经元突起,肿瘤细胞不表达OLIG2和CD34。IDH1 p.R132H为阴性,核ATRX表达保留。
【鉴别诊断】血管中心性胶质瘤的某些区域具有与MYB或MYBL1变异型弥漫性星形细胞瘤相同的结构和细胞学特征,这两种肿瘤类型被认为具有重叠的形态。这些肿瘤类型之间的组织遗传学关系在遗传水平上得到加强;实际上,所有血管中心性胶质瘤都有MYB重排,最常见的是MYB-QKI融合。鉴于其独特的生物学行为,区分MYB或MYBL1变异型弥漫性星形细胞瘤与成人型IDH突变型或IDH野生型弥漫性星形细胞瘤更为重要。此外,还需要和反应性胶质增生进行鉴别,反应性胶质细胞增生时胶质细胞等距分布、很少有丝分裂、低至缺失Ki-67标记、很少或没有细胞学非典型性、可能显示含铁血黄素色素沉积。
【细胞学】无临床相关性
【诊断性分子病理学】测序表明结构变异导致MYB或MYBL1与伙伴基因融合。最常见的伴侣基因PCDHGA1、MMP16和MAML2。MYB在该肿瘤中很少与QKI融合;MYB-QKI融合通常见于血管中心性胶质瘤。MYB或MYBL1变异型弥漫性星形细胞瘤为IDH和H3野生型。虽然测序决定了基因融合的性质,但其他方法(如间期FISH)也可以证明MYB或MYBL1的重排。
【必要的和理想的诊断标准】必要的:无间变组织学特征的弥漫性星形细胞瘤、无IDH和H3基因突变和MYB或MYBL1结构改变,或DNA甲基化谱支持MYB或MYBL1变异型弥漫性星形细胞瘤;理想的:缺乏MAP2和OLIG2表达。
【分期】不适用
【预后和预测】可用的结果数据有限,但临床表现良好。在一篇报道11名儿童患者中,9名在中位随访12年后病情稳定或无疾病迹象;1名患者在17个月后因复发性疾病需要手术,另一名患者死于该疾病。在第二篇报道中,16例MYB或MYBL1改变的胶质瘤患者在中位随访6.2年后均存活;4名未接受初次全切除的患者因复发需要手术治疗。在一篇中位随访2.5年的18名患者(主要是成年人)中,只有1名患者因3年后复发而需要手术,无一人死亡。在癫痫患者中,约90%在切除后癫痫发作消失,其余患者癫痫发作频率降低。
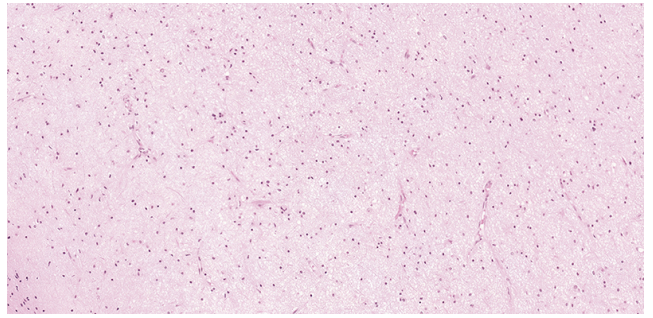
图1:MYB或MYBL1变异型弥漫性星形细胞瘤特征性具有相对单一形态的胶质细胞增生,其细胞核温,且弥漫渗透于神经纤维中。
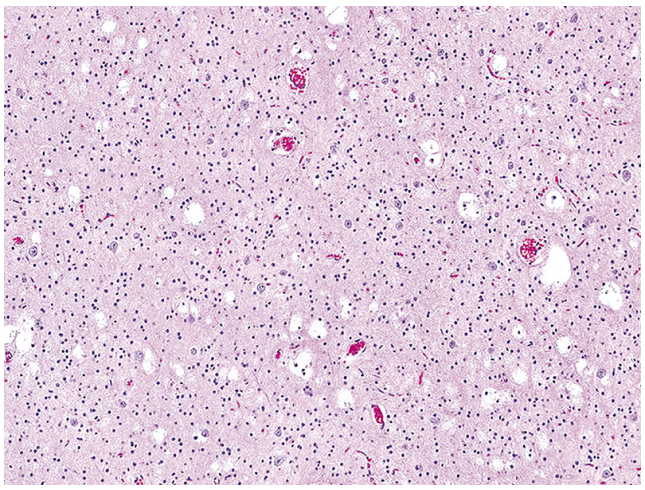
图2:MYBL1变异型弥漫性星形细胞瘤具有胶质细胞密度轻度增加和非典型性。
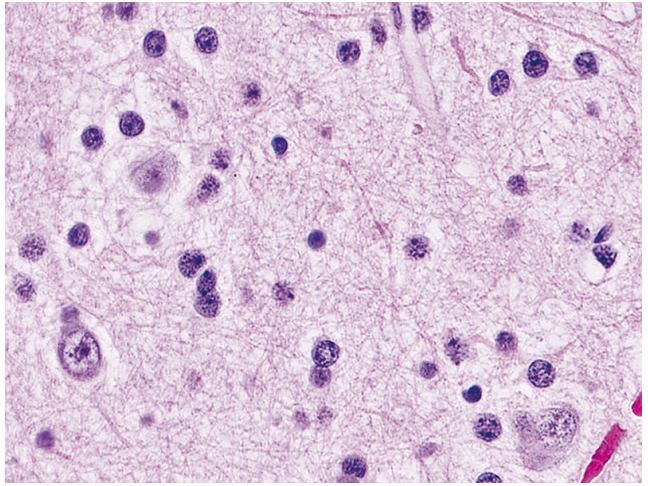
图3:MYBL1变异型弥漫性星形细胞瘤具有胶质细胞密度轻度增加和非典型性。
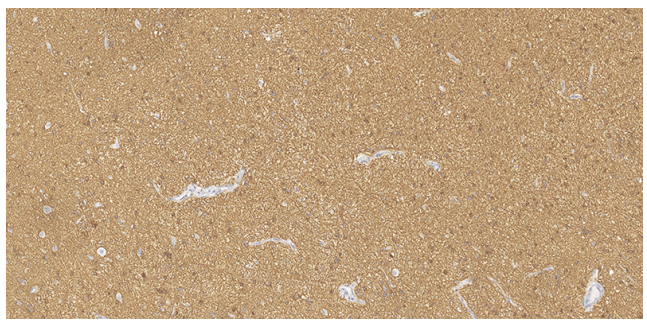
图4:肿瘤细胞和背景神经纤维弥漫表达GFAP。
(2)血管中心性胶质瘤
【定义】血管中心性胶质瘤(Angiocentric gliomas)是一种弥漫性胶质瘤,主要由薄壁、形态温和的双极细胞组成,至少部分聚集在血管周围。几乎所有血管中心性胶质瘤都有MYB::QKI基因融合,其余的通常有另一个MYB改变(WHO 1级)。
【ICD-0编码】9431/1
【ICD-11编码】2A00.0Y和XH41C5其他特定的脑胶质瘤和血管中心性胶质瘤
【相关术语】不推荐:血管中心性神经上皮瘤,单形性血管中心性胶质瘤。
【亚型】无
【部位】血管中心性胶质瘤通常位于大脑皮层,但脑干是该肿瘤越来越常见的部位。
【临床特征】血管中心性胶质瘤患者通常表现为慢性难治性部分性癫痫。头痛和视力障碍是其他常见的
症状。
【影像学】在大脑皮层,血管中心性胶质瘤通常位于颞叶或额叶。脑干的例子也有报道。在MRI上,这些肿瘤通常边界清楚,无对比增强,在T2加权和FLAIR图像上呈高信号。在某些病例中,T1加权MRI显示肿瘤周围呈环状高信号。邻近侧脑室的杆状延伸和营养不良性钙化是其他可变特征。
【流行病学】对于这种罕见的肿瘤,目前还没有基于人群的流行病学数据。大多数病例发生在儿童和年轻人中,中位年龄为13岁(范围:2岁~79岁)。虽然文献中描述的血管中心性胶质瘤男性患者略多于女性患者,但尚不清楚性别偏好。
【病因学】绝大多数血管中心性胶质瘤是散发性的,与任何特定的危险因素都没有关系。只有一例与1型神经纤维瘤病和Koolen-de Vries综合征相关的病例报道,因此尚不清楚这些是否只是巧合。
【大体表现】血管中心性胶质瘤受累结构扩张,皮质灰质-白质交界处模糊。质硬或质软和胶状。可发生囊性变,实性成分灰白灰褐色。
【组织病理学】典型的血管中心性胶质瘤具有细胞学上一致的双极梭形细胞,细胞核细长,颗粒染色质围绕大小不等血管;这些细胞呈菊形团样放射状排列,或沿血管轴纵向形成单层或多层袖套样。梭形细胞成分可广泛渗透软组织,密度可不等,形成致密的神经鞘瘤样结节,呈紧密交叉束状排列,并在软脑膜表面下方以水平或垂直栅栏排列聚集。黏液样和微囊性变可能很明显。残留的神经元并不明显畸形。一些血管中心性胶质瘤含有上皮样成分,可能包含圆形核旁结构,内部有颗粒状点状斑点,对应于室管膜瘤中出现的EMA免疫反应性微管腔,并在超微结构水平上在血管中心性胶质瘤中得到证实。虽然组织学上出现典型的核分裂象,但在大多数病例中,核分裂象少,未见微血管增生或坏死。核分裂象增加和其他间变性特征的报道很少,但这些发现的临床意义尚不确定。
【免疫表型】在免疫组化研究中,GFAP的表达是规律的,并且一个近乎恒定的发现是EMA至少呈逗点状或环状(微腔)模式的细胞质阳性。膜性EMA表达是血管周围和膜下位置的一些上皮样细胞特征。肿瘤细胞不标记神经元标记物,与大多数其他低级别星形细胞瘤相比,主要是OLIG2阴性。Ki-67增值指数通常<5%(通常<1%), 但在手术后6年未复发的其他典型病变中可有增值指数为10%的情况。
【鉴别诊断】需要和室管膜瘤、室管膜下瘤、浸润性星形细胞瘤、星形母细胞瘤、毛细胞星形细胞瘤进行鉴别。
【细胞学】无临床相关性
【诊断性分子病理学】实际上,所有血管中心性胶质瘤在6q23.3的MYB位点均表现出重排和/或拷贝数改变,包括缺失或扩增。大多数重排涉及MYB和QKI基因之间的融合。从多项研究中获得的数据显示,74例血管中心性胶质瘤中有73例(99%)发现MYB改变。在可以进行适当分析的情况下,在这些系列的47个肿瘤中,有41个证实了MYB-QKI融合。MYB很少与其他几个基因融合,如PCDHGA1。血管中心性胶质瘤缺乏TP53、ATRX、IDH1、IDH2和组蛋白H3基因突变。另一种MYB改变频率相对较高的中枢神经系统肿瘤是儿童弥漫性星形细胞瘤,MYB或MYBL1改变。
【必要的和理想的诊断标准】必要的:具有弥漫生长结构和局灶性血管中心模式的胶质瘤;理想的:单一形态的梭形细胞,具有星形细胞和室管膜分化的免疫表型和/或超微结构证据。
【分期】不适用
【预后和预测】血管中心性胶质瘤通常有惰性行为,放射学上稳定。在大多数情况下,可以实现完全切除,并且可以治愈的。术后并发症和肿瘤复发并不常见。没有已知的预后或预测因素。
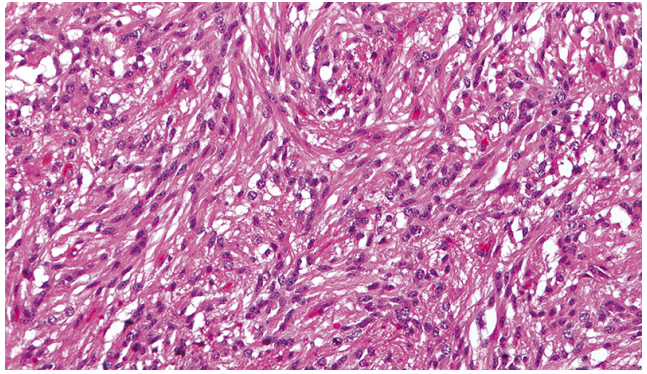
A:在大多数血管中心性胶质瘤中,特别是在肿瘤的实性区域,具有双极性细胞质突起的拉长细胞。
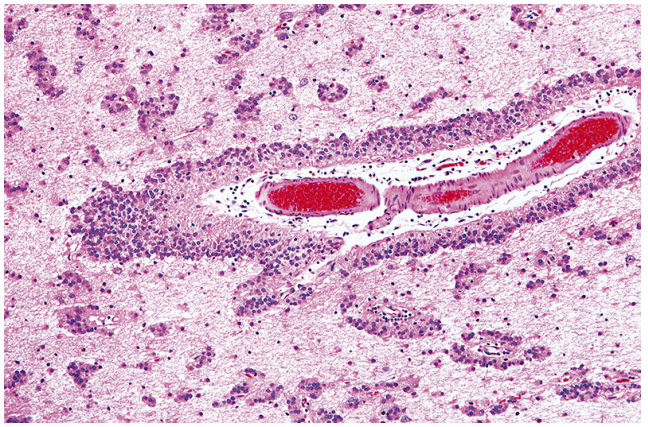
B:注意明显的血管中心模式和残留的神经元。
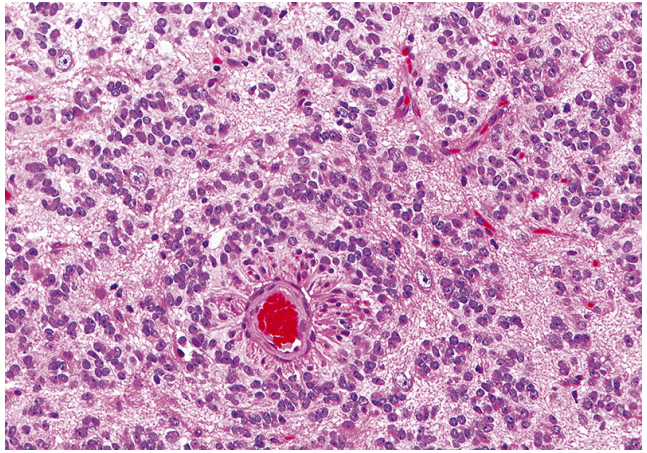
C:残留的神经元存在于显示合胞体模式的肿瘤细胞中。
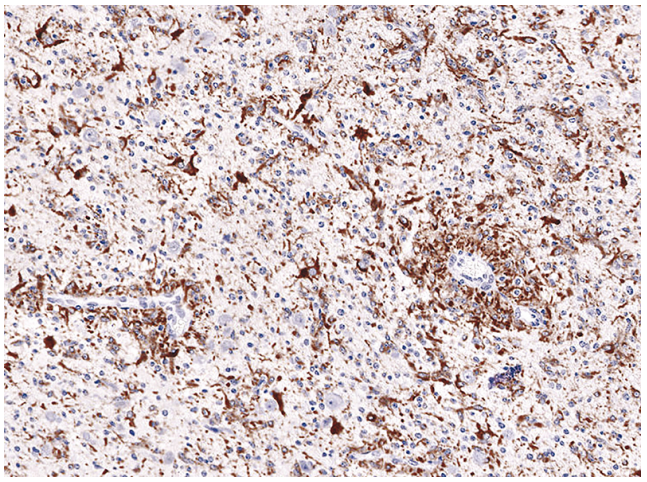
D:血管周围肿瘤细胞GFAP阳性表达。
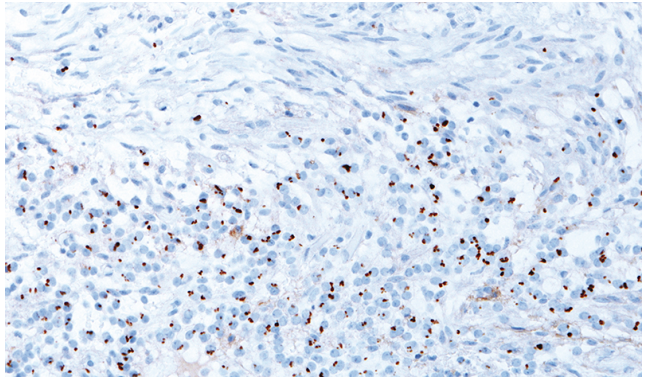
E:EMA逗点状阳性表达。
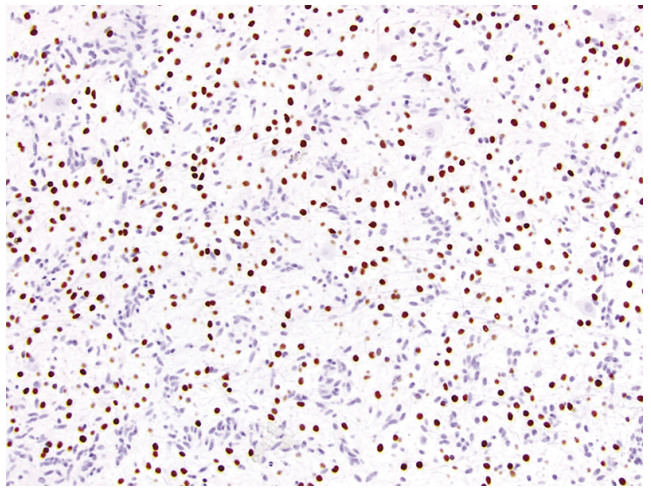
F:肿瘤细胞OLIG2阴性表达,阳性细胞为少突细胞(oligodendrocytes)。
【参考文献】
[1] Diagnostic Pathology: Neuropathology,3rd.2022.
[2] WHO Classification of Central Nervous System Tumours.5th,2021























共0条评论