[导读] 作者:王学利
1、引言
肺癌是世界范围内发病率及死亡率最高恶性肿瘤,其中非小细胞肺癌(non small cell lung cancer,NSCLC)分为腺癌、鳞状细胞癌和大细胞癌等,其中腺癌占大多数。近年来随着肿瘤分子生物学发展、精准医学的观念提出,肺癌治疗日趋个体化。针对分子靶点的新一代抗肿瘤药物将凭借其特异性和靶向性,已经成为晚期肺癌的研究及治疗热点,其中最具有代表性的是以表皮生长因子受体(epidermal growth factor receptor, EGFR)为靶点的基因突变型肺腺癌患者的靶向治疗。EGFR是表皮生长因子受体家族成员之一,具有酪氨酸激酶活性,参与细胞中一系列重要生理过程,与肿瘤细胞增殖、血管生成、肿瘤侵袭及转移有关,在多种实体肿瘤中过表达。
关于肿瘤异质性,上世纪90年代Adelstein等和Mangum等就通过回顾性分析相继提出混合型SCLC和NSCLC概念,然而实际临床诊疗过程否定了肿瘤异质性的作用,回顾性临床研报道更倾向于病理类型转化。肺腺癌治疗后向SCLC转化病例较常见,其内在发生机制及特异性肿瘤标志物变化一直是临床研究的热点及难点,至今仍未完全阐述清晰。笔者在本文报道1例由于TKI耐药导致肺腺癌转化为SCLC病例,望能提高对该肿瘤的认识。
2、病例分享
患者,男性,55岁,因“右肺腺癌术后32个月。”于2021年12月27日入院。2019年4月肺穿刺活检示肺腺癌;2019-04-17在全麻下行胸腔镜下肺叶切除术+胸腔镜纵隔淋巴结清扫术+胸腔镜下胸膜粘连松解术。术后未正规治疗及复查,术后完善基因检测L858R,2021年2月19日复查胸部CT示肿瘤复发?考虑肿瘤复发予以厄洛替尼抗肿瘤治疗,同时针对肋骨病理性骨折于2021年3月1日行粒子植入治疗。服用靶向治疗后门诊随访胸部CT示PR,2021年10月复查CT示右肺病灶稳定,左肺下叶背段新增小结节。其影像学检测如下。
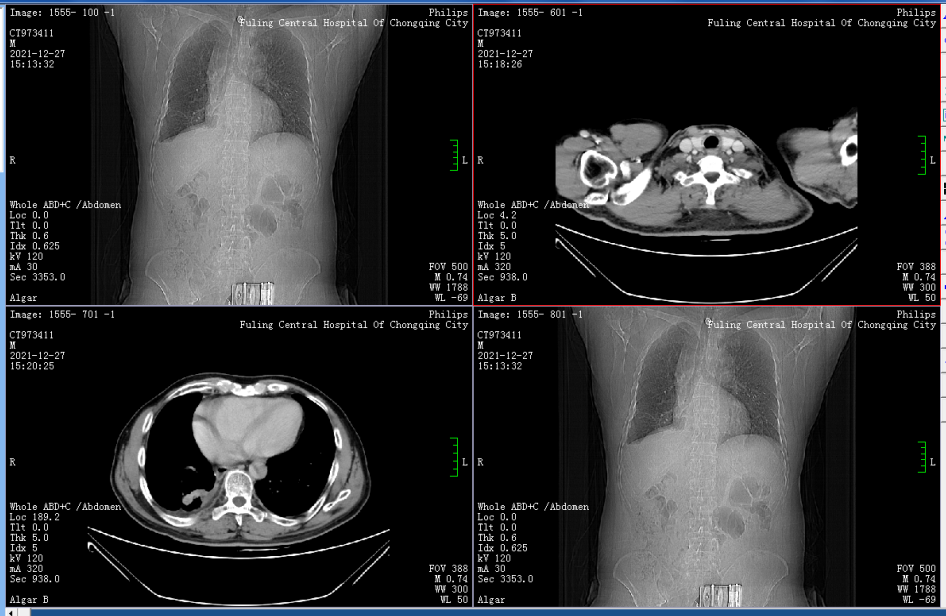
2022年元旦期间穿刺送检病理示浸润性肺腺癌成分,局部见小细胞神经内分泌癌成分,肿瘤细胞免疫组化结果示:ALK/D5F3(弱+);CK5/6(-);CK7(腺癌+);Ki-67(+60%);NapsinA(腺癌-/+);P40(-);P53(异常缺失);P63(-);PD-1(-);PD-L1(+20%);TTF1(++);CD117(小细胞癌+);CD56(小细胞癌++);CgA(-);Syn(小细胞癌+)。最终病理诊断结果:结合组织形态学和免疫表型,符合复合型小细胞神经内分泌癌,但不能完全除外肺腺癌治疗后抵抗,转化为小细胞癌。请结合临床,综合分析。
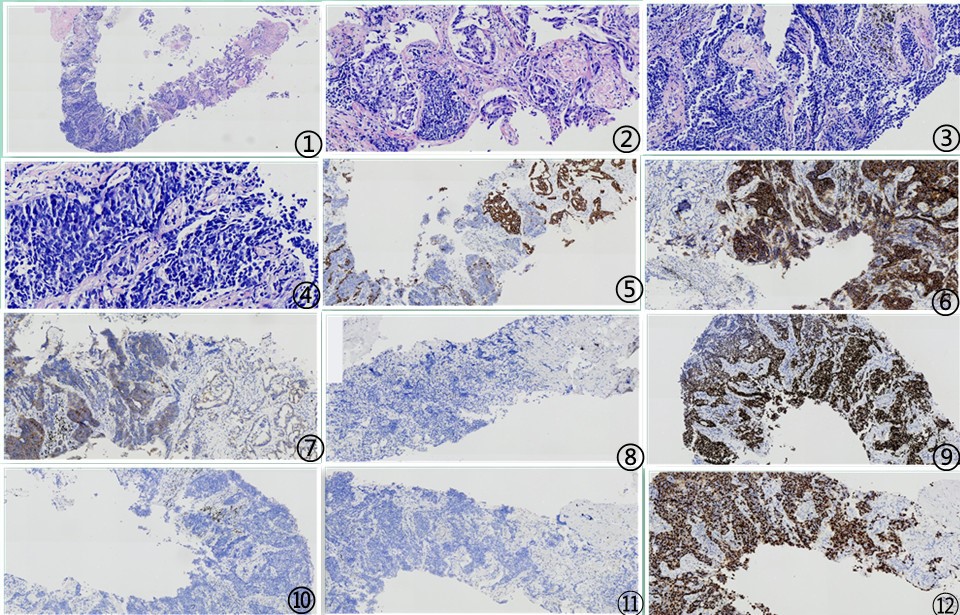
图1 低低倍镜下见腺癌和小细胞神经内分泌癌成分;图2 低倍镜下见腺癌和小细胞神经内分泌癌成分;图3 中倍镜下小细胞神经内分泌癌成分;图4 高倍镜下小细胞神经内分泌癌成分;图5 CK7腺癌成分弥漫强阳性而小细胞癌成分阴性;图6 小细胞癌CD56弥漫强阳性;图7小细胞癌CD117阳性;图8 小细胞癌CgA阴性;图9小细胞癌TTF1弥漫强阳性;图10 小细胞癌NapsinA阴性;图11小细胞癌P40阴性;图12小细胞癌增殖指数Ki67高表达,约80%;
遂复习以前病例切片,2019年04月03日肺穿刺标本,肿瘤细胞免疫组化示:CD45RO(散在+);CK-P(+);ERCC1(+);Ki-67(+,50%);P40(-);P53(-);PD-1(-);PD-L1(-);RRM1(-/+);Stathmin(++);TOPOII(II级);TS(+/-);β-tubulin(++);CDX2(-);Napsin A(+);TTF1(+);Villin(-);病理结果示(肺穿刺标本)浸润性肺腺癌。
后04月17日在全麻下行胸腔镜下肺叶切除术+胸腔镜纵隔淋巴结清扫术+胸腔镜下胸膜粘连松解术,送检标本至病理科;大体:右下肺叶组织一个,距支气管断端4cm处被膜边缘见灰白色结节一个,体积4cm×3cm×2.5cm,切面灰白灰褐色质中,选切五块。免疫组化示:CD45RO(+);CDX2(-);CK-P(+);ERCC1(+);Ki-67(+,50%);P40(-);P53(-);RRM1(++);Stathmin(++);TOPOII(II级);TS(-);TTF1(+);Villin(-);β-tubulin(++); 最终诊断:(右下肺叶)浸润性肺腺癌,腺泡型为主,未见明确脉管内癌栓及脏层胸膜侵犯,肿瘤最大径4cm;(第七组、第九组、第十组、第十一组)淋巴结共6枚未见癌组织转移(0/6)。
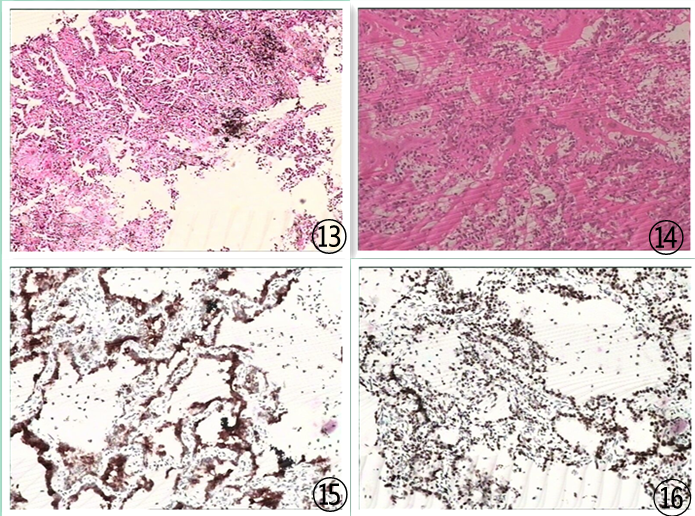
图13 肺穿刺标本示腺癌成分;图14大体标本见腺癌成分;图15腺癌成分CK7弥漫强阳性;图16腺癌成分TTF1弥漫强阳性;
该患者继续在我院接受治疗,临床效果不佳,春节转院后失访。
3、讨论
3.1临床特征
EGFR基因突变肺腺癌多见于亚裔人种、女性、非吸烟者,且高分化肺腺癌患者更易出现EGFR突变。一般情况下肺腺癌向SCLC转化后病情进展较快,有效治疗手段少,总体预后较差,文献发现国外39个病例研究中,肺腺癌转化为SCLC中位时间为19个月,转化为SCLC后中位生存期 6个月,女性生存期显著长于男性。多数肺腺癌患者接受EGFR-TKI治疗后14-26个月可发生耐药,其发生率为5%-14%。与原发SCLC相比,转化SCLC患者预后相对更差,可能是因为绝大部分SCLC转化源自EGFR-TKI耐药难治转移性恶性肿瘤。研究显示肺腺癌转化前后EGFR突变类型保持一致,推断EGFR-TKI治疗后SCLC与腺癌同源。
2020年中国临床肿瘤学会(Chinese Society of Clinical Oncology,CSCO)小细胞肺癌诊疗指南推荐,标准SCLC化疗+继续原EGFR-TKI作为转化性SCLC患者治疗方案(Ⅲ类证据、Ⅲ级推荐)。ProGRP、NSE均是诊断SCLC灵敏度及特异度均较高的生物标志物,研究结果发现与初诊相比,部分病例转化后ProGRP、NSE水平成倍增高,表明ProGRP、NSE作为肺腺癌患者EGFR-TKI治疗后SCLC转化情况的预测指标。文献提示血清NSE快速升高通常意味着EGFR-TKIs导致腺癌向SCLC转化迹象示血清NSE水平显著升高可能代表着肺腺癌细胞正向SCLC转化,更加确定重复活检的必要性。研究结果显示CD56、Ki-67在SCLC转化后亦有向高表达发展趋势,符合SCLC恶性程度更高特征,提示SCLC转化患者的预后较差。
3.2、分子基因学
表皮生长因子受体酪氨酸激酶抑制药(epithelial growth factor receptor tyrosine kinase inhibitors,EGFR-TKIs)可逆地与EGFR三磷酸腺苷结合位点相竞争,阻断EGFR信号传递,从而抑制肿瘤生长增殖,能明显改善EGFR敏感突变NSCLC患者临床预后,国内外临床研究已证实70%EGFR突变者对靶向药物有效,EGFR-TKIs一线治疗EGFR突变晚期NSCLC疗效优于单纯化疗,可延长患者无进展生存期(progression free survival, PFS)及总生存期,美国国立综合癌症网络(National Comprehensive Cancer Network, NCCN)指南已将EGFR-TKI做为晚期EGFR突变肺腺癌患者一线治疗方案。但令人遗憾的是随着用药时间的延长,多数患者在平均用药12个月后出现病情进展。
患者EGFR基因为19号外显子突变。文献报道肺腺癌中EGFR突变型比野生型更常见,同时突变型更易转化为SCLC,研究发现肺腺癌EGFR第19外显子突变(50.0%,9 /18)较第21外显子突变(27.8%,5/18) 转化为SCLC频率更高。JIANG等研究发现SCL转化后大部分保留与原发肺腺癌( 83.3%,15/18) 相同基因突变,只有小部分失去原基因突变或获得另一种类型基因突变,这种现象可能与SCLC转化不同机制有关。
EGFR-TKI治疗耐药后发生SCLC转化是临床最常见转化方式。放疗、化疗、靶向治疗、免疫检查点抑制剂等治疗后进展或耐药时,均应再次病理活检以确认是否出现肺腺癌向SCLC转化。TKI耐药机制有:①T790M突变引起继发耐药,占总患者50%以上;②酪氨酸激酶代偿,如c-MET扩增和人表皮生长因子2(human epidermal growth factor receptor 2,HER-2)突变也起着重要作用;③代偿信号通路激活,如PI3K/Akt信号通路和TOPK-c-Jun通路等;④组织病理转化,包括EM表型转化和SCLC转化,肿瘤最初即存在两种混合成分,最初诊断时腺癌可能优势主导成分,经治疗后SCLC逐渐占据主导成分。无论由于哪一种机制发生,都提示重复活检的重要性。本病例支持第四种机制,暨组织病理转化,但病例太少,仍需大样本多中心深入研究。
对于非小细胞肺癌与SCLC间转化机制,其中有以下几种学说:肿瘤异质性的假说,是肿瘤干细胞在细胞增殖和分化过程中,原癌干细胞分化成特异性的肿瘤干细胞,这种肿瘤干细胞既能分化为NSCLC和SCLC,也能形成肿瘤异质性,且EGFR-TKI能够抑制NSCLC和SCLC进展起主导作用。而NSCLC向SCLC转化假说,是先分化为NSCLC细胞,然后在EGFR-TKI作用下转化成 SCLC。肿瘤异质性假说多认为是发生在使用EGFR-TKI治疗前,而NSCLC为SCLC假说使用EGFR-TKI治疗后。还有大部分学者认为非小细胞肺癌与SCLC来源于共同肿瘤干细胞。具有EGFR敏感突变肿瘤细胞的起源细胞,也同时具有分化为神经内分泌肿瘤细胞的潜能,例如SCLC细胞;且在靶向作用于如常见TP53基因和RB1基因后,某些特定细胞也具有向SCLC细胞转化的潜在可能性,且某些特定细胞如肺泡Ⅱ型细胞,也可以是EGFR基因突变的腺癌细胞中的起源细胞。这对于临床区分其耐药机制及治疗增加难度和挑战。
Rudin与Peifer等通过动物模型基因测序发现,肺腺癌中多见EGFR、KRAS基因突变,而在SCLC中多见RB及Tp53基因突变。RB1基因缺失突变在SCLC中几乎可达100%。后来人们对肺腺癌转化为SCLC患者再次活检分析基因型发现100%患者肺癌组织中均存在RB1基因缺失,这暗示在此类转化耐药患者中RB1缺失可能在转化过程中发挥一定作用,亦或EGFR-TKIs可能导致RB1缺失的出现。另一个导致转化的原因可能与II型肺泡上皮细胞增殖与分化有关,通常我们认为肺腺癌来源于肺泡上皮细胞,SCLC来源于神经内分泌细胞;Sutherland等发现当敲除II型肺泡上皮细胞中的RB1及Tp53基因时会导致SCLC,II型肺泡上皮细胞具有转化为SCLC及肺腺癌等潜能。II型肺泡上皮细胞增殖及分化受EGFR水平调节,EGFR表达可促进II型肺泡上皮细胞增殖及分化,当EGFR基因突变患者使用EGFR-TKIs后,可能导致这种促进其分化的力量削弱,甚至消失,异常分化可能导致II型肺泡上皮细胞向小细胞肺癌发展。
3.3、临床治疗
虽然肺腺癌转化为SCLC机制尚不明确,但目前此类转化型肺癌的治疗多以SCLC标准治疗为主,给予依托泊苷联合铂类方案化疗。为明确靶向治疗后肺腺癌转化为SCLC原因,还需要大量的临床及实验室研究。国际上虽有NSCLC转化为SCLC案例报道,但在临床工作中类似病例很少见,部分原因可能是多数耐药后病例未能行二次活检,未发现病理类型的转化。对于靶向治疗后耐药的EGFR基因突变型患者,均应进行二次活检。目前临床病理明确靶向耐药后转化型SCLC患者数量有限,尚不能明确哪些临床特点可促使肺腺癌向小细胞肺癌转化。靶向治疗以基因突变点为靶标,在反复治疗中患者基因靶点可能出现变化。对于治疗后耐药患者积极行再次组织活检十分必要。明确患者基因型变化情况,调整制定精确治疗方案,才能真正达到个体化精准治疗目的。
4、小结
本文报道NSCLC EGFR-TKI耐药后SCLC 转化病例,总结其特点如下:①该患者无吸烟史;②组织形态学及免疫表型由肺腺癌转化为SCLC;③转化SCLC时伴随NSE水平显著升高;④转化的SCLC虽携带EGFR敏感突变基因但对EGFR-TKI不敏感;⑤SCLC标准EP化疗方案对转化的SCLC疗效明显。
复习本病例所有相关切片,32个月在我院活检后明确肺腺癌,遂行肺叶切除,常规充分取材,但未能全部取材,不能完全除外复合型小细胞神经内分泌癌,腺癌成分为主,局灶为小细胞癌可能性,经过治疗,腺癌成分被抑制,而小细胞癌成分突显出来,本次活检也是提示混合型小细胞癌,仍可见少量腺癌成分。因患者拒绝后续活检,只能提示为临床治疗抵抗后转化可能性。因该病例临床上罕见,笔者第一次见,仍需深入研究探索。
参考文献:
[1] Ahn S , Hwang S H , Han J , et al. Transformation to Small Cell Lung Cancer of Pulmonary Adenocarcinoma: Clinicopathologic Analysis of Six Cases[J]. Journal of Pathology and Translational Medicine, 2016, 50(4).
[2]RB loss in resistant EGFR mutant lung adenocarcinomas that transform to small-cell lung cancer[J]. Nature Communications, 2015, 6:6377.
[3]赵盼,桑蝶,张育荣,王依盟.肺腺癌转化为小细胞肺癌的临床特征分析[J].癌症进展,2021,19(07):690-692+740.
[4]蔡锐,杜安妮,伍定勇,王璇.吉非替尼抵抗致肺腺癌患者转化为小细胞肺癌1例[J].医药导报,2021,40(07):948-950.
[5]李进,饶敏,陆月明.肺腺癌向小细胞肺癌转化1例[J].临床肺科杂志,2019,24(10):1937-1940.
[6]郑崇,王锦聪,宋永彬.晚期肺腺癌EGFR-TKI治疗后转化为小细胞肺癌1例及文献复习[J].中国临床研究,2021,34(06):815-819.DOI:10.13429/j.cnki.cjcr.2021.06.022.
[7]胡廷婷,龚巧燕,徐珽.非小细胞肺癌EGFR-TKI耐药后转化为小细胞肺癌2例[J].中国药师,2016,19(12):2321-2323.
[8]薛淑萍,俞婷婷,张琰,单莉.肺腺癌靶向治疗后小细胞肺癌转化的病例报道[J].中国肺癌杂志,2015,18(10):656-660.
[9]朱魁魁,张盛,伍钢,孟睿.非小细胞肺癌治疗后转化为小细胞肺癌的临床研究进展[J].肿瘤预防与治疗,2020,33(02):179-183.
[10]白文文,张若辉,甄婵军,宋玉芝,于汶卉,付丽媛,周志国.7例肺腺癌转化小细胞癌患者的临床病理特征分析[J].中国肿瘤临床,2020,47(15):776-779.
















共0条评论