[导读] 作者:王学利
1、病例分享
患者,男性,60岁,主因咳血1月余入院。胸片示左肺巨大占位(图1),于全麻下行开胸探查术,术后送检左上肺切除标本至病理科。大体:紧邻肺膜下可见一灰白色肿物,大小为4.5*4.5*3cm,肿物切面灰白间灰褐色,质中,界不清;镜下:肿瘤细胞呈分叶状,体积大且失黏附分布,胞浆丰富呈嗜酸性,多核和奇异的细胞呈弥散性分布,胞核大且异型明显,通常为分叶状可见大的核仁(图2);免疫组化结果示肿瘤细胞CEA、CK19、CK7、TTF-1、Vimentin(图4)及CK(图3)等呈阳性表达;肿瘤细胞LCA、P40、P63、S-100和Desmin等呈阴性,肿瘤细胞增殖指数Ki-67约50%;最终病理诊断结果:左上肺周围型巨细胞癌伴显著坏死,患者于术后9个月死亡。
2、讨论
2.1、概述
肺巨细胞癌(giant cell carcinoma,GCC)是一种含有明显巨大细胞核或多核巨细胞成分的少见原发性高度恶性肺肿瘤,由Hadley和Bullock等于1953年首次报告,由形态各异的多核瘤巨细胞构成,FishbacK等提出该肿瘤诊断标准是巨细胞应占肿瘤细胞>10%。1981年WHO肺肿瘤分类将其归入肺大细胞癌的一个亚型,而1999年分类中GCC被归为伴有多形性、肉瘤性或肉瘤样癌的一个亚型;WHO(2004)分类中肺GCC是肉瘤样癌中的一个亚型;而WHO(2015)肺肿瘤分类中将多形性癌、梭形细胞癌和GCC独立归于一个章节,仍要求肿瘤性巨细胞至少占10%,小活检或细胞标本中可描述肿瘤成分而不要求做出确切诊断结果。
2.2、临床特征
肺GCC临床罕见,约占肺部恶性肿瘤的0.3%-0.4%,约占原发性肺癌1%-5%。患者发病年龄普遍偏大,患者平均年龄50-60岁,较其他非小细胞肺癌患者年龄要低;男性多于女性,男女之比约为5:1,往往伴有较长吸烟史。大多数患者病变早期无特殊临床表现,临床表现与周围型肺部肿瘤类似,如咳嗽,痰中带血,胸痛等。值得注意的是部分患者还能分泌异位HCG而造成男性乳腺发育。影像学表现肺部病灶多发生于肺支气管远端或外周部,肿块以周围型多见,以上叶肺多见,右肺略多于左肺,仅有不到30%病变是在段以上支气管;体积大呈圆形或类圆形,中间薄壁状,CT值类似于肌肉组织,可有空洞,易误诊为肺炎或结核等。形态以肿块多见,通常边界清楚,分叶征和毛刺征不明显,胸膜牵拉征相对不明显,易侵犯胸壁引起肋骨破坏。但最大特点是肿瘤生长速度快,具有很强的侵袭性生物学行为,容易出现多器官的转移。肺GCC常见转移器官与其他非小细胞肺癌相似,包括脑、骨、肝、肾上腺等部位,亦有不常见的转移部位的文献报道,包括胃肠道、肾、心脏等部位。
2.3、病理学特征
确诊依靠病理学检查,肺GCC主要表现为一组由高度多形的多核或单核的肿瘤性巨细胞组成的非小细胞癌癌,无腺癌、鳞状细胞癌或大细胞癌的特殊排列方式。肿瘤细胞体积巨大,形态学多样,呈弥漫性分布,间质很少;肿瘤细胞通常为分叶状,失去黏附性且相互分离;细胞浆丰富呈嗜酸性,多核和奇异的细胞呈弥散性分布,胞核大且异型明显,通常为分叶状可见大的核仁,并且有人提出该肿瘤诊断标准是巨细胞应占肿瘤细胞的10%以上,单个瘤巨细胞核直径>4或5个静止期淋巴细胞,且胞核大小相差≥5倍,这种界定有助于区别于其他含巨细胞的肺癌。此外有研究证实部分GCC还能异位分泌激素,同时会伴有神经内分泌分化,肿瘤细胞周围有中性粒细胞的伸入运动。大多数GCC常与其他类型癌并存,其中以腺癌最多,约占45%。免疫组化上皮性标记物特别是低分子CK和Vimentin呈阳性表达,提示GCC除具有腺癌免疫表型特点外,在分化过程中还获得了肉瘤的某些表型,而TTF1对于诊断肿瘤是否为肺原发性有一定的指导意义。
2.4、鉴别诊断
主要和如下肿瘤性或非肿瘤性肺病变鉴别诊断:①含有巨细胞的其他类型肺癌:肺癌中出现瘤巨细胞并不少见,但这些巨细胞大多分散于癌组织中,而不会成片分布,并可见典型成分有助于鉴别诊断。②肺原发性肉瘤及转移性肉瘤:极为罕见。一般上皮性标记阴性,可以通过自身特征性免疫标记物区分。③肺原发性绒癌:罕见,形态上与肺GCC相似,肺GCC也可以对HCG呈阳性反应,但肺GCC缺乏2种滋养层细胞成分和呈丛状排列形态学特征;另外肺GCC总体上表现为细胞学的多形性及与其他癌成分的共存,均与绒癌不同,再根据GCC相关免疫表型鉴别。④大细胞神经内分泌癌:肿瘤细胞较大,呈多角形,胞质嗜酸,胞核多形性,核仁较明显,核分裂象多见,常见大面积坏死。免疫组化神经内分泌标记物为阳性,电镜下可见神经内分泌颗粒物。⑤转移性肾上腺皮质癌:罕见,可根据临床病史、肿瘤大小和免疫表型加以鉴别,转移性肾上腺皮质癌α-inhibin和melan-A等阳性。⑥肺隐球菌病:除多核细胞及凝固性坏死外,可见厚荚膜;特殊染色PAS及六胺银有助于诊断。⑦巨细胞间质性肺炎:肺组织病变较弥漫,分布不均,程度不一,多数肺泡腔内有大小不同的多核巨细胞沉积,胞质不均匀,像多个细胞融合而成;肺泡隔内有中性粒细胞、淋巴细胞和巨噬细胞等炎细胞浸润,晚期可见不同程度纤维化改变。X线示两侧全肺或大部分肺野有斑点状、结节状、条索状、网织状弥漫性病灶,部分区域可见肺气肿改变等,则有助于诊断。⑧Erdheim-Chester病(ECD):病镜下为大量泡沫样脂质富集或嗜酸性胞质的组织细胞,免疫组化染色CD68和CD163等阳性,而CD1a、langerin等阴性,电镜检测Birbeek颗粒缺如。⑨Rosai-Dorfman病(RDD):可见大量体积较大的组织细胞,呈多边形或类圆形,直径约为淋巴细胞10-30倍,胞质丰富,淡嗜酸性,胞核膜光滑,有小嗜碱性核仁,部分组织细胞的胞质内见较多淋巴细胞和中性粒细胞等,组织细胞表达S100等。
2.5、发病机制
部分肺GCC患者进展快速、容易发生远处转移机制目前并不甚清楚,可能机制如下:①不同类型GCC生物学行为差异大。根据蒋代凤等人研究发现肺GCC存在不同的转移水平,高转移细胞株分泌基质金属蛋白酶-2活性高于低转移细胞株,同时高转移细胞株内的增殖细胞核抗原、CK18蛋白和血管生长因子mRNA显著高表达,P16、钙调蛋白和nm23-H1蛋白显著低表达。这些因素都可促进肿瘤快速生长和远处转移。②不同GCC的增殖能力差异较大。王浩等人发现GCC高转移株细胞(95D)细胞增殖能力显著高于低转移细胞株(95C),处于S期的95D细胞数目也明显高于95C细胞;在蛋白质水平方面,95D细胞P27的表达虽低于95C细胞,但CDK2磷酸化Rb的表达不同程度高于95C 细胞。
2.6、临床治疗及预后
肺GCC的治疗原则是手术为主,术后根据情况辅以放化疗及免疫等综合治疗方法,但化疗效果不明显。一组69例肺GCC患者研究显示,无论单因素或多因素分析,根治性切除与否对患者的生存期影响有统计学意义。此类肿瘤恶性程度高,预后差,因此即使手术多数患者也会在16-18个月内复发或死亡,平均生存期为12月左右。单纯化疗效果不佳,文献报告化疗后首次评估中69%患者仍为疾病进展,EGFR突变情况报告不一,对于EGFR突变患者采用EGFR-TKI治疗疗效报道结果不一。Tamura等报道1例肺GCC患者EGFR19位点突变,吉非替尼治疗无病生存期长达35.9个月;Weng等报道2例EGFR突变患者EGFR-TKI后无病生存期分别是13个月和4.3个月;但Ushiki等报道1例EGFR突变患者采用吉非替尼治疗无效,可能因为患者还存在其他耐药突变。
肺GCC恶性程度高,临床进展迅速,预后较差,影响预后的因素与临床分期有关。而Zhao等研究认为含巨细胞肺癌患者的预后比梭形细胞癌以及含梭形细胞癌患者的差,含巨细胞癌是影响含梭形/巨细胞成分肺癌患者术后生存的危险因素。肿瘤组织有部分坏死、纵隔淋巴结的转移及病理分期晚都预示患者生存期缩短,因此早期诊断,选择合适的治疗方案可延长生命。该肿瘤治疗效果差,重在预防,如避免主动和被动吸烟,避免长期接触粉尘。
总之由于肺GCC发病率极低,临床进展迅速,尚无有效治疗手段,总体预后差,需要对其临床特征、病理形态学特点和治疗方法进一步总结和研究。
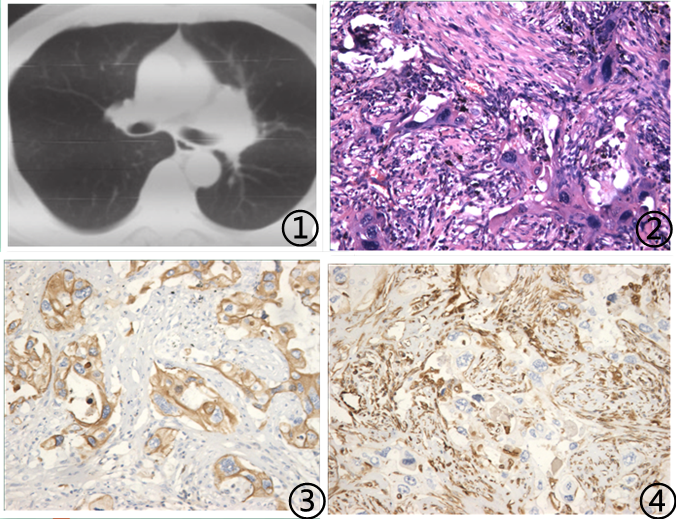
图1X线示肺巨大占位性病变,图2镜下肿瘤细胞分叶状,体积大,胞浆嗜酸性,胞核大且异型明显;图3肿瘤细胞CK弥漫强阳性;图4肿瘤细胞Vimentin阳性。
参考文献略。














共0条评论