众所周知,蛋白激酶对于细胞的存活、生长、分化极为关键,受体酪氨酸激酶(如ALK、RET、MET、NTRK、FGFR、ROS1)与相应配体结合,即为不同的信号传导通路。相关通路的异常在人类癌症发生中具有重要意义,甲状腺癌也不例外,如受体酪氨酸激酶编码基因的重排、导致配体依赖性二聚化在甲状腺癌发生中具有重要意义。相关配体与受体酪氨酸激酶中的激酶结构域结合,产生可以自主活化的融合性致癌蛋白;少见的情况下也有下游信号的转化重组。
具体到甲状腺癌而言,激酶融合相关的癌并不常见,但临床主要见于儿童及年轻人,或见于切尔诺贝利事件的受害者。随着相关研究的不断深入,蛋白激酶抑制剂已经可以用于包括甲状腺癌在内的某些肿瘤临床治疗。不管是较早的多激酶抑制剂,还是选择性较强的新型抑制剂,在甲状腺癌都有较好的效果。不过,临床实践中还存在某些问题,比如对于大部分激酶重排来说,免疫组化标记可能不是太可靠、或尚未得到确切验证;但鉴于尚无条件对所有病例均进行分子检测,因此还需找到某些提示需进行分子检测的临床病理特征;其次,鉴于激酶融合相关甲状腺癌并不常见,因此这组病例的具体分子遗传学特征、长期临床预后等也并不完全清楚。有鉴于此,哈佛大学医学院麻省总医院病理专家Chu等针对激酶融合相关甲状腺癌进行了一项单机构、大规模研究,文章发表于著名病理专业期刊《Mod Pathol》。为帮助大家更好的了解相关内容并注意在临床实践中提高对相关病例的警惕性,我们将该文中与病理有关的重要内容编译介绍如下。
该研究自作者所在单位2013年至2020年5月的相关数据中,共计检索出395例做了靶向基因重排分析的甲状腺原发癌,其中甲状腺乳头状癌212例(54%),髓样癌55例(14%),未分化(间变性)癌39例(10%),滤泡癌36例(9%),嗜酸细胞癌24例(6%),低分化癌23例(6%),甲状腺原发分泌性癌1例(<1%),未分类的癌5例(1%)。
检出激酶融合的病例有62例(16%),具体有乳头状癌57例(14%)(其中经典型29例,弥漫硬化亚型21例,实性亚型4例,滤泡亚型2例,高细胞亚型1例),低分化癌2例(<1%),间变性癌2例(<1%),分泌性癌1例。最常见有重排的激酶基因依次为RET(31例,8%),BRAF(6例,2%),ALK(3例,<1%),MET(2例),ROS(1例)。
病例赏析
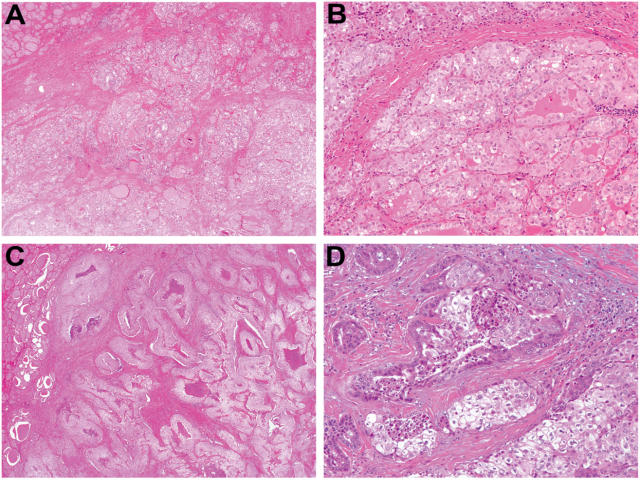
图1. ALK重排的甲状腺癌:(AB)本例为ALK-STRN融合的甲状腺乳头状癌,低倍镜下呈多结节状生长,且有横跨肿瘤的纤维化;高倍镜下可见滤泡结构。(CD)本例为ALK-STRN融合的低分化甲状腺癌,且同时有TP53 c.772G>C突变。组织学上,本例为多个实性结节,且伴粉刺状坏死及广泛纤维化;有一处0.1cm的病灶呈滤泡型乳头状癌表现,且与周围高级别形态区域突然异型;高级别形态区域混有透明细胞、嗜酸性细胞、鳞状细胞且有坏死。
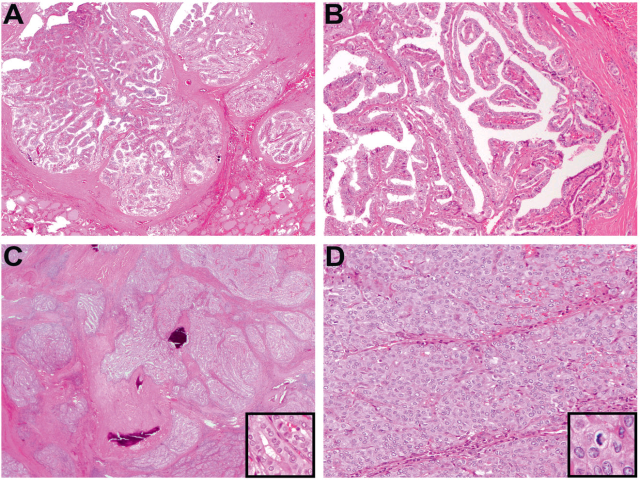
图2. BRAF融合相关的甲状腺癌。(AB)本例在BRAF融合基础上,同时还有TP53的突变以及TERT启动子突变,组织学上为显著乳头结构形成的多发结节,周边有致密纤维化。(CD)本例为SND1-BRAF融合的高细胞亚型乳头状癌,组织学上有广泛纤维化、将肿瘤细胞分隔呈不规则岛状(左图插图示高细胞特征);约10%的肿瘤成分呈实性、梁状结构,且核分裂增加(如插图,最高达4个/10HPF)、局灶有坏死。
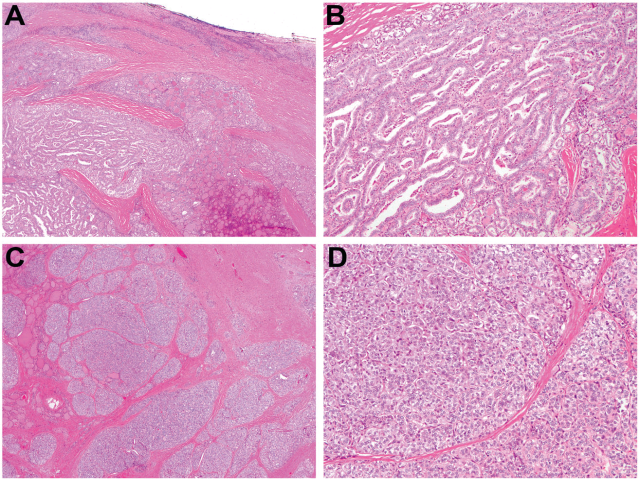
图3. MET重排的甲状腺癌。(AB)一例EML4-MET融合的甲状腺乳头状癌,其特点为分叶状、有横跨病变的纤维化,呈显著滤泡结构并有少量乳头状成分(约占肿瘤的20%)。(CD)一例具有CCDC30-ROS1融合的甲状腺乳头状癌,组织学表现为大量失血结节,细胞淡染至透明,并有分枝状纤维化。
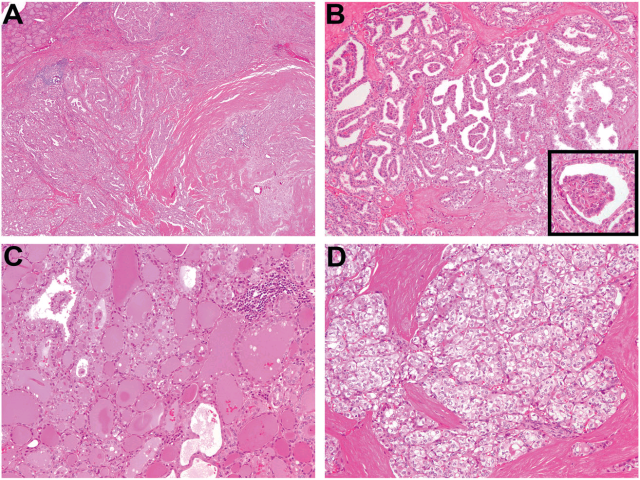
图4. 具有NTRK重排的甲状腺癌。(AB)一例具有 IRF2BP2-NTRK1融合的甲状腺乳头状癌,肿瘤呈分叶状,部分乳头融合,并有少量胶质;肿瘤内散在肾小球样结构。(C)一例具有TPM3-NTRK1融合的甲状腺乳头状癌,主要为滤泡状结构,且有大量胶质,散在小灶的乳头状结构。(D)一例具有SQSTM1-NTRK3融合的甲状腺乳头状癌,组织学呈实性表现,散在微滤泡结构及流水样纤维化。
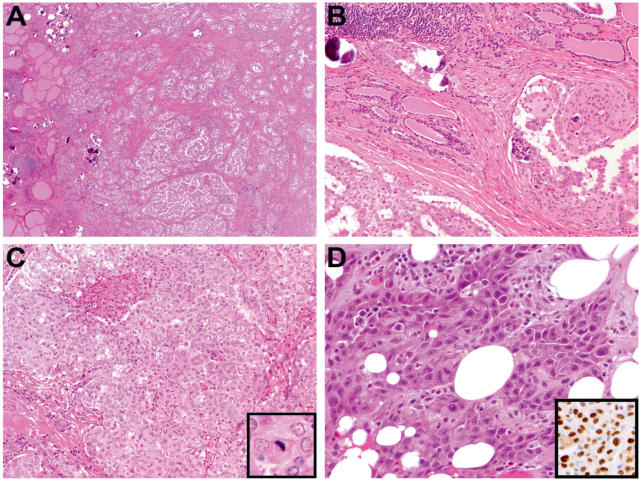
图5. 具有RET融合的甲状腺癌。(AB)一例具有CCDC6-RET融合的甲状腺乳头状癌,组织学表现为大量富于细胞的结节,间质有硬化表现;背景中散在大小不等的砂粒体及伴桑葚状鳞化的肿瘤细胞巢。(C)一例有CCDC6-RET融合、同时有CDH1突变的甲状腺乳头状癌,组织学表现为实性结构,且核分裂高达3个/10HPF,局灶有坏死。(D)一例自儿童期发病、病史较长的甲状腺乳头状癌,在肩胛转移灶处出现了间变性转化;细胞中等程度多形性,呈鳞状表现,常见核分裂;插图示免疫组化PAX8弥漫阳性。
小结
根据相关病例及文献内容,本文原作者提出了甲状腺癌中确定活化激酶融合的相关思路,具体参见下图。
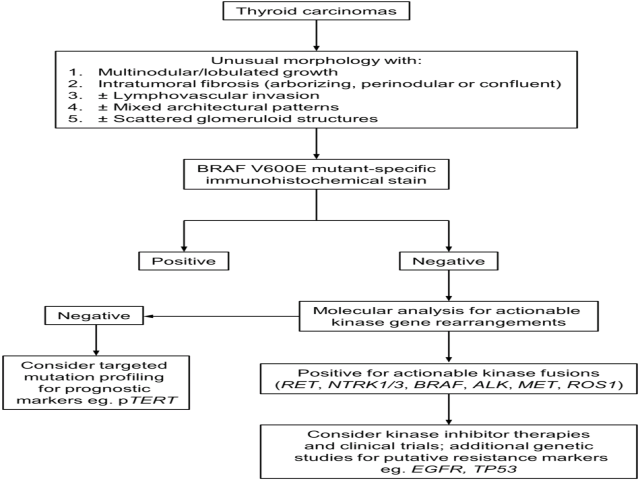
图6. 甲状腺癌中活化激酶融合检查思路。
图6简述:
1.如甲状腺癌中有不常见形态学表现,则应进行BRAF V600E突变特异性免疫组化检查。这些不常见形态学表现有:多结节状/或分叶状生长,肿瘤内有纤维化(可呈树枝状、结节旁、融合性等),脉管侵犯,混合型结构表现,散在肾小球样结构。
2.如BRAF V600E突变特异性免疫组化阴性,则进行活化激酶基因重排的分子检测;如该结果阴性,则考虑对某些具有预后意义的标记进行靶向性突变检测,如pTERT;
3.如活化激酶基因重排分子检测阳性,则可考虑进行激酶抑制剂治疗或参加临床试验;也可对某些耐药标记进行遗传学检测,如EGFR、TP53等。
更多临床及病理相关信息详见原文
点击下载英文文献
参考文献
Chu YH, Wirth LJ, Farahani AA, et al. Clinicopathologic features of kinase fusion-related thyroid carcinomas: an integrative analysis with molecular characterization. Mod Pathol. 2020;10.1038/s41379-020-0638-5.
doi:10.1038/s41379-020-0638-5



















共0条评论