[导读] 编译整理:强子
一文了解磷酸盐尿性间叶性肿瘤(一)
一文了解磷酸盐尿性间叶性肿瘤(二)
六. 磷酸盐尿性间叶性肿瘤中的FGF23及其他磷调节因子
磷酸盐尿性间叶性肿瘤所致的骨软化症大部分是由于FGF23产生过度所介导的。FGF23正常情况下由骨细胞和骨母细胞分泌,作用于近端肾小管上皮细胞,提高尿液中磷酸盐的浓度。FGF23在跨膜共受体α-Klotho的辅助下,与FGF受体(FGFR)结合;其中的Klotho表达于肾脏,与FGF23在肾脏的特异性活性有关。FGF23受体中特征性最为明确的是FGFR1,其传导的信号使得下游涉及细胞增殖、存活、分化、迁移的相关信号激活。如FGF23过量,则钠-磷共转运体发生变化,降低肾脏近端小管对磷酸盐的再吸收。FGF23活性突变是家族性常染色体显性遗传性低磷酸盐性佝偻病的原因。
基于上述基础研究的内容,血清中FGF23的水平也可用于骨软化症的诊断,或者用于相关肿瘤术后复发的监测,并可以通过对不同静脉血样的FGF23水平分析来指导隐匿性肿瘤的定位。对于绝大部分磷酸盐尿性间叶性肿瘤来说,手术切除后FGF23水平迅速下降。
绝大部分磷酸盐尿性间叶性肿瘤可通过mRNA水平、或蛋白水平检测出FGF23的表达,非高磷酸盐尿性的亚型也可检出FGF23的表达。这一指标对于该肿瘤诊断的特异性,取决于所用检测方案,本文原作者认为显色原位杂交相对较好,因为该方案可以在福尔马林固定、石蜡包埋切片中进行且可以定位肿瘤细胞。也有通过免疫组化检测其蛋白表达的研究,但本文原作者认为目前的抗体特异性并不完美。
七. 免疫组化特点
磷酸盐尿性间叶性肿瘤诊断中,免疫组化价值有限。大部分研究均认为该肿瘤免疫表型仅为vimentin阳性,偶有病例会局灶表达CD34、SMA、PGP9.5、S100、Syn、牙本质基质蛋白(dentin matrix protein)-1。最近也有研究称该肿瘤常表达SATB2、CD56、ERG、生长抑素受体2A。SATB2的表达表明该肿瘤具有骨细胞分化。
如前所述,部分病例中也进行了FGF23的免疫组化检测,但目前的商用抗体在特异性方面还有些问题,未能得到广泛应用。
八. 分子遗传学特点
分子遗传学层面来说,大部分磷酸盐尿性间叶性肿瘤都具有FN1-FGFR1的融合;约6%的病例具有FN1-FGF1的融合。约30-40%的病例并未检出上述融合,其具体机制尚有待进一步阐明。
九.“非高磷酸盐尿性”的磷酸盐尿性间叶性肿瘤
近些年已经明确,有些软组织和骨的肿瘤会有磷酸盐尿性间叶性肿瘤的形态学特点,且有FGF23的表达,但且并无明确的骨软化症。这类肿瘤即非高磷酸盐尿性的亚型。
出现这一现象,可能是临床表现的异质性所致,比如部分患者的骨软化症尚未出现临床表现,也有人提出是因为在临床出现显著血磷水平降低之前就发现了肿瘤,还有人认为这组肿瘤的FGF23水平较低、或是患者有某些代偿机制。
十. 非磷酸盐尿性间叶性肿瘤导致的骨软化症
如前文所述,此前曾报道多种类型的间质肿瘤均可视为磷酸盐尿、骨软化症的病因,但是目前认为这些大部分都是误诊的磷酸盐尿性间叶性肿瘤。还有些则是由于着急发表论文所导致的问题。比如本文原作者就曾遇到一例:2004年,考虑患者的骨软化症是由于内生性软骨瘤所致,但2年后,该患者的C1椎体发现了磷酸盐尿性间叶性肿瘤。因此,虽然还不能武断的说肿瘤所致骨软化症的唯一原因就是磷酸盐尿性间叶性肿瘤,但诊断其他肿瘤会导致骨软化症之前还是要慎之又慎,除非证实这一其他肿瘤会产生FGF23、和/或并无磷酸盐尿性间叶性肿瘤相关分子遗传学事件。
目前已明确,多发性、系统性软组织肿瘤及骨肿瘤患者中已有明确的伴血清FGF23升高、肿瘤所致骨软化症的案例,具体如1型神经纤维瘤病情况下的多发性神经纤维瘤、多发性骨纤维性发育不良相关的McCune-Albright综合征。表皮痣综合征中也有伴肿瘤相关骨软化症的罕见病例。
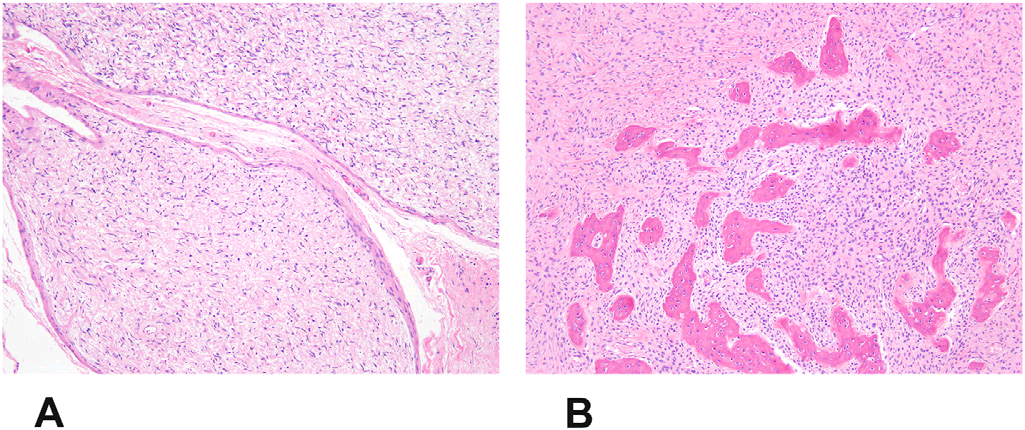
图1. (A)一例1性神经纤维瘤病、多发性丛状神经纤维瘤患者的骨软化症;(B)一例多发性骨纤维性发育不良相关伴内分泌异常(McCune-Albright综合征)患者的骨软化症。这两个病例中,FGF23水平升高似乎是病变整体所致,而不是某单一病变中表达水平高所致。
结肠腺癌、卵巢浆液性癌、前列腺癌、肾脏透明细胞癌、肺的小细胞癌、甲状腺间变性癌中,均有伴血清FGF23水平升高的骨软化症相关报道。
点击下载英文文献
参考文献
Phosphaturic mesenchymal tumors: A review and update[J].Seminars in diagnostic pathology,2019,36(4):260-268.
DOI:10.1053/j.semdp.2019.07.002














共0条评论