[导读] 文章来源:中华神经科杂志,2019,52(2):110-115;作者:张伟赫 汪伟 罗杰 秦耿 焦劲松 王宇 金轶 李争运 顾卫红
摘要
目的
探讨谷蛋白共济失调(gluten ataxia,GA)的临床、影像及小肠病理学特点及其诊治。
方法
回顾性分析中日友好医院神经内科2018年7月收治的1例经临床、血清学及十二指肠病理证实为GA患者的临床表现及诊治过程,并总结其临床特征。
结果
患者为青年男性,临床表现为慢性进行性小脑共济失调,头颅磁共振成像提示小脑蚓部及双侧半球萎缩。血人类白细胞抗原-DQ2位点呈阳性,IgA型抗麦胶蛋白抗体定性为阳性,定量为39.39 RU/ml,十二指肠活体组织检查发现慢性炎症性改变,部分绒毛呈轻度萎缩,上皮细胞内可见淋巴细胞浸润,提示存在亚临床麸质敏感性肠病。诊断上考虑为GA,给予无麸质饮食联合静脉注射丙种球蛋白治疗后,患者小脑语言、走路不稳及日常活动明显好转,2个月后小脑共济失调体征进一步改善,可独自驾车长途旅行。
结论
GA是一类对谷蛋白敏感所致的免疫介导且临床可逆的获得性小脑共济失调。中国大陆人群GA患者基因型、血清学特点及临床表型可能与欧美人群相似。
谷蛋白共济失调(gluten ataxia,GA)为麸质敏感性肠病(乳糜泻)神经系统损害的最常见类型,由Hadjivassiliou等[1]于1998年首次定义,为具有遗传易患性个体长期摄入谷蛋白所致的一类免疫介导性小脑共济失调(cerebellar ataxia,CA)。以往观点认为GA主要在欧美人群中发病,且在该人群进行性散发CA中的占比高达25%[2],而亚洲人群不会或极少发生GA。但随着亚洲国家的饮食"西方化(谷类取代稻类饮食)",日本及伊朗等国家以及中国台湾地区相继有GA病例报道[3,4,5]。据我们所知,到目前为止尚无中国大陆人群GA的完整病例报道。尽管我国学者Guan等[6]通过研究发现,中国大陆散发CA人群中可能存在GA,但该研究仅进行了血清学相关抗体的检测,并未进一步针对患者个体进行基因型、小肠病理及治疗效果等整体评估。我们对我院收治的1例血清学和十二指肠病理证实的GA患者进行报道,并对GA的临床、影像、病理学特点及其诊治要点进行总结,旨在提高临床医生对这一类可治疗性散发CA的认识。
临床资料
一、病例特点
患者男性,41岁,汉族,主因"进行性行走不稳伴言语不利1年半"于2018年7月5日入住中日友好医院神经内科病房。患者于2016年12月左右无明显诱因下自觉容易疲劳,双腿发软。2017年1月开始出现行走不稳,走路时左右摇晃,呈醉酒样。此后行走不稳渐加重,并出现持物不准不稳,讲话费力,呈吟诗样。患者自发病以来无明显头晕、尿便障碍、饮水呛咳、睡眠行为异常、慢性腹泻及皮炎等症状。后患者就诊于上海某三甲医院,行头颅MRI提示小脑萎缩,头部多巴胺转运体PET成像提示双侧尾状核、双侧壳核前部和后部多巴胺分布未见异常,遗传性小脑共济失调基因检测未见明显突变,诊断为多系统萎缩-小脑型(cerebellar type multiple systemic atrophy,MSA-C),给予司来吉兰、金刚烷胺等药物治疗。患者服用上述药物3个月后症状无明显改善便自行停药。随后患者辗转于多家医院均未获得明确诊断。患者既往于2年前曾接触易燃易爆酸性染料,约半年时间。平素饮食以面食(面条、馒头等)居多,吸烟饮酒史20余年,已戒除。否认CA等家族性遗传病史。入院后体检:日常生活能力基本不受影响,但不能完成精细活动。卧位血压106/71 mmHg(1 mmHg=0.133 kPa),立位血压(3 min)112/72 mmHg。意识清楚,中度构音障碍(小脑语言),双侧腱反射活跃,双侧病理征未引出。双侧指鼻试验及跟膝胫试验不稳准,走路呈宽基底步态,罗姆伯格征睁闭眼均不稳。余内科及神经系统体检未见明显异常。
二、实验室检查
血、尿、便常规,生化全套,凝血六项(凝血酶原时间、凝血酶原活动度、国际标准化比值、活化部分凝血酶原时间、纤维蛋白原定量、D-二聚体),心肌梗死四项(肌酸激酶同工酶、肌红蛋白、肌钙蛋白、B型钠尿肽),抗核抗体谱及抗中性粒细胞胞质抗体,肿瘤标志物,甲状腺功能,铜蓝蛋白,血清维生素E水平,白细胞介素组合(IL-1、2、6、8、10)以及免疫球蛋白抗体+补体均正常。传染病检测未发现乙型肝炎、梅毒、人类免疫缺陷病毒感染等传染性疾病。腰椎穿刺测脑脊液压力为80 mmH2O(1 mmH2O=0.009 8 kPa),脑脊液蛋白定量为0.494 g/L(正常值0.15~0.45 g/L),IgG定量为68 mg/L(正常值<40 mg/L)。脑脊液未见肿瘤细胞,TORCH、寡克隆区带、神经副肿瘤抗体(包括抗Yo、锌指蛋白4、超氧化物歧化酶1、脑表皮生长因子跨膜蛋白、谷氨酸脱羧酶65等抗小脑神经元抗体)、自身免疫性脑炎抗体均未见异常。血尿毒物分析未检出重金属、农药及其他毒物。血人类白细胞抗原(HLA)-DQ2位点呈阳性,IgA型抗麦胶蛋白抗体(anti-gliadin antibodies,AGA)定性为阳性(图1A),IgA型AGA定量为39.39 RU/ml(正常值<25.00RU/ml),抗谷氨酰胺转移酶(transglutaminase,TG)抗体阴性,抗肌内膜抗体阴性。HLA基因型和麸质敏感性肠病相关抗体检测由杭州欧蒙医学检验所进行,HLA-DQ2/DQ8采用DNA微阵列法,麸质敏感性肠病相关抗体定性和定量检测采用间接免疫荧光法和酶联免疫吸附(ELISA)法。
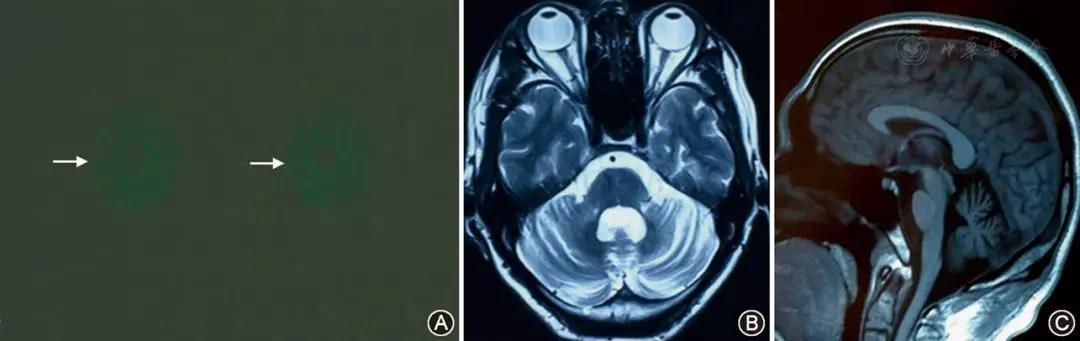
图1 间接免疫荧光法提示患者血清IgA型抗麦胶蛋白抗体阳性(A,绿色圆形荧光,箭头) ×20;头颅磁共振成像提示患者小脑蚓部及双侧半球明显萎缩,第四脑室扩大(B、C)
Figure 1 Indirect immunofluorescence staining showed seropositive IgA type anti-gliadin antibodies (A, green round fluorescence) ×20; Brain magnetic resonance imaging exhibited cerebellar vermis and hemispheres atrophy, with 4th ventricular dilatation (B, C)
三、影像学和神经电生理检查
患者头颅MRI(2018年4月3日,外院)提示小脑蚓部及双侧半球萎缩(图1B、图1C)。单光子发射计算机断层扫描(SPECT)示双侧小脑血流灌注减低,左侧为著(图2)。颈椎MRI和胸部CT均未见明显异常。神经传导及针极肌电图未见感觉运动轴索性神经病,肛门括约肌及尿道括约肌肌电图未见特征性改变,皮肤交感反射未见异常。
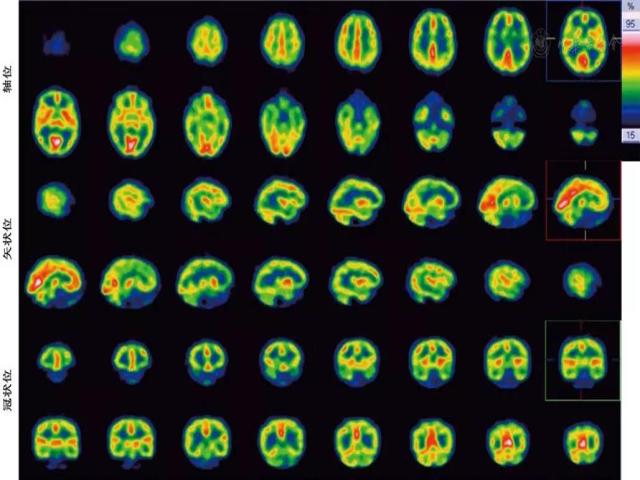
图2 患者行单光子发射计算机断层扫描,示双侧小脑血流灌注减低,左侧为著,大脑半球散在灌注缺失(红色区域减少或消失,参见图片右上角比色条)
Figure 2 Single photon emission computed tomography exhibited diffused hypoperfusion in bilateral cerebellum, and scattered perfusion reduction in both cerebral hemispheres of the patient (decrease of red locations, see color bar on the right side)
四、十二指肠活体组织检查
患者于2018年7月31日行内窥镜十二指肠活体组织检查,于十二指肠球部9点和12点两个位置分别取肠黏膜标本4块。其中1块十二指肠黏膜呈慢性炎症性改变,部分绒毛呈轻度萎缩(图3A),上皮细胞内可见淋巴细胞浸润,免疫组织化学染色显示CD3+ CD4+T淋巴细胞浸润(图3B),未见隐窝增生。
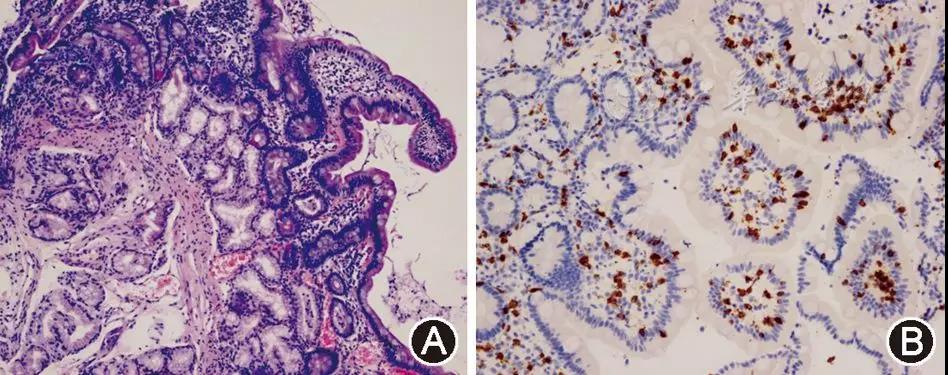
图3 患者十二指肠活体组织检查病理结果。A:HE染色示肠绒毛轻度萎缩×100;B:CD3免疫组织化学染色示肠绒毛可见T淋巴细胞浸润×200
Figure 3 Histopathological findings in duodenal biopsy. A: Hematoxylin-eosin staining showed mild villus atrophy ×100; B: CD3 immunohistochemical staining (brown) identified T lymphocytic infiltration in the intestinal villus ×200
五、治疗及预后
患者于2018年7月14日开始启动无麸质饮食(GFD),自觉停止接触麸质后行走不稳及构音不清等症状逐渐好转。为进一步清除AGA,患者于2018年8月1日接受静脉注射丙种球蛋白0.4 g·kg-1·d-1,连续5 d治疗。同时辅以口服丁苯肽、辅酶Q10、甲钴胺及尼麦角林改善神经元功能等治疗,随访2个月余患者小脑言语、走路不稳及日常活动进一步改善,可独自驾车长途旅行。神经系统体检提示构音障碍、指鼻和跟膝胫试验不稳及罗姆伯格征较入院时均有明显好转。复查IgA型AGA定量为46.23 RU/ml(正常值<25.00 RU/ml)。
讨论
乳糜泻亦称麦胶敏感性肠病或谷蛋白病,由古希腊医生Aretaeos首次描述,Gee[7]于1888年再次报道。然而,直到1953年方被荷兰儿科医生Dicke等[8]推广于世。乳糜泻为一类具有遗传易患性个体摄入谷蛋白后,导致不同系统产生过度免疫反应的自身免疫性疾病,可累及多个脏器,主要表现为肠病、疱疹样皮炎和神经系统疾病[9]。作为乳糜泻神经系统损害最常见的类型,GA最初的定义为谷蛋白敏感的血清学标志物AGA阳性的特发性散发共济失调[1],后续研究发现GA的发病是小脑浦肯野细胞上的抗原成分与谷蛋白存在交叉免疫反应所致[10]。目前已知,欧美人群乳糜泻的发病与人类HLA Ⅱ类分子强烈相关,其中约90%的乳糜泻患者携带HLA-DQ2,而在GA患者中,该基因型约占70%,也就是说HLA-DQ2阳性为诊断GA的充分非必要条件[9]。此外,少数患者可能携带HLA-DQ8[9]。本例患者HLA-DQ2呈阳性,提示中国人群GA可能与欧美人群相似,同样携带HLA-DQ2基因型。
GA通常表现为单纯的CA,多数患者起病隐匿,缓慢进展;平均发病年龄53岁(略晚于乳糜泻患者),男女均可患病。临床上几乎全部患者均表现为步态共济失调,肢体(尤其是下肢)共济失调、构音障碍、眼震及其他小脑眼征亦较为常见[9,11]。少数患者可伴有肌阵挛、舞蹈症、腭肌震颤、眼阵挛肌阵挛综合征等运动症状。多达60%的GA患者同时存在长度依赖的感觉运动轴索性神经病[11]。影像学上,大约60%的GA患者头颅MRI提示小脑萎缩,但全部患者均存在以小脑蚓部为主的磁共振波谱异常(N-乙酰天冬氨酸/肌酸比例显著下降),提示GA患者小脑在发生结构性病变之前已经存在功能异常[11,12]。本例患者即以步态共济失调为首发及主要表现,病程上缓慢进展,逐渐出现肢体共济失调及小脑语言,头颅MRI提示小脑蚓部及半球萎缩,与以往欧美文献报道相符。除此之外,本例SPECT提示小脑弥漫性灌注减低,在以往病例中罕有报道,这一异常是否提示GA的发病存在血管因素(如血管炎机制)参与尚需进一步研究。
小肠活体组织检查为诊断乳糜泻的金标准,为提高检出率,一般建议进行十二指肠多处取检。其典型病理表现包括:(1)绒毛部分或完全萎缩;(2)隐窝增生;(3)上皮内淋巴细胞或浆细胞浸润(>25/100个肠细胞)[13]。与乳糜泻不同的是,GA患者腹泻、胀气等胃肠道症状不足10%,但超过1/3患者的十二指肠活体组织检查可发现与乳糜泻类似的肠道病变[11,14]。我们对本例患者十二指肠共取检4处,其中1处病理发现轻度的绒毛萎缩和淋巴细胞浸润,虽然略轻于Marsh提出的乳糜泻肠病理标准[13],但我们考虑可能存在两点原因:一是患者并不伴有胃肠道症状;二是患者在接受小肠活体组织检查时已进行GFD治疗2周,使得原本较轻的肠道损伤迅速得以恢复。
GA的血清学标志物包括IgA和IgG型AGA、TG抗体系列、抗脱酰胺麦胶蛋白肽(DGP)抗体及抗肌内膜抗体等,几种抗体联合检测可以提高诊断的敏感度和特异度。AGA是最早被发现也曾一度被认为是检测GA最好的血清学标志物,但由于其在MSA-C、遗传性共济失调甚至健康人群中均有一定的检出率[15],因此其临床应用受到极大的挑战。然而,TG6抗体的阳性率可能存在地域和人种差异,TG2抗体仅见于38%的GA患者,且滴度一般较低[11],被认为特异度更高的DGP抗体[16]在成人患者的敏感度却低于儿童人群[9]。因此,在绝对特异的标志物出现以前,尤其对于国内患者来讲,IgA型AGA仍然是诊断GA最适合的指标之一。依据本例患者经验,对于原因不明的散发CA患者推荐常规进行IgA型AGA及TG抗体系列初筛,如条件允许再进行特异度更高的抗肌内膜和DGP抗体进行验证。
GA的诊断主要依赖临床特征和血清学检测,对于具有遗传易患性且有谷蛋白过敏史或胃肠症状的患者,应行血清IgA型AGA和TG抗体系列检测,若阳性且GFD后临床症状逐渐改善,则支持GA的诊断,十二指肠活体组织检查发现典型表现则可进一步证实。然而,考虑到中国国情,加之GA可孤立于乳糜泻其他经典症状单独存在,对CA患者贸然进行多种昂贵的血清学抗体检测和有创性小肠活体组织检查显得不合时宜。因此,依据本例患者诊治经验,我们建议临床上对于病因不明的散发CA,可先行HLA-DQ2/DQ8基因型筛查,若发现患者携带其中一类基因(尤其是HLA-DQ2),在进行血清学抗体检测发现抗体阳性时可行十二指肠活体组织检查进一步验证,同时启动GFD试验性治疗观察疗效。此外,以往研究表明由于AGA在MSA-C和遗传性CA人群中亦有一定的检出率[15],因此在诊断GA时需严加排除。遗传性CA多有明确的家族史和致病基因,而MSA-C则会出现显著的自主神经功能紊乱和睡眠行为异常[17],这在GA患者中均极为罕见,且前两种疾病对GFD均无明显疗效,可资鉴别。本例患者曾被误诊为MSA-C和遗传性CA,然而其临床和电生理均未提示自主神经功能损害,基因筛查亦为阴性,同时排除了副肿瘤小脑变性、中毒、铜蓝蛋白和维生素E缺乏等因素,综合HLA-DQ2和IgA型AGA阳性,十二指肠活体组织检查提示小肠绒毛萎缩和炎性改变,更为重要的是GFD和静脉注射免疫球蛋白治疗有效,考虑诊断GA明确。
无论伴有胃肠道症状与否,GA的治疗仍首选GFD[18],然而治疗效果却取决于CA的病程(小脑浦肯野细胞的丢失为不可逆性损害)长短[9,11]。因此尽早识别并早期治疗显得极为必要。关于GFD能否清除血清中的AGA尚存在争议[11]。对于那些接受GFD之后无效或血清AGA未消失的患者需联合免疫治疗。两项小样本研究发现联合静脉注射免疫球蛋白治疗能够改善绝大多数GA患者的临床症状[4,19]。目前尚无更多证据推荐皮质类固醇激素和其他免疫治疗。本例患者经过2个多月的GFD联合静脉注射免疫球蛋白治疗后血清中IgA型AGA水平并未下降,同样表明GFD和(或)静脉注射免疫球蛋白并不能清除所有GA患者的AGA抗体。然而,考虑到患者CA的临床症状却得以改善,表明AGA滴度可能与GA的预后并无直接相关性。
综上所述,GA是一类对谷蛋白敏感所致的新型、免疫介导且临床可逆的获得性CA。由于其临床上多以不伴胃肠道症状的慢性进行性CA为主要表现,常被误诊为遗传变性病。考虑到后者的不可治疗性特点,对于临床上无明确家族史及自主神经功能损害的患者应尽早进行GA筛查。此外,本研究表明中国大陆人群亦可发生GA,且其基因型、血清学特点及临床表型可能与欧美人群相似。然而,由于国内对GA的研究尚处于初期阶段,尚需增加病例数量以求进一步探究国内患者的人群发病率和临床表征。
参考文献略
















共0条评论