来源:妇产科在线
作者:郑文新
【编者按】HPV病毒载量与宫颈病变的具体关系在学术界一直存在广泛的争议,产生的主要原因是HPV载量测定的标准化问题。例如HC2报告的HPV载量结果,既不能清晰HPV载量的各HPV基因型别组成,也不能明确HPV载量来自于多少样本的细胞数量,因此被称为半定量检测。随着技术的进步,HPV载量测定的标准化问题也逐渐得到解决。例如采用荧光定量PCR技术(qPCR)测定人体细胞内的独特基因,以获得单位细胞的病毒载量,即获得医生取样细胞数量及其相对病毒含量,可更近一步反应真实病毒感染程度。HPV载量测定的标准化问题的解决能否使HPV病毒载量与宫颈病变关系的研究成为新的热点呢?在“第三届 CSCCP 会议暨第十四届全国子宫颈癌前病变及子宫颈癌热点研讨会”上,美国德克萨斯大学西南医学中心 郑文新教授带来的《HPV病毒载量测定在宫颈癌筛查和预防中的角色》讲题,对这相关背景和问题做了详细梳理和阐述。
【专家主要简介】郑文新教授,美国德克萨斯大学西南医学中心Mark and Jane Gibson 冠名杰出荣誉教授,病理学终身教授,妇产科学终身教授。
宫颈癌筛查的历史及HPV测定在宫颈癌筛查及预防中的共识
HPV载量测定从本世纪初开始,其优势一直没有得到很好的发展,所以HPV病毒载量的测定仍然存在很多争议。但是对于以下三点我们已经达成了基本共识:HPV测定对于宫颈癌的筛查是有效的;HPV分型可以作为一个初筛方法;HPV感染,特别是高危类型,是宫颈癌的高危因素。
HPV 载量测定在宫颈癌中的作用
病毒载量的相关问题
通常人们认为感染物质的量越多,疾病越容易产生。然而,目前关于HPV感染的相关文献报道存在争议。HPV病毒载量是指:单位感染上皮细胞中HPV拷贝数。HPV病毒载量的多少决定于两个因素:感染的上皮细胞数量以及感染细胞中病毒的总数量。HPV病毒存在形式为游离病毒(存在于细胞浆及体液)和整合的HPV病毒(在E2位点整合于宿主DNA)。HPV病毒载量在不同时间内的变化,目前还没有大量文献阐述,今后可以尝试调查研究在不同时间内同一种类型的病毒载量变化来预测某种疾病。病毒载量和HPV持续感染的关系仍需研究,由于HPV类型很多,所以关系比较复杂。
病毒载量检测方法
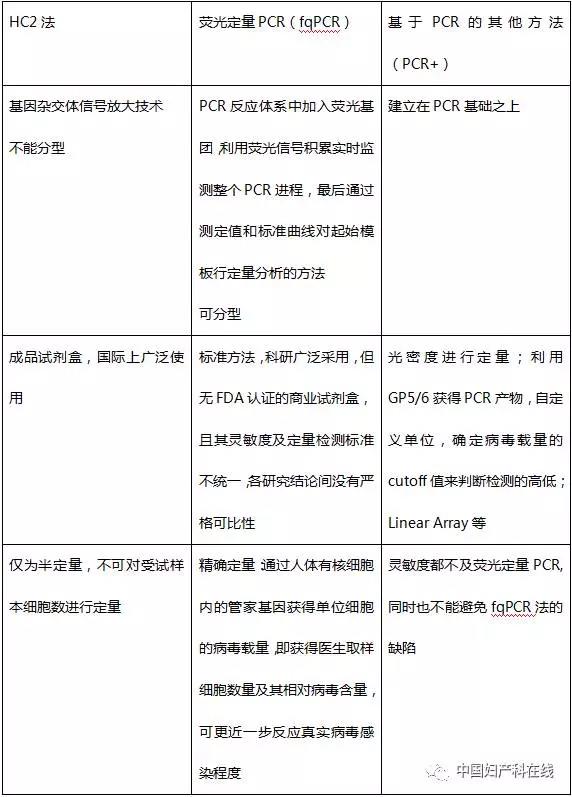
HPV载量检测的临床目的
①找到病毒载量与持续性HPV感染、宫颈癌致病hrHPV型别、宫颈癌病变的细胞学和病理学结果的相关性。
②病毒载量检作为一种生物学标志,可以预测宫颈癌病变疾病演变风险并对疾病进行随访的研究。
病毒载量研究在宫颈癌中的争议
郑文新教授引用相关文献指出病毒载量研究在宫颈癌中的争议,首先提到了病毒载量检测能有效弥补细胞学检查假阴性率高的缺陷(56.Bigras,G.et al.,Br J Cancer, 2005);高病毒载量患者进展为CIN2/3的风险高;初始病毒载量≥100pg/ml的患者在随访过程中病变进展为CIN2/3+的累积风险显著增高(Dalstein,v.,et al.,Int J Cancer 2003);同时提到在随访第8年,HPV16初始高载量的女性其进展为CIN3+绝对风险最高,(Thomsen,L.T.,et al.,Int J Cancer,2005);高载量HPV多重感染进展为CIN2+的风险比高载量单一HPV感染高4—6倍,与细胞学为NILM的女性相比,高载量HPV多重感染与宫颈癌癌前病变显著相关,但在LSIL和HSIL无差异(Schmitt,M.,et al.,J Clin Microbiol,2013);HPV16高载量的女性从最初的正常细胞学开始在随后的15年内其进展为CIN3的风险稳步增高,在15年后高达23%(23.Ylitalo,N.,et al.,Lancet,2000);
郑教授最后向大家分享了深圳一项基于人群的宫颈癌筛查研究,发现高载量HPV感染所占比例随宫颈病变级别升高而逐渐升高(p<0.05)(Luo et al., JLGTD,2017)。同时提到了不支持病毒载量预测宫颈病变分级的文献,横向研究,结果显示鳞状上皮细胞癌患者的平均病毒载量显著高于其他病例,但是应用β-acting标准化后,差异消失;同时该文献还提到HPV载量测定不能区分宫颈癌病变的级别,游离HPV,整合HPV和混合HPV比例随着病变的严重性无差异性改变。(Cheung,JL,J Infect Dis 2006)。有些文献对于病毒载量存在自身矛盾。
对于HPV载量的检测持部分否定意见小结
目前没有完全否定HPV载量对于宫颈病变检测意义的报道。
部分否定的结论:
①HPV载量可以识别宫颈癌,但不能区分病变是HSIL还是LSIL,ASCUS;
②能够鉴别LSIL,但是无法鉴别<CIN2的各级病变;
③HPV病毒载量与细胞学结果相关,但是与组织学结果无关;
④CIN1/2病变中病毒载量高于组织学正常/CIN3+者,不能够预测疾病的严重性;
⑤各级宫颈细胞学结果间,HPV16整合型数量显著不同,但是与疾病的严重性无关;
⑥HPV载量高低与宫颈病变的严重性相关,但是标准化后不相关;
⑦某些HPV型别的病毒载量与疾病严重性相关,但是与其他类型HPV不相关,
⑧混合感染的HPV病毒载量与疾病严重性相关,但是型别特异性病毒载量与疾病严重程度不相关;
⑨应用fq-PCR方法检查HPV载量与疾病严重性相关,但使用HC2法测定,相关性消失。
争议产生的原因可能在于研究对象,标本等材料不同;进行HPV检测方法不同(缺乏标准化检测方法),总的病毒载量,整合型和游离的病毒载量,特异型HPV或者非特异性HPV等HPV检测内容不一等方面;许多无临床研究,其研究设计与样本量不同;对于fq-PCR,大多数采用了管家基因对病毒载量标准化,但是管家基因普遍存在于炎症细胞中。因此,所有试验方法所得到的HPV病毒载量不程度的受到炎症细胞数量的影响;在病例-对照研究和横向研究中,无法确定HPV初始感染时间和持续的时间,限制了有关病毒载量与宫颈病变发展关系的研究;多重HPV感染与宫颈癌发展的相关机制目前尚不清楚。
结论及展望
在美国,HPV病毒载量目前还没在临床应用,但HPV载量相关研究是个热点,预测疾病严重性方面有潜在前景。然而,在HPV病毒载量检测应用于临床前,需要解决以下问题:检测手段标准化,用于临床比较或者相关性研究时,相应的细胞学和阴道镜检查方法也要标准化,需要大样本和足够长的随访时间的临床试验验证。今后病毒载量也可作为一项可行的检测方法,但需要建立病毒载量检测方法标准化,同时需要多中心,大样本的临床前瞻性研究。














共0条评论