[导读] 年初,奥拉帕利(Olaparib)获FDA批准,用于治疗HER2阴性、BRCA阳性的乳腺癌患者。这是第一个批准用于治疗携带BRCA突变乳腺癌的药物,此药继卵巢癌之后又将为乳腺癌患者带来福音。继之而来的必定有临床实践的变化,今天我们就一起来看看最新NCCN指南中,乳腺癌基因检测的相关情况。
一、HER2基因检测
HER2是大家最为熟悉的乳腺癌基因检测。毫无疑问,HER2作为乳腺癌重要的靶向药物预测指标,仍是分子检测的第一步。其检测结果直接影响临床治疗方案,即HER2(扩增)阳性患者可使用靶向药物曲妥珠单抗进行治疗。

图1.HER2状态直接影响治疗方案
这里需要一提的是,2018版ASCO/CAP关于HER2检测的指南中,对HER2扩增的判读标准进行了更新。关于更新内容,在往期的公众号中已有发布,此处不再赘述。目前中国的指南尚未更新,ASCO/CAP指南为我们带来指导的同时,也促使我们思考,到底怎么样的判读标准才更适合国内的情况?
二、BRCA1/2基因检测
乳腺癌除了检测HER2基因外,想必另一个值得关注的就是BRCA1/2基因的检测了。由于安吉丽娜.朱莉事件,使BRCA1/2进入公众视野。大家已经知道,BRCA1/2基因突变可以增加乳腺癌和卵巢癌的发生风险,但检测BRCA1/2基因的意义并不仅限于此。随着研究的不断深入,BRCA1/2检测对指导用药也具有了关键作用。那么到底哪些人应该进行BRCA检测呢?下面我们就从遗传预测和靶向治疗两个方面来谈一下。
1、遗传预测
NCCN中对BRCA检测的原则是这么描述的:满足下列标准中的一个或多个,就需要进一步的个性化风险评估、基因咨询及基因检测和管理。
(1)家族中携带已知致病的BRCA1/2突变
(2)患乳腺癌且含有一个或多个下列情况:
① 确诊年龄≤45岁
② 确诊年龄46-50岁且:
●在任何年龄存在额外的原发性灶
●≥1位血缘近亲患者乳腺癌(在任何年龄)
●≥1位血缘近亲患有前列腺癌(Gleason score ≥7)
●未知或有限的家族史a
③ 确诊年龄≤60岁的三阴性乳腺癌
④ 任意年龄确诊且:
≥1个血缘近亲有以下情况:
●乳腺癌确诊年龄≤50y
●卵巢癌
●男性乳腺癌
●转移性前列腺
●胰腺癌
≥2个额外的乳腺癌原发灶(任何年龄或血缘近亲中存在此种情况)
(3)德系犹太人血统
(4)男性乳腺癌
(5)胰腺癌
(6)转移性前列腺癌
(7)任何年龄的前列腺癌(Gleason score ≥7)且:
① ≥1位血缘近亲确诊为卵巢癌、胰腺癌或者转移性前列腺癌,或者年龄≤50岁确诊乳腺癌
② ≥2位血缘近亲在任何年龄确诊乳腺癌或前列腺癌
③ 德系犹太人血统
(8)在没有胚系突变分析的情况下,在肿瘤样本中检出BRCA1/2突变
(9)无论家族史如何,以确定一些患者是否能从靶向治疗中获益
(10)不符合其他标准,但≥1位一级或二级亲属有以上情况,应讨论解释未受影响个体检测结果的重大局限性。
2、靶向治疗
上面已提到,对于靶向治疗的检测,是不需要考虑家族史的。对于适合单药治疗的HER2阴性复发或IV期(M1)乳腺癌患者,建议检测BRCA1/2胚系检测;BRCA1/2突变的患者,可以采用PARP抑制剂奥拉帕尼进行治疗。

图2.HER2阴性患者强烈建议检测BRCA1/2胚系突变
三、乳腺癌21基因检测
NCCN指南中建议,淋巴结阴性、激素受体阳性、HER2阴性的患者可进行21基因检测,并根据复发评分来确定治疗方案。但由于中国没有自己的大数据支持,亦或存在其它原因,目前国内鲜有开展此项目。期待不远的将来,这项检测能为我国乳腺癌患者带来帮助。
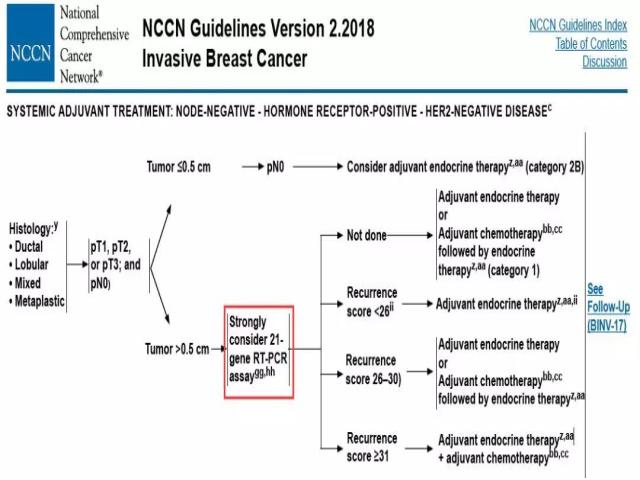
图3:NCCN指南建议检测乳腺癌21基因
四、PIK3CA基因检测
乳腺癌中PI3K/AKT 信号通路异常非常常见,其中PIK3CA的突变最为常见,突变率高达30%。有不少研究表明,携带PIK3CA基因突变的患者对HER2靶向药物治疗存在耐药性,但目前NCCN指南中尚未纳入PIK3CA基因检测。乳腺癌中的PIK3CA基因突变是否需常规检测,有待观望。
注:
a. NCCN(National Comprehensive Cancer Network):美国国立综合癌症网络。其每年发布的各种恶性肿瘤临床实践指南,得到了全球临床医师的认可和遵循,是临床治疗中主要的参考依据。
b.本文引用指南内容来自于:乳腺癌NCCN指南(2018.V2)及遗传家族高风险评估-乳腺癌和卵巢癌NCCN指南(2019.V2)
















共0条评论