[导读] 随着高分辨CT的普遍应用,以及肺癌筛查的开展,CT上表现为GGO的病例增多,为了明确性质,可能会采取经皮肺穿刺等方法进行活检,以期得到病理结果。GGO是一个影像学概念,在组织学上会有什么样的表现、对GGO进行活检得到的小标本应该如何处理以及如何诊断,成为人们关注的问题。
作者:朱翔(北京大学医学部病理学系 北京大学第三医院病理科)
GGO的概念
GGO的英文全称是Ground-glass opacity,即磨玻璃密度影,一般是指高分辨率或薄层CT图像上肺组织密度轻度增加的影像表现,但其内的支气管血管束仍可显示。GGO可进一步分为纯GGO及混合型GGO。
GGO的病理学基础
GGO在组织病理学上,可以表现为多种形式。比如肺泡壁增厚、肺泡腔塌陷、肺泡体积缩小、含气量减少以及肺泡腔内出现细胞、渗出液及组织碎片。这些现象都可能导致CT上这部分肺组织密度轻度增加。但究竟是什么原因导致上述变化,是我们取活检送病理最关注的,也就是GGO的病理诊断。
GGO的可能病理学类型
1. 非肿瘤性病变
①肺淤血、肺水肿可由于肺泡间隔内毛细血管扩张充盈、肺泡腔内水肿液的渗出而导致肺泡壁增厚、肺泡腔内含气量减少,在CT上可表现为GGO;
②非特异性间质性肺炎(NSIP)可因肺泡间隔及间质内多量慢性炎细胞浸润(富细胞型)或纤维化、胶原沉积(纤维化型)而致肺泡间隔增宽,亦可在CT上表现为GGO;
③脱屑性间质性肺炎(DIP)、肺泡蛋白沉积症等则因为肺泡腔内出现了较多的巨噬细胞或蛋白性颗粒样物质充填了肺泡腔而致GGO的表现。
上述均为非肿瘤性病变在CT上均表现为GGO,但是往往成片、多灶或境界不清。
2.肿瘤性病变
①我们目前关注的是境界清楚的磨玻璃密度病变及磨玻璃密度结节(GGN)。而这一类病变的恶性可能性增加。肿瘤性GGN在病理上主要表现为肿瘤性的上皮细胞沿着肺泡壁生长,即贴壁生长,然后在其基础上根据肿瘤细胞的类型、病变范围的大小及有无浸润进行进一步的分型。
②根据2015版WHO肺肿瘤分类,以贴壁生长为主的腺上皮病变,包括浸润前病变、不典型腺瘤样增生(AAH)和原位癌(AIS)(非粘液性、粘液性)。
如果贴壁生长的范围≤0.5,为AAH
如果肿瘤整体范围>0.5厘米,≤3厘米,全部为贴壁生长,则为AIS,在CT上可能表现为纯GGO/GGN
如果肿瘤细胞出现呈贴壁生长以外的生长方式,如腺泡状、乳头状、微乳头状、实体性生长,或浸润了间质,而这些病变范围≤0.5厘米,则称为微浸润性腺癌(MIA)
如这些病变范围>0.5厘米,则诊断为浸润性腺癌
如果出现淋巴管、血管、胸膜侵犯,或出现肿瘤性坏死或气道播散,则无论范围大小,均称为浸润性腺癌。其中贴壁生长以外的成分,在CT上可能表现为密度更高的实性部分,此时称为混合型GGO/GGN。
③如果贴壁生长的肿瘤细胞呈粘液柱状,甚或出现杯状细胞,根据有无浸润及浸润范围的大小可能表现为粘液性原位癌、粘液性微浸润性腺癌,或浸润性粘液腺癌。由于粘液的分泌,肺泡腔内可能充填多少不等的粘液,相比于非粘液性贴壁生长为主的腺癌,在CT上密度会增加,甚至表现为实性,一定程度上失去磨玻璃密度的特点。
④如果肿瘤>3厘米,但绝大多数的范围均表现为贴壁生长,而浸润的成分≤0.5厘米,虽然不能放入微浸润性腺癌的范畴(微浸润性腺癌的诊断要求肿瘤大小不超过3厘米),但是其生物学行为可能非常好,提示浸润与否及其范围是影响肿瘤生物学行为更重要的因素。
⑤如果肺野中出现多个GGN,需要判断多原发或肺内转移的可能。但目前没有证据级别非常高的判断标准。以下几点可以借鉴:
是否为同时发生
有无淋巴结转移
组织学类型是否相同
有无原位病变
基因状态是否相同
⑥有一些肿瘤转移至肺,在CT上也可以表现为GGO/GGN。例如黑色素瘤转移至肺,在一定时期,肿瘤细胞可以沿着肺泡壁浸润生长,肺泡的结构轮廓可以大致保持,在CT上密度增加,但非实性。
GGO小标本取材及诊断术语
1.小标本取材及固定
①CT或B超引导下的经皮肺穿刺活检、经纤维支气管镜肺组织活检等所取到的标本,均称为活检标本,俗称小标本。小标本的诊断对于疾病的定性、分型和靶向治疗意义重大。
②标本从离体到固定时间不宜超过半小时,活检标本直接放入固定液(10%中性缓冲福尔马林)中,固定时间≥6小时、≤24小时,活检标本应全部取材。
2.小标本的病理诊断
2015版WHO对小标本的诊断术语提出了建议。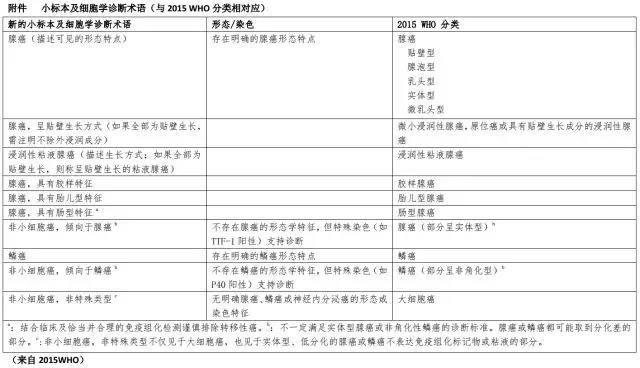
①对于有明确形态学特征和免疫组化表型的病变,小标本可直接诊断具体病变类型。
②由于取材的局限性,无法对病变进行全面评价,故类似原位癌、微浸润性腺癌、肉瘤样癌、大细胞癌等则无法直接诊断。
③对于对病变成分的比例有要求的肿瘤,比如腺鳞癌等,也无法在小标本上直接诊断。但是小标本中所体现的组织学的特点及构成,均能够也应该在诊断中予以体现。故在诊断术语中,可以使用倾向于某种类型,或对具有的某种特征予以说明,请参见下表。
④对于没有任何形态学分化并且免疫组化及特殊染色均为阴性的肿瘤,可诊断为非小细胞癌组织类型不明确型(NSCLC,NOS),其所对应的切除标本的诊断为大细胞癌。
3.小标本的基因检测
①对诊断为腺癌或NSCLC,NOS的小标本,或不吸烟、年轻的鳞癌患者的小标本,应该进行基因检测。2018NCCN指南提出应常规进行EGFR、ALK、ROS1的基因检测。
②面对标本小,检测项目多的情况,合理使用标本,尽量做到诊断与检测彼此兼顾,非常重要。病理科与临床科室多交流、沟通,建立合适的流程,利用有限的标本尽力完成患者的病理诊断与基因检测。比如临床科室提供详尽的病史及临床资料,便于病理科鉴别诊断;病理科在保证准确性的前提下,用尽量少的免疫组化指标完成诊断,节省标本进行基因检测;临床科室和患者充分沟通,对基因检测的项目予以确定,避免反复追加检测项目。
③GGO/GGN是目前肺癌早期筛查和诊断中常常遇到的情况,其诊断与鉴别诊断具有重要意义,而临床、影像、介入以及病理的协同合作是重要环节。














共0条评论