本标准起草单位: 复旦大学附属肿瘤医院、河北医科大学附属第二医院、北京朝阳医院
本标准起草人: 杜祥、张祥宏、金木兰
来源:中国抗癌协会肿瘤病理专业委员会
1、范围
本标准规定了胃癌的病理诊断的程序及基本要求。本标准适用于全国各级各类医疗卫生机构对胃癌的病理诊断。
2、规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅所注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
《临床技术操作规范-病理学分册》
《病理科建设与管理指南(试行)》(卫办医政发(2009)31号)
《肿瘤病理规范化诊断标准总则》
3、术语和定义
3.1 胃癌gastric carcinoma
来源于胃黏膜上皮细胞的恶性肿瘤。
3.2 上皮内瘤变/异型增生gastric intraepithelial neoplasia, GIN/ Dysplasia
胃黏膜上皮不同程度的细胞和结构异型性为特征的病变,根据病变程度,分为低级别和高级别两级。
3.3 早期胃癌early gastric carcinoma
限于黏膜、或黏膜和黏膜下层的侵袭性癌,无论淋巴结是否有转移。
3.4 进展期胃癌advanced gastric carcinoma
癌组织侵达肌层或更深者,无论其有否淋巴结转移。
4、标本类型及固定
4.1 标本类型
日常工作中常见的标本类型包括:内镜活检,内镜下黏膜切除术/内镜下黏膜剥脱术标本(EMR/ESD)(参考文献1)和根治术标本。
4.2 标本固定
4.2.1 标本的采集与送检,编号与登记、固定液及固定时间参见总则。
4.2.2 获取后的标本应及时固定(宜半小时内固定)。
(1)内镜活检标本:离体后,应由内镜医师及时将活检黏膜组织基底面粘附于滤纸上,立即浸入固定液中固定。
(2)内镜下黏膜切除术/内镜下黏膜剥脱术标本:应由内镜医师展平标本,黏膜面向上,使用大头针固定于软木板(或泡沫板)上,避免过度牵拉导致标本变形,标记口侧及肛侧方向,黏膜面朝下(图1 )后立即放入固定液,宜行基底切缘及侧切缘的标记,以利于镜下切缘的辨认(参考文献1、2)。
图1内镜下黏膜切除术/内镜下黏膜剥脱术标本固定示意图


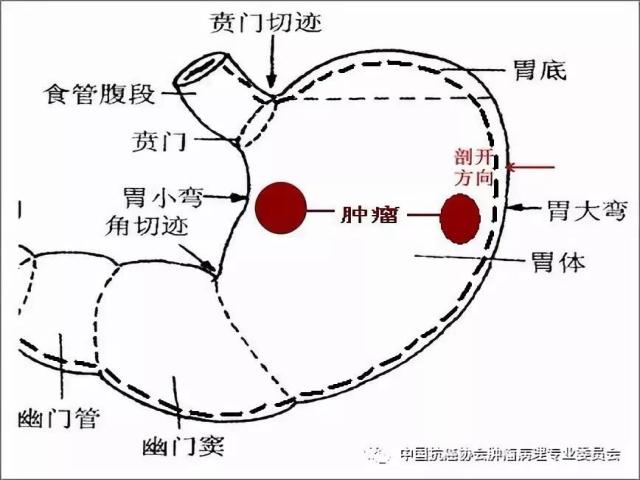
(3)根治标本,通常是沿胃大弯侧打开胃壁,如肿瘤位于胃大弯,则避开肿瘤沿大弯侧打开胃壁,确保标本的充分渗透和固定(图2)。
图2 标本固定前剖开示意图

5、取材及大体描述规范
取材时,应再次核对基本信息,如姓名、床位号、住院号、标本类型。
5.1 活检标本
5.1.1 描述及记录
描述送检组织的大小及数目。
5.1.2 取材
送检黏膜全部取材,应将黏膜放置于纱布或透水纸中以免丢失,必要时可标记。
5.2 内镜下黏膜切除术/内镜下黏膜剥脱术标本
5.2.1 大体检查及记录
测量并记录标本和肿瘤的大小(长径×短径)、肿瘤的肉眼分型以及肿瘤各方位距切缘的距离,并建议进行大体标本拍照。
5.2.2 取材
由于肿块距切缘距离一般较近,切缘的评估尤其重要。宜标记基底及侧切缘,以便在镜下观察时能够对切缘做出定位,并评价肿瘤切缘情况。
每间隔2-3mm平行切开标本(图3),如临床特别标记可适当调整,分成大小适宜的组织块,应按同一包埋方向全部取材。记录组织块对应的方位(宜附图并做好标记)。黑色实线示包埋面,红色虚线示不需包埋面。
图3内镜下黏膜切除术/内镜下黏膜剥脱术标本取材示意图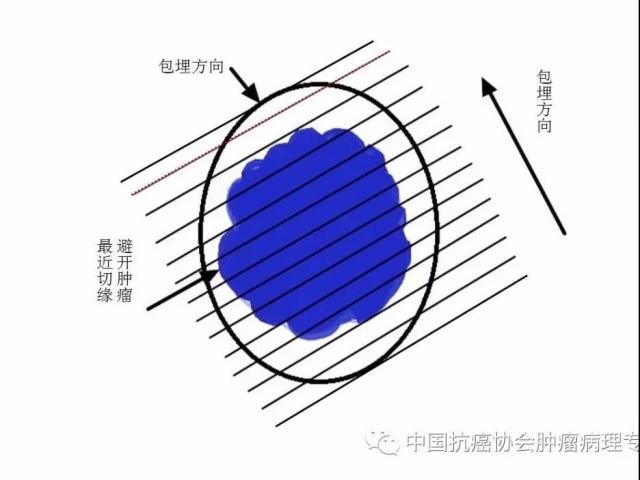
5.3 根治术标本
5.3.1 大体检查及记录
应根据幽门及贲门的特征来正确定位。测量胃大弯、小弯长度,胃网膜的体积;检查黏膜面,应描述肿瘤的部位、大小(新辅助治疗后标本,测量瘤床的大小;内镜下黏膜切除术后标本,描述溃疡/黏膜缺损区/疤痕的大小以及有无肿瘤的残余)、数目、形状、浸润深度、浸润范围、肿瘤与两侧切缘的距离。应观察除肿瘤以外的胃壁黏膜是否有充血、出血、溃疡、穿孔等其他改变;观察浆膜面有无充血、出血、渗出、穿孔、肿瘤浸润等;肿瘤周围胃壁有无增厚及弹性情况;如有另送的脾脏、十二指肠等,依次描述。宜做肿瘤浆膜面的标记,以正确评估肿瘤浸润深度。
应按临床医生已分组的淋巴结取材;
如临床医生未送检分组淋巴结,应按淋巴结引流区域对胃周淋巴结进行分组(图4),一般分为贲门淋巴结,小弯侧淋巴结(胃左淋巴结+胃右淋巴结),幽门上淋巴结、幽门下淋巴结和大弯侧淋巴结(胃网膜左淋巴结+胃网膜右淋巴结)。所有检出淋巴结均应取材。未经新辅治疗的根治术标本应至少检出15枚淋巴结。
应描述淋巴结的数目及大小,有无融合,有无与周围组织粘连,如有粘连,注意需附带淋巴结周围的结缔组织。
图4 胃淋巴结分组
5.3.2 取材
(1)肿块:如见明显肿块,取材应不少于4块,须包括肿瘤浸润最深处、肿瘤与肿瘤周围交界部位的组织;若病变不明显或新辅助治疗后根治术标本,则可疑区和瘤床需全部取材,应附图显示并标记取材组织块的位置。如见其他异常病灶,应取材。推荐取材组织大小不大于2.0×1.5×0.3cm。
(2)切缘:胃的远端、近端切缘常规至少取材各一块,如肿瘤距切缘较远(≥4cm),可切缘离断取材;如肿瘤距切缘较近及无法判断肿瘤与切缘的关系时,应取材垂直切缘。
(3)应取材除肿瘤以外的胃壁黏膜(充血、出血、溃疡、穿孔等其他改变)。
(4)应取材周围正常胃黏膜。
(5)应全部包埋分组淋巴结,较大淋巴结应剖开。
(6)应取材另送检的十二指肠、脾脏等其他器官。
6、病理诊断分类、分级和分期方案
6.1 组织学分型(附件1,表1,参考文献3)
推荐同时使用WHO(消化系统肿瘤)和Laurén分型。
6.2 组织学分级
依据腺体的分化程度分为高分化、中分化和低分化(高级别、低级别)。
6.3 胃癌分期(附件2)
推荐美国癌症联合会(AJCC)和国际抗癌联盟(UICC)联合制定的分期。
7、HER2检测 (参考文献4)
确诊胃癌病例应进行HER2检测。
8、新辅助治疗后根治术标本的病理学评估(附件3)
新辅助治疗后病理学改变的基本特征包括:肿瘤细胞退变、消退,大片坏死。纤维组织增生、间质炎症细胞浸润,钙盐沉积等。可能出现大的无细胞黏液湖,不能将其认为是肿瘤残余。
胃癌的疗效分级系统宜采用NCCN指南标准。
9、病理报告内容及规范(附件4)
9.1 病理报告内容应包括标本类型、肿瘤部位、肉眼分型、肿瘤大小、组织学类型及分级,浸润深度,有无合并其他肿瘤成分,有无脉管侵犯,切缘及淋巴结转移情况。应评估标本切缘及黏膜下浸润深度(内镜黏膜切除术标本)。
9.2 应评估新辅助治疗后根治术标本疗效反应。
9.3 应报告合并的其他病变。
附件1
胃癌WHO分型
WHO2010(第四版)
乳头状腺癌
管状腺癌
黏液腺癌
低黏附性癌(包括印戒细胞癌及其他变异型)
混合型腺癌
少见亚型
腺鳞癌
伴有淋巴样间质的癌
肝样腺癌
鳞状细胞癌
未分化癌
绒毛膜癌
癌肉瘤
壁细胞癌
粘液表皮样癌
胚胎型癌
内胚窦瘤
嗜酸细胞腺癌
潘氏细胞癌
表1 Laurén分型及WHO分型对应表
Laurén分型 | WHO分型 |
肠型 | 低级别乳头状腺癌 低级别管状腺癌 |
混合型 | 高级别乳头状/管状腺癌 |
弥漫型 | 无或很少有腺管形成的癌包括(包括印戒细胞癌及其他变异型) |
不确定型 | 未分化癌 腺鳞癌 鳞状细胞癌 小细胞癌 其他少见类型胃癌 |
附件2
胃癌TNM分期(2010年AJCC)
T 原发肿瘤
Tx 原发肿瘤不能评估
T0 无原发肿瘤证据
Tis 原位癌:无黏膜固有层侵犯的上皮内瘤变,高级别异型增生
T1 肿瘤侵及黏膜固有层、黏膜肌层或黏膜下层
T1a 肿瘤侵及黏膜固有层或黏膜肌层
T1b 肿瘤侵及黏膜下层
T2 肿瘤侵及固有肌层
T3 肿瘤侵及浆膜下层
T4 肿瘤侵透(穿破)浆膜层或侵犯邻近器官
T4a 肿瘤侵透浆膜(脏层腹膜)
T4b 肿瘤侵犯邻近器官
N 区域淋巴结
Nx 区域淋巴结不能评估
N0 无淋巴结转移
N1 1~2个淋巴结转移
N2 3~6个淋巴结转移
N3 7个或7个以上淋巴结转移
N3a 7~15个淋巴结转移
N3b ≥16个淋巴结转移
M 远处转移
M0 无远处转移
M1 远处转移
胃癌分期
分期 | T | N | M |
0期 | Tis | N0 | M0 |
IA期 | T1 | N0 | M0 |
IB期 | T2 | N0 | M0 |
T1 | N1 | M0 |
IIA期 | T3 | N0 | M0 |
T2 | N1 | M0 |
T1 | N2 | M0 |
IIB期 | T4a | N0 | M0 |
T3 | N1 | M0 |
T2 | N2 | M0 |
T1 | N3 | M0 |
IIIA期 | T 4a | N1 | M0 |
T3 | N2 | M0 |
T2 | N3 | M0 |
IIIB期 | T4b | N0 N1 | M0 |
T4a | N2 | M0 |
T3 | N3 | M0 |
IIIC期 | T4a | N3 | M0 |
T4b | N2 N3 | M0 |
IV 期 | 任何T | 任何N | M1 |
附件4
胃癌病理诊断报告书推荐格式
一、胃癌根治术标本报告格式
姓名: 性别: 年龄: 送检日期: 病理号:
住院号: 床号: 科室: 送检医师: 标本类型:
肉眼所见:
胃癌根治术标本:大弯长20cm,小弯长14cm,大网膜16×15×10cm,于胃窦小弯侧见一6.5×4.0×1.5cm肿块,距上切缘3cm,距下切缘4cm,切面灰白灰红色,有坏死,肉眼浸润至浆膜面,肿瘤周围黏膜未见其他病变。
另送:
(1)贲门淋巴结:7枚,直径0.3-0.9cm;(2)小弯淋巴结:4枚,直径0.4-0.6cm;
(3)大弯淋巴结:2枚,直径0.3-0.4cm;(4)幽门上淋巴结:3枚,直径0.4-0.5cm;
(5)幽门下淋巴结:3枚,直径0.3-0.5cm;
另送近端切缘:环状黏膜组织一块,1.5×1.0×0.5cm。
另送远端切缘:环状黏膜组织一块,2.0×1.0×1.0cm。
病理诊断:
(全胃)腺癌,中分化。肠型(Laurén分型)。肿瘤浸润至浆膜层,可见脉管及神经侵犯,标本近端及远端切缘未见癌累及,周围黏膜未见其它病变。
淋巴结(4/20)见癌转移,其中:贲门淋巴结(3/7),小弯淋巴结(1/4),大弯淋巴(0/2),幽门上淋巴结(0/3),幽门下淋巴结(0/3)另送第8组淋巴结(0/1)。
pT4N2M0
HER2(免疫组织化学):肿瘤细胞 3+
报告医师签名: 审核医师签名: 报告日期: __________________________________________________________________
二、内镜下胃黏膜切除标本:
姓名: 性别: 年龄: 送检日期: 病理号:
住院号: 床号: 科室: 送检医师: 标本类型:
肉眼所见:
黏膜组织一块,大小40×30mm,病变大小20×15mm,肉眼分型IIa+IIc,四周断端肉眼未见病变。
病理诊断:
(内镜下黏膜切除)乳头状腺癌,高分化。肿瘤侵透黏膜肌层,浸润黏膜下层,黏膜下浸润深度0.2mm,未见脉管侵犯。水平切缘及基底切缘未见肿瘤。
pT1bNxMx。
HER2(免疫组织化学):肿瘤细胞 3+
报告医师签名: 审核医师签名: 报告日期:
___________________________________________________________________________
点击查看PC端视频
点击查看手机端视频
参 考 文 献
1.中国消化内镜活组织检查与病理学检查规范专家共识(草案)(2014版). 中华消化杂志,2014,34(9):577-581
2. 消化道黏膜病变内镜粘膜下剥离术治疗专家共识(2012版).中华胃肠外科杂志,2012,15(10):1083-1086
3.Laurén P. The two histological main types of gastriccarcinoma: diffuse and socalled intestinal-type carcinoma. An attempt at ahisto-clinical classification. Acta Pathol Microbiol Scand.1965; 64: 31-49.
4.中国胃癌HER2检测指南,中华病理学杂志,2011,40,8:553-557



















共0条评论