[导读] 作者:周志华(无锡101医院病理科)
临床信息:患者女,42岁,因腹痛来我院消化内科就诊。行胃镜检查,于胃底和胃窦处各见一扁平隆起,大小分别为0.3cm和0.6cm,对两处病灶进行活检。
实验室检查:血常规:血红蛋白 101 g/L; 胃蛋白酶原检测:PGⅠ3.9 ng/ml (正常值:>80 ng/ml) , PGⅡ 19.0 ng/ml(正常值:<40 ng/ml), PGⅠ/PGⅡ比值 0.29(正常值: ≥3.89)。血胃泌素检测值 387.9 pg/ml (正常值:< 100 pg/ml)。
影像学检查:腹部MRI:肝、胰腺、脾、双肾及肾上腺未见异常。
光镜所见:
一、胃底黏膜:
1.见增生的上皮样细胞,呈实性片状、巢状或腺样排列,细胞形态较一致,胞核染色质细腻,核分裂像少见(图1a,b);免疫组化显示上述瘤细胞CgA (图1c)、Syn和CD56均阳性,不表达胃泌素,Ki67增殖指数< 2%。CgA免疫组化还显示肿瘤周边的腺体存在神经内分泌细胞的“线性增生”,即一个腺管内出现5-6个神经内分泌细胞;部分腺体内神经内分泌细胞更为明显,阳性细胞数可明显超过6个(图1d)。
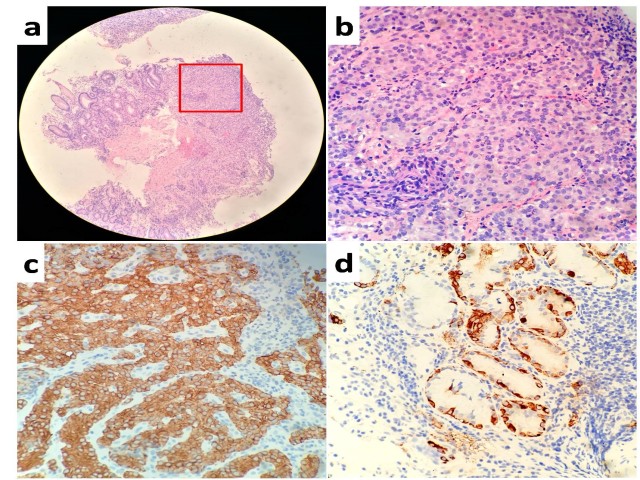
图1.胃底处病变。图a,b显示神经内分泌肿瘤病灶(图b为图内红色方框区域的放大图像);图c,免疫组化显示瘤细胞表达CgA; 图d,CgA免疫组化染色,显示肿瘤旁黏膜的腺体内神经内分泌细胞呈“线性增生”(一个腺管内出现5-6个神经内分泌细胞),部分腺管阳性细胞数可超过6个。
2.肿瘤周边胃底黏膜,未见泌酸腺,代之以幽门腺样的黏液腺(假幽门腺化生,图2a),局灶还可见肠上皮化生(图2b),固有层内有较多淋巴细胞浸润(图2a),可深达黏膜肌内;免疫组化显示,化生的腺体表达MUC6(图2c),与胃窦幽门腺具有相似的表型,证实瘤旁胃底黏膜出现假幽门腺化生;同时,化生的腺体胃泌素表达呈阴性(图2d),说明腺体内不含G细胞。由于G细胞在胃窦黏膜必然出现,因此说明胃镜取材部位确实不是胃窦,也从侧面证实上述腺体出现假幽门腺化生。
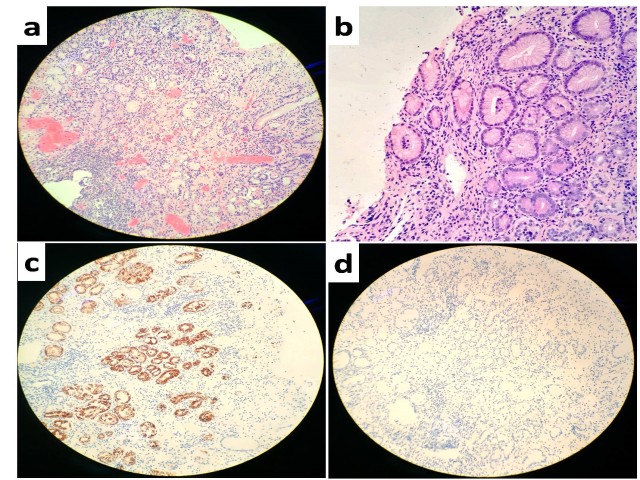
图2.胃底处瘤旁胃黏膜的病变。图a,黏膜内见显著的淋巴细胞浸润;图b,部分腺体肠化(白色箭头),可见杯状细胞和嗜酸性的吸收上皮;图c,免疫组化显示腺上皮表达Muc6,说明其具有胃窦幽门腺的分化特征(假幽门腺化生);图d,为图c的连续切片,免疫组化染色标记胃泌素,所有腺体均为阴性,提示取材部位并非胃窦,进一步证实该处病变为假幽门腺化生。
二、胃窦黏膜:
1.亦见形态单一的瘤细胞,呈巢状、腺管样排列,核分裂像少见,局灶见瘤细胞浸润黏膜肌层(图3a);免疫组化显示,瘤细胞表达CgA(图3b)、Syn和CD56,但不表达胃泌素,Ki67增殖指数< 2%。
2.肿瘤周边的胃窦黏膜,见一定量的淋巴细胞浸润,但腺体无萎缩或肠化(图3c);免疫组化显示腺体内部分细胞表达胃泌素,每个腺管内阳性细胞数多在5个以上(图3d,该图主要显示腺管的横切面,如在纵切面上显示,每个腺体的阳性细胞应明显超过5个)。由于正常胃窦的每个腺体中G细胞数量一般不超过5个,上述结果说明胃窦黏膜存在G细胞增生。
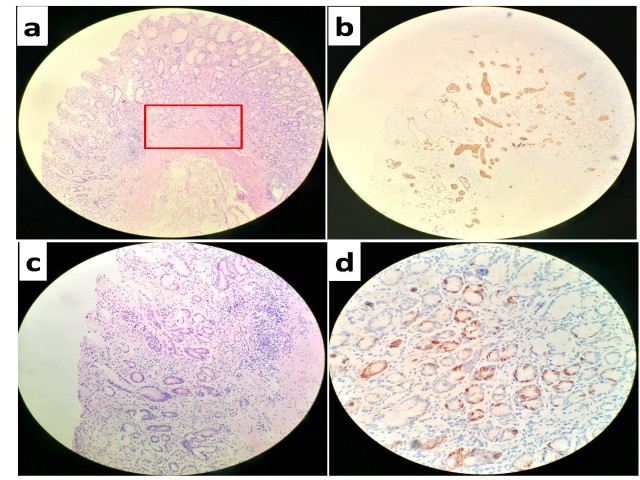
图3. 胃窦处病变。图a,黏膜内见成巢的神经内分泌肿瘤细胞,可侵犯黏膜肌层(红色方框区域);图b,免疫组化显示瘤细胞表达CgA; 图c,胃窦处瘤旁胃黏膜可见淋巴细胞浸润,但无萎缩和肠化;图d,免疫组化标记胃泌素,见较多阳性细胞,提示G细胞增生。
特殊染色:未查见幽门螺杆菌。
病理诊断:
胃底神经内分泌肿瘤(G1),局限于黏膜内;胃窦神经内分泌肿瘤(G1),侵及黏膜肌层;自身免疫性胃炎。综上,考虑为自身免疫性胃炎相关的Ⅰ型胃神经内分泌肿瘤。
讨论:
胃的神经内分泌肿瘤(NET)主要起源于肠嗜铬细胞(ECL细胞)或G细胞(分泌胃泌素),以ECL细胞起源者多见。本例患者的瘤细胞不表达胃泌素,并非G细胞起源,而是ECL细胞起源,且分程度较高(G1)。胃的NET可分为三型:1,Ⅰ型,伴高胃泌素血症和慢性萎缩性胃炎;2,Ⅱ型,伴有Zollinger-Ellison综合征或多发性内分泌肿瘤(此型患者在胃以外其他部位的发生胃泌素瘤导致高胃泌素血症);3,Ⅲ型,为散发型,无明确病因。研究显示,Ⅰ型胃NET最多见,占所有胃NET的70%-80%,分级主要为G1,一般采取内镜下治疗并定期随访,患者预后在三型胃NET中最好;Ⅱ型较Ⅰ型恶性程度偏高,部分为G2,5%-35%病例可发生区域淋巴结转移,预后较Ⅰ型差,但总体预后仍较好,需针对胃以外的胃泌素瘤病灶进行治疗;Ⅲ型恶性程度最高,主要为G2或G3,转移较前二者多见,在三型胃NET中预后最差,需积极手术治疗切除胃原发灶。由于上述三型胃NET在病因、预后和治疗策略方面存在明显差异,因此病理医师必须对其进行准确分类,以指导临床治疗。
Ⅰ型胃NET伴有高胃泌素血症和慢性萎缩性胃炎,可由自身免疫性胃炎(A型胃炎)或幽门螺杆菌相关的慢性胃炎所引发。自身免疫性胃炎主要见于40岁以上女性,机体产生壁细胞抗体或内因子抗体,攻击胃壁细胞,致使胃酸分泌减少,反馈性触发胃窦G细胞增生并产生大量胃泌素,刺激ECL细胞持续过度增生形成肿瘤。临床上,自身免疫性胃炎患者有胃酸分泌减少的表现(PGⅠ和PGⅠ/PGⅡ比值均下降,胃液PH值增高),并伴有高胃泌素血症,同时内因子缺乏以及胃酸减少影响铁吸收,导致贫血(巨细胞性贫血或缺铁性贫血)。
自身免疫性胃炎的病理改变包括:1.胃底、体黏膜出现显著的淋巴细胞浸润,可浸润至固有膜深部至黏膜肌,泌酸腺受破坏导致壁细胞缺失。2. 胃底、体黏膜出现假幽门腺化生,肠上皮化生或胰腺腺泡化生。假幽门腺化生与胃窦的幽门腺一样,可表达Muc6,但化生的假幽门腺无G细胞,不表达胃泌素,这一特点不同于胃窦幽门腺(含有G细胞,可产生胃泌素)。3.上述化生的腺体内可见神经内分泌细胞增生,可以是结节样增生或“线性增生”,后者表现为一个腺管内出现5-6个神经内分泌细胞(ECL细胞),免疫组化可将其显示出来。4.胃窦部腺体G细胞增生,同时无明显炎症或萎缩肠化。
本例患者诊断为Ⅰ型胃NET,且为自身免疫性胃炎相关的NET,依据在于:1.胃底,胃窦见增生的形态一致的小圆形肿瘤细胞,表达神经内分泌的标志物,而不表达胃泌素,提示为ECL细胞起源的胃NET。2.具有上述自身免疫性胃炎的病理学改变。3.临床特征符合自身免疫性胃炎的特点,包括:高胃泌素血症;胃酸分泌减少(PGⅠ和PGⅠ/PGⅡ比值均下降);贫血。此外,自身免疫性胃炎患者可检测到壁细胞或内因子抗体,可作为诊断的特异指标,但并非所有自身免疫性胃炎患者都能检测到上述抗体。本例患者胃底、胃窦黏膜的病理学改变以及临床表现,满足自身免疫性胃炎相关的Ⅰ型胃NET的诊断条件。
本病应与Ⅱ型和Ⅲ型胃NET进行鉴别。Ⅱ型胃NET是由于胃以外脏器的胃泌素瘤(如,胰腺的胃泌素瘤)引起高胃泌素血症刺激ECL细胞持续增生,最终导致NET;由于高胃泌素血症还可促进壁细胞的增生和胃酸分泌,此类患者常有较严重的消化性溃疡。而本例患者泌酸腺呈现萎缩性改变,缺乏胃酸分泌,无消化性溃疡的表现,并且磁共振检查也未见其他脏器的胃泌素瘤病灶,因此可以排除Ⅱ类神经内分泌肿瘤的可能。Ⅲ型神经内分泌肿瘤为散发性,多为单个病灶,无高胃泌素血症,且胃底、胃体处黏膜无自身免疫病性胃炎的病理学改变,因此本病例也可以排除Ⅲ型胃NET的可能。
体会:
1.对胃的NET,病理医师仅作出NET的诊断是不够的,更重要的是对其进一步细致分型,为后续的临床治疗和预后评估提供指导。
2.胃NET的分型诊断不仅需要精细考察胃黏膜的病理学改变,还必须结合患者的临床特征(性别、年龄,有无消化性溃疡和贫血,胃酸分泌减少还是亢进)、实验室检查(胃泌素和胃蛋白酶的测定)和影像学检查结果(胃以外的其他脏器有无占位)进行综合判断。因此,病理医师与临床医师的交流尤为重要。
3.如怀疑为Ⅰ型胃NET,尤其是自身免疫性胃炎相关的NET时,除观察胃底/体处黏膜的病变外,还应对胃窦处黏膜进行充分活检,并辅以免疫组化染色综合判断方能得出准确结论。
















共0条评论