淋巴瘤概述
淋巴瘤是起源于淋巴结及结外淋巴组织的恶性肿瘤的统称,是因异常增生的淋巴样肿瘤细胞取代正常淋巴细胞而形成。主要表现为局部或全身无痛性淋巴结肿大,并可伴有全身各器官、组织的累及,有时会有发热、盗汗、消瘦、瘙痒等全身症状。
根据肿瘤的组织病理学特点,淋巴瘤可分为霍奇金淋巴瘤(Hodgkin’s lymphoma,HL)和非霍奇金淋巴瘤(non—Hodgkin’s lymphoma,NHL)两大类。其中NHL发病率远高于HL。根据肿瘤细胞起源的不同,NHL可分为B细胞、T细胞和NK细胞淋巴瘤三大类,其中B细胞肿瘤占70-85%。
最新的WHO淋巴组织肿瘤分类将淋巴瘤分为80多种亚型【1】。每一亚型诊断最为重要的依据是病理形态学改变,但临床特点、免疫表型和遗传学异常也对淋巴瘤的诊断与分型具有重要意义。
本文将结合最新版NCCN的B细胞淋巴瘤临床实践指南【2】,介绍几种常见B细胞淋巴瘤亚型的临床病理学特点。
弥漫性大B细胞淋巴瘤(Diffuse Large B-Cell Lymphoma,DLBCL)
临床特点
发病率最高的淋巴瘤亚型,约占新诊断NHL的40%,在我国的发病率更高。发病年龄广泛,从儿童至老年人均可患病,但以60~70岁患者居多,男性略多于女性。尽管标准的R-CHOP(利妥昔单抗+环磷酰胺+多柔比星+长春新碱+泼尼松)方案使DLBCL的10年总生存(OS)率提高了20%,但仍有30%患者初始治疗失败。不同的分子亚型、特殊的分子表达及相关信号通路的激活均与DLBCL预后的异质性相关。
病理学诊断
基本要素
对所有切片进行血液病理学检查,其中至少1个蜡块具有肿瘤代表性。如果所获标本不足以确诊,则需要重新活检。通常,单独的细针穿刺(Fine Needle Aspiration,FNA)或粗针活检(Core Needle Biopsy)不宜作为淋巴瘤初始诊断的依据。但在某些情况下,当淋巴结难以切除或切取活检时,联合FNA和粗针活检,并结合适当的鉴别诊断辅助检查(免疫组化、流式细胞术、PCR检测IgH和TCR基因重排、FISH检测主要的染色体易位)可以为诊断提供充分的信息。
确定诊断及GCB和non-GCB免疫分型
石蜡切片推荐应用的免疫组化抗体panel :CD20、 CD3、CD5、CD10、CD45、BCL2、BCL6、Ki-67、IRF-4/MUM1 、MYC。
流式细胞术所选择的细胞表面标志:kappa/lambda、CD45、CD3、CD5、CD19、CD10、CD20。
特定情况下有助于诊断的检查
进一步鉴别淋巴瘤亚型的免疫组化抗体panel:cyclin D1、kappa/lambda、CD138、EBV、ALK、HHV8, SOX11。
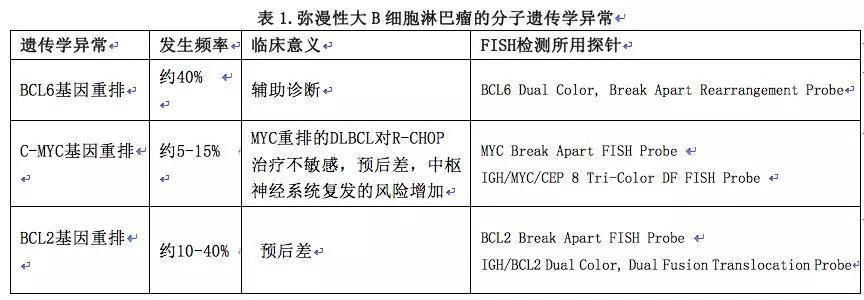
细胞遗传学或FISH检测:MYC、BCL2、BCL6重排。(表1.)
滤泡性淋巴瘤(Follicular Lymphoma,FL)
临床特点
约占NHL的22-35%,仅次于DLBCL。FL 的遗传标记是 t(14;18)(q32;q21) 异位,导致 bcl2 蛋白持续过量表达,损害了正常生发中心凋亡功能。临床上,FL 通常是惰性,除了病情进展,多数患者没有临床症状。事实上,绝大部分患者是在 III 期和 IV 期的进展期诊断。FL是对化疗和放疗最有效的恶性肿瘤之一。
病理学诊断
基本要素
对所有切片进行血液病理学检查,其中至少1个蜡块具有肿瘤代表性。如果所获标本不足以确诊,则需重新活检。通常,单独的细针穿刺(Fine Needle Aspiration,FNA)或粗针活检(Core Needle Biopsy)不宜作为淋巴瘤初始诊断的依据。但在某些情况下,当淋巴结难以切除或切取活检时,联合FNA和粗针活检,并结合适当的鉴别诊断辅助检查(免疫组化、流式细胞术、PCR检测IgH和TCR基因重排、FISH检测主要的染色体易位)可以为诊断提供充分的信息。FNA 不能作为组织学分级的依据。
确定诊断的免疫分型
石蜡切片推荐应用的免疫组化抗体panel:CD20、CD3、CD5、CD10、CD21、CD23、BCL2、BCL6
流式细胞术所选择的细胞表面标志:kappa/lambda、CD19、CD20、CD5, CD23, CD10
特定情况下有助于诊断的检查
分子遗传学检测:抗原受体基因重排,BCL2重排。
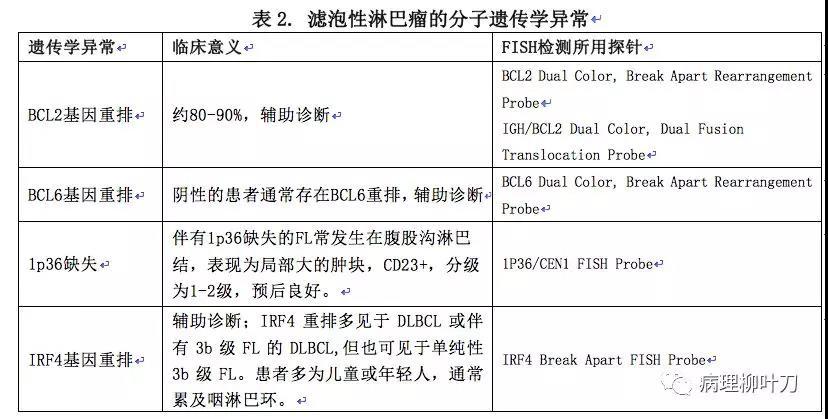
细胞遗传学或FISH检测:t(14;18), BCL6, 1p36, IRF4/MUM1 重排。(表2.)
免疫组化抗体panel: Ki-67,IRF4/MUM1(3级FL),cyclin D1
伯基特淋巴瘤(Burkitt Lymphoma,BL)
临床特点
约占NHL的2.5%。是可能来源于滤泡生发中心细胞的高度恶性的B细胞肿瘤,在我国多发于儿童和青年人,部位以上颌骨或下颚骨(非洲患者),腹腔器官(北美患者)和中枢神经系统为主。临床治疗不论分期应以化疗为主,辅以放疗。临床诊断近年来探索区分介于弥漫大B细胞淋巴瘤和伯基特淋巴瘤之间而无法区分的灰区淋巴瘤,主要借助其免疫表型和分子异常类型确诊。
病理学诊断
基本要素
对所有切片进行血液病理学检查,其中至少1个蜡块具有肿瘤代表性。如果所获标本不足以确诊,则需重新活检。通常,单独的细针穿刺(Fine Needle Aspiration,FNA)或粗针活检(Core Needle Biopsy)不宜作为淋巴瘤初始诊断的依据。但在某些情况下,当淋巴结难以切除或切取活检时,联合FNA和粗针活检,并结合适当的鉴别诊断辅助检查(免疫组化、流式细胞术、PCR检测IgH和TCR基因重排、FISH检测主要的染色体易位)可以为诊断提供充分的信息。
确定诊断的免疫分型
石蜡切片推荐应用的免疫组化抗体panel:CD45(LCA)、CD20、CD3、CD10、Ki-67、BCL2、BCL6、TdT
流式细胞术所选择的细胞表面标志:kappa/lambda、CD45、CD20、CD3、CD5、CD19、CD10、TdT
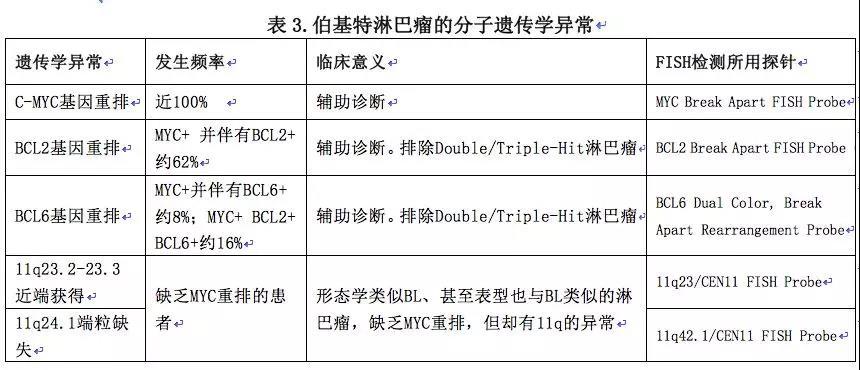
细胞遗传学或FISH检测:t(8;14)或其变异型;MYC重排。(表3.)
特定情况下有助于诊断的检查
FISH:BCL2,BCL6重排
原位杂交检测EBER
结外边缘区淋巴瘤 ,胃MALT淋巴瘤(Extranodal Marginal Zone B-Cell Lymphoma, Gastric MALT Lymphoma)
临床特点
约占NHL的5%。MALT淋巴瘤是一类起源于粘膜相关淋巴组织的结外B细胞性非霍奇金淋巴瘤,常见发病部位包括胃肠道、肺、甲状腺、眼眶等,其中50%左右发生在胃肠道。
病理学诊断
基本要素
对所有切片进行血液病理学检查,其中至少1个蜡块具有肿瘤代表性。如果所获标本不足以确诊,则需要重新活检。
胃MALT淋巴瘤需要内镜下活检,FNA不足以诊断。
确定诊断的免疫分型
石蜡切片推荐应用的免疫组化抗体panel:CD20, CD3, CD5, CD10, BCL2, kappa/ lambda, CD21 or CD23, cyclin D1,BCL6
流式细胞术所选择的细胞表面标志:kappa/lambda、CD19、CD20、CD5、CD23、CD10
幽门螺杆菌染色,如阳性,须通过PCR或FISH检测t(11;18)
特定情况下有助于诊断的检查
分子遗传学分析检测:抗原受体基因重排;MYD88 突变(假如出现浆细胞分化,要与WM鉴别 )
细胞遗传学或FISH检测: t(1;14),t(3;14),t(11;14),t(11;18),t(14;18).(表4.)

套细胞淋巴瘤 (Mantle Cell Lymphoma,MCL)
临床特点
约占NHL的6%。MCL的恶性程度高、预后较差,兼有惰性淋巴瘤和侵袭性淋巴瘤的最差特征。
病理学诊断
基本要素
对所有切片进行血液病理学检查,其中至少1个蜡块具有肿瘤代表性。如果所获标本不足以确诊,则需重新活检。通常,单独的细针穿刺(Fine Needle Aspiration,FNA)或粗针活检(Core Needle Biopsy)不宜作为淋巴瘤初始诊断的依据。但在某些情况下,当淋巴结难以切除或切取活检时,联合FNA和粗针活检,并结合适当的鉴别诊断辅助检查(免疫组化、流式细胞术、PCR检测IgH和TCR基因重排、FISH检测主要的染色体易位)可以为诊断提供充分的信息。
确定诊断的免疫分型
石蜡切片推荐应用的免疫组化抗体panel:CD20、CD3、CD5、cyclin D1、 CD10、 CD21、CD23、BCL2、BCL6、ki-67
流式细胞术所选择的细胞表面标志:kappa/lambda、CD19、CD20、CD5, CD23, CD10
特定情况下有助于诊断的检查
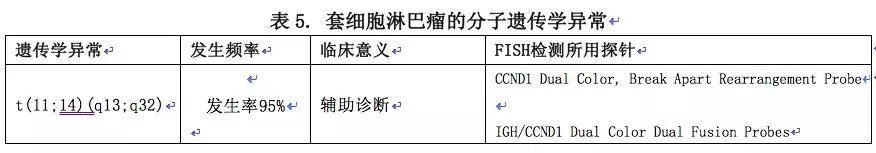
细胞遗传学或FISH检测:t (11;14);t (14;18);CLL相关遗传学检查。(表5.)
流式细胞术所选择的细胞表面标志:CD200
参考文献
[1].Swerdlow, S.H.,Campo,E., Pileri SA. ,et al., The 2016 revision of the World Health Organization classification of lymphoid neoplasms. Blood, 2016. 127(20): p. 2375-90.
[2]. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®) . B-cell Lymphomas.Version 7.2017.
文章仅供公益交流学习,不代表本网站立场,欢迎提供素材,投稿、转载请联系微信1392271329


















共0条评论