[导读] 执笔人单位:
复旦大学附属肿瘤医院病理科复旦大学上海医学院(王坚、朱雄增);
北京大学医学部病理学系(郑杰);
中国医学科学院北京协和医学院北京协和医院病理科(陈杰);
广东省人民医院病理科(刘艳辉)
为进一步在全国推动胃肠道间质瘤(gastrointestinal stromal tumor,GIST)的规范化诊断和治疗,建立包括外科、影像科、病理科、消化内科和肿瘤内科等在内的多学科协作模式,中国抗癌协会临床肿瘤学协作专业委员会(CSCO)胃肠道间质瘤专家委员会组织各学科专家对中国GIST病理诊断共识(2011年版)的修订工作进行了多次讨论,根据最新的临床研究和基础研究等循证医学证据对共识进行了修改和补充,经广泛征求意见后,形成中国GIST诊断治疗共识(2013年版),并在《临床肿瘤学杂志》上正式发表。本解读就该共识的病理诊断部分作一简要介绍,并对其中的部分内容予以补充和说明。
一、关于GIST的定义
GIST是胃肠道最常见的间叶源性肿瘤,临床可以表现为从良性到恶性,免疫组织化学检测通常表达CD117和DOG1,显示卡哈尔细胞(Cajalcell)分化,大多数病例具有KIT或PDGFRA活化突变,少数病例涉及其他分子异常。
二、对标本的要求
与2011年版共识相同,主要是提醒和敦促外科医师在手术标本的处理上能更合乎规范。
三、关于GIST的病理诊断
1.基本诊断:从事GIST病理诊断的医师应熟悉GIST的基本形态,并了解GIST的一些特殊形态。GIST的基本病理组织学形态包括梭形细胞型(70%)、上皮样细胞型(20%)和梭形细胞-上皮样细胞混合型(10%,图1~3),并可有多种排列结构。即便为同一病理组织学亚型的GIST,形态也可有很大的差异。除经典形态外,GIST还可有一些特殊形态,包括少数病例还可见多形性细胞,尤其在上皮样细胞型GIST中(图4)。除出血、囊性变和坏死外,间质可呈硬化性,可有钙化,特别是小GIST(图5);偶可呈黏液样(图6)等。此外,发生于小肠的GIST常可见嗜伊红色的丝团样纤维小结(Skeinoid fiber),对诊断也有一定的提示性意义。

2.靶向治疗后的GIST:2013年版共识增加了分子靶向治疗后GIST的形态学改变:肿瘤可以发生坏死和/或囊性变(图7);在部分病例中细胞密度明显降低,瘤细胞成分稀疏,间质广泛胶原化(图8),可伴有多少不等的炎性细胞浸润和组织细胞吸收反应(图9)。少数病例经靶向治疗后在免疫表型和镜下形态上可有所改变,包括CD117失表达,可发生横纹肌肉瘤样分化或去分化等。临床上对分子靶向治疗效果的评判主要根据影像学(改良Choi标准)。近年来,经分子靶向治疗后再经手术切除的GIST标本也逐渐增多,可从组织学上对疗效协助评判。根据坏死和变性区域在整个肿瘤内所占的比例分为:(1)轻微效应,<10%;(2)低度效应,10%-50%;(3)中度效应,51%-90%;(4)高度效应,>90%。
3.GIST的免疫组织化学:多组大宗病例报道显示CD117和DOG1在GIST中的表达具有高度一致性,有鉴于此,2013版共识推荐联合采用CD117和DOG1,并建议加用阳性对照。需注意的是:(1)少数非GIST肿瘤也可表达CD117和/或DOG1,如直肠肛管恶性黑色素瘤和腹膜后平滑肌瘤等,应联合采用其他标志物,如S-100蛋白、HMB45、α-平滑肌肌动蛋白(SMA)和结蛋白等,或采用分子检测加以鉴别;(2)平滑肌肿瘤中可混杂多少不等CD117阳性的卡哈尔细胞和/或肥大细胞,可被误诊为GIST。CD34与CD117和DOG1配伍使用时在GIST的诊断和鉴别诊断中仍具有较高的价值,但其阳性率低于CD117和DOG1。与胃肠胰神经内分泌肿瘤不同的是,Ki-67阳性指数在GIST中尚无明确的临界值可用于评估危险度,有待于更多病例的统计分析。此外,免疫组织化学检测琥珀酸脱氢酶(succinate dehydrogenase,SDH)B有助于识别SDH缺陷型GIST(SDH-deficient GIST)。SDH缺陷型GIST失表达SDHB。新近报道显示,在SDHB失表达的病例中,SDHA失表达约占28%,与SDHA胚系突变相关。
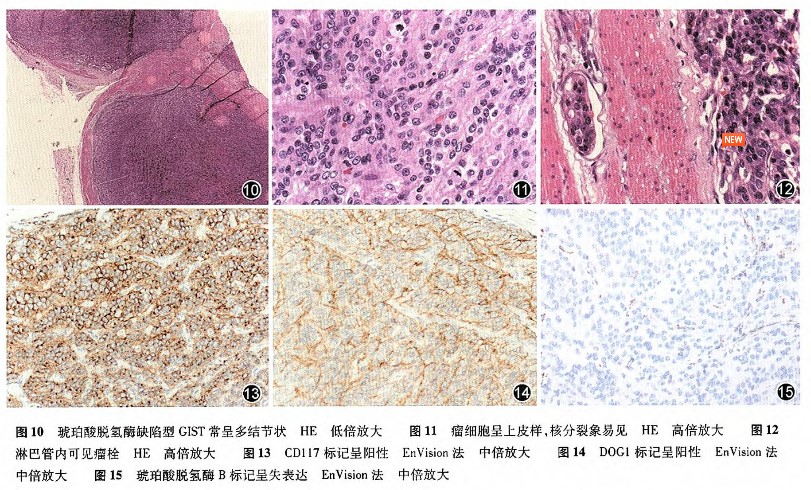
4.关于SDH缺陷型GIST:该型GIST几乎均发生于胃,约占GIST的5.0%~7.5%。临床上可以表现为Carney三联征(GIST、副神经节瘤和肺软骨瘤,多发生于女性儿童和青年人)或Carney.Stratakis综合征(一种具有不完全显现率的常染色体显性遗传性疾病,表现为家族性胃GIST和副神经节瘤),也可为散发性。Carney三联征中只需存在任何两种成分即可做出诊断,但因肿瘤发生的异时性而不易被诊断。组织学上SDH缺陷型GIST常呈多结节状生长(图10),多为上皮样型(图11),也可为混合型,常见淋巴管侵犯(图12)和/或区域淋巴结转移。免疫组织化学标记可表达CD117和DOG1(图13,14),但SDHB呈失表达(图15)。分子检测无KIT或PDGFRA基因突变,约半数病例显示为SDH亚单位之一(SDHA、SDHB、SDHC或SDHD)功能丧失性胚系突变,其中30%为SDHA突变,20%为SDHB、SDHC或SDHD突变,另一半数病例可能为SDH复合体的表观基因沉默,存在广泛的基因组甲基化,大多为高甲基化。SDH缺陷型GIST的发病机制尚未完全明了,可能与SDH缺失导致琥珀酸累积,从而触发低氧诱导因子-1α(HIF1α)介导的假缺氧信号通路相关。SDH缺陷型GIST还存在胰岛素样生长因子1(IGF1)信号的活化,可高表达胰岛素样生长因子受体1R(IGF1R)。与经典型GIST不同的是,SDH缺陷型GIST的预后较难预测。依据肿瘤大小和核分裂象不能预测肿瘤的生物学行为,肿瘤小和核分裂象少的可发生肝转移,肿瘤大和核分裂象多的却可不转移。另一特点是发生转移的间隔期较长,需长期随访。一些病例即使发生转移,患者也可生存较长时间。针对SDH缺陷型GIST的治疗以手术切除和清扫区域淋巴结为主。SDH缺陷型GIST对TKI抑制剂(甲磺酸伊马替尼和舒尼替尼)反应不佳。TKI抑制剂多用于病情进展且不能通过手术完整切除者。其他一些可能具有潜在疗效的新激酶抑制剂包括瑞格非尼、尼洛替尼和索拉非尼。IGF1R抑制剂Linsitinib(OSI-906)和热休克蛋白抑制剂等尚处于临床实验阶段。
 5.关于GIST的病理诊断思路:(1)对于组织学形态符合典型GIST且CD117和DOG1阳性的病例,可做出GIST的诊断。需注意的是,少数病例也可为弱阳性表达CD117,特别是有PDGFRA基因突变的上皮样型GIST。此外,如CD117和DOG1标记均为阳性,但分子检测无KIT基因或PDGFRA基因突变时需考虑是否有野生型GIST的可能性;(2)对于组织学形态考虑为GIST,但是CD117(-)、DOG1(+)或CD117(+)、DOG1(-)的病例,在排除其他类型肿瘤后可做出GIST的诊断。因这部分病例在GIST中的所占比例较少(约5%左右),建议加做分子检测,以确定是否存在KIT或PDGFRA基因突变。例如CD117(-)、DOG1(+)的病例组织学上多为上皮样型,分子检测常显示PDGRFA基因突变,并可为D842V(耐药型)。如果经过分子检测也无KIT或PDGFRA基因突变,建议请GIST病理学专家讨论后做出最终诊断;(3)对于组织学形态符合典型GIST,但CD117和DOG1均为阴性的病例,需要进行KIT或PDGFRA基因检测,如有KIT或PDGFRA基因突变,可诊断为GIST,如无KIT或PDGFRA基因突变,在诊断为野生型GIST之前需要考虑是否有非GIST的可能性,必要时再请GIST病理学专家讨论后做出最终诊断。GIST的病理诊断思路参见图16。
5.关于GIST的病理诊断思路:(1)对于组织学形态符合典型GIST且CD117和DOG1阳性的病例,可做出GIST的诊断。需注意的是,少数病例也可为弱阳性表达CD117,特别是有PDGFRA基因突变的上皮样型GIST。此外,如CD117和DOG1标记均为阳性,但分子检测无KIT基因或PDGFRA基因突变时需考虑是否有野生型GIST的可能性;(2)对于组织学形态考虑为GIST,但是CD117(-)、DOG1(+)或CD117(+)、DOG1(-)的病例,在排除其他类型肿瘤后可做出GIST的诊断。因这部分病例在GIST中的所占比例较少(约5%左右),建议加做分子检测,以确定是否存在KIT或PDGFRA基因突变。例如CD117(-)、DOG1(+)的病例组织学上多为上皮样型,分子检测常显示PDGRFA基因突变,并可为D842V(耐药型)。如果经过分子检测也无KIT或PDGFRA基因突变,建议请GIST病理学专家讨论后做出最终诊断;(3)对于组织学形态符合典型GIST,但CD117和DOG1均为阴性的病例,需要进行KIT或PDGFRA基因检测,如有KIT或PDGFRA基因突变,可诊断为GIST,如无KIT或PDGFRA基因突变,在诊断为野生型GIST之前需要考虑是否有非GIST的可能性,必要时再请GIST病理学专家讨论后做出最终诊断。GIST的病理诊断思路参见图16。
6.关于GIST的鉴别诊断:从事GIST病理诊断的病理医师不仅要熟悉GIST的各种形态学表现,也要了解各种易被误诊为GIST的肿瘤,包括:(1)平滑肌肿瘤,包括食管和贲门平滑肌瘤、盆腹腔平滑肌瘤以及发生于胃肠道、肠系膜和腹膜后等处的平滑肌肉瘤;(2)炎性纤维性息肉,可表达CD34,分子检测也可有PDGFRA基因突变;(3)肠系膜和盆腹腔内纤维瘤病;(4)消化道型神经鞘瘤;(5)直肠和肛管恶性黑色素瘤;(6)其他,包括炎性肌纤维母细胞瘤、胃肠道透明细胞肉瘤(胃肠道神经外胚层瘤)、胃肠道血管周上皮细胞肿瘤、胃肠道滑膜肉瘤、肠系膜树突细胞肿瘤/肉瘤、胃肠道丛状纤维黏液瘤、血管球瘤和发生于腹腔内的精原细胞瘤等。
7.关于野生型GIST的诊断:野生型GIST指组织学形态和免疫组织化学标记均符合GIST,但分子检测无KIT和PDGFRA基因突变。目前已知的野生型GIST包括以下几种情形:(1)SDH缺陷型GIST,包括伴有Carney三联征或Carney-Stratakis综合征,以及一些散发性病例;(2)非SDH缺陷型GIST,包括NF1相关型和BRAF基因突变(外显子15V600E突变)等。
8.关于GIST的分子检测:2013年版共识认为分子检测应该在符合资质的实验室进行。需要指出的是,分子检测不仅可用于指导临床治疗和预测分子靶向治疗药物的疗效,还有助于一些疑难病例的诊断和鉴别诊断。对病理诊断明确且评估为中一高危(NIH2008年改良版)或预后分组为3以上(WHO)的GIST,均应加做分子检测。尚无条件开展分子检测的单位,建议在病理报告的备注中注明到有条件的单位加做分子检测,进一步明确病理诊断,并确定具体突变类型以指导临床治疗。与免疫组织化学标记结果相似,分子检测结果也应作为病理报告的一部分。存在以下情况时应进行分子检测:(1)原发可切除GIST术后评估为中-高危或预后分组为3以上,拟进行分子靶向治疗;(2)术前拟进行分子靶向治疗;(3)所有初次诊断的复发和转移性GIST,拟进行分子靶向治疗;(4)继发性耐药需要重新检测;(5)经综合性治疗后发生复发或转移的GIST需要重新检测;(6)疑难病例或CD117与DOG1表达不一致者;(7)鉴别KIT或PDGFRA基因突变以外的野生型GIST;(8)鉴别同时性和异时性、多发性原发GIST。检测基因突变的位点,至少应包括KIT基因的第9、11、13和17号外显子以及PDGFRA基因的第12和18号外显子,可酌情增加检测PDGFRA的第14号外显子。由于大多数GIST(65%~85%)的基因突变发生在KIT基因第11或9号外显子,因此可以优先检测这2个外显子。对于继发耐药的患者,宜增加检测KIT基因的第14和18号外显子。
9.小GIST和微小GIST的概念:直径≤2cm的GIST统称为小GIST,2013版共识则进一步将直径≤1cm的GIST定义为微小GIST(microGIST),其中的大多数病例为偶然发现。尽管大多数小GIST或微小GIST病例在临床上呈良性或惰性经过,但确有极少数病例显示侵袭性行为,尤其是核分裂象计数>5/50HPF或>10/50HPF者。
四、关于GIST的危险度评估
GIST的危险度评估适用于原发完全切除的GIST。以下几种情形病理医师可不作危险度评估:(1)各类活检标本,包括细针穿刺活检、芯针穿刺活检和内镜活检等;(2)已发生复发和/或转移的GIST;(3)经过分子靶向治疗的GIST。
目前对GIST危险度的评估系统主要有两种,其一为NIH2008年改良版,其二为美国武警部队病理学研究所(AFIP)、2010年版《WHO消化系统肿瘤分类》和2013年版《WHO软组织肿瘤分类》中采用的预后分组,从事GIST诊治的医师均应熟悉。
需要指出的是:(1)GIST的危险度评估或预后分组与GIST的良恶性判断是两个问题,病理科医师可根据相关的参数评估危险度或预后分组,但不宜对GIST做出具体性质上的诊断,除非肿瘤已发生腹腔内播散或肝脏转移等情形;(2)NIH2008年改良版危险度评估和WHO预后分组存在不一致的情形,例如胃或小肠GIST,平均直径为9cm,且核分裂象≤5/50HPF者,NIH2008年改良版分别被评估为中危(胃)和高危(小肠),WHO则将其归入3a组,即为良性,但患者发生疾病进展的百分率在胃为3.6%,小肠为24.0%;(3)临床和病理对具体病例的危险度评估或预后分组也会有不一致的情形,主治医师应综合临床、影像和病理等各方面的资料进行分析和判断。
根据我国的病理现状,以及临床、病理和影像等多学科之间的协作,2013年版共识仍推荐采用NIH2008年改良版,WHO分类中的预后分组可作为参考。NIH2008年改良版中原有的小错误在2013年版共识中得到了纠正,但仍有不足之处,如无法对直径≤2cm、核分裂象(6-10)/50HPF、发生于胃者进行评估,本解读根据GIST病理诊断共识专家组讨论意见,对2013年版共识再次进行了小幅的修订,参见表1。

肿瘤大小的测量包括术前影像学、术中和术后对标本的直接测量,各单位应视具体情况而定。目前,大多数病例均为对固定后标本的直接测量,可能会有一定的误差。有条件的单位,应对离体的标本在新鲜状态下及时测量。对一些特殊情况,如囊性变、坏死和碎瘤组织,临床和病理医师均应注意参考术前或靶向治疗前影像学。
核分裂象计数时应计数分裂象活跃的区域,至少计数50个高倍镜视野。建议对核分裂进行如实计数,尤其是>10/50HPF者。
多中心性GIST常与NF1相关,多发生于小肠,CD117和DOG1阳性,但无KIT或PDGFRA基因突变,SDHB阳性,IGF1R阴性。对于同一部位同时有多个病灶,或不同部位同时有多个原发病灶,应将各种参数如实列出,供临床医师参考。例如,胃和小肠的双原发GIST,应分别注明各自的肿瘤大小和核分裂象,均行免疫组织化学标记和分子检测。
五、关于GIST的规范化病理诊断报告
在病理报告中必须准确注明原发部位、肿瘤大小和核分裂象数,肿瘤有无破裂则需要根据临床和其他辅助检查。病理报告中应附有免疫组织化学和分子检测结果,后者可另附(如请外单位检测)。GIST病理报告的推荐格式参见表2。

2013年中国胃肠道间质瘤病理诊断共识专家组成员(姓名按汉语拼音字母顺序排列):
曹登峰(中国医学科学院北京协和医学院肿瘤医院)、
陈 杰(中国医学科学院北京协和医学院北京协和医院)、
陈丽荣(浙江大学医学院附属第二医院)、
侯英勇(复旦大学附属中山医院)、
李向红(北京大学肿瘤医院)、
李 奕(辽宁省肿瘤医院)、
李增山(第四军医大学西京医院)、
刘艳辉(广东省人民医院)、
柳 萍(北京大学第一医院)、
王 坚(复旦大学附属肿瘤医院复旦大学上海医学院)、
薛 玲(中山大学附属第一医院)、
张红英(四川大学华西医院)、
张 声(福建医科大学附属第一医院)、
郑 杰(北京大学医学部)、
周晓军(南京军区南京总医院)、
朱雄增(复旦大学附属肿瘤医院复旦大学上海医学院)
参考文献(略)

















共0条评论