患者,男性,30岁,山东人,汉族,教师。
第一次住院(2007年12月07日入院)。
主诉:泡沫尿2月余,水肿1月。
现病史:患者2个多月前上呼吸道感染后出现尿中泡沫增多,无肉眼血尿,尿量不少,未予重视,1个多月前出现眼睑水肿,腰酸乏力,遂至外院就诊,查尿蛋白++,隐血+++,RBC 满视野,异形红细胞为主,24小时尿蛋白定量6.88g,血清肌酐(Scr)144.8μmol/L,B 超双肾形态大小正常,拟诊“慢性肾炎,肾功能不全”,予“前列地尔、双嘧达莫、虫草”治疗,复查尿常规及肾功能无明显改善。半个月前在外院给予激素(泼尼松50mg,每日一次)治疗,一周后复查Scr 130μmol/L,尿蛋白++,隐血+++。今为进一步诊治转入我院。发病以来患者无关节痛、皮疹、口腔溃疡,无皮肤紫癜,无眩晕、耳鸣、听力下降,无咳嗽、发热、咯血,胃纳及睡眠尚可,大便正常,尿量约1500ml/d,体重无明显变化。
既往史:对“青霉素及乙醇”过敏,家族史无特殊。
体格检查:体温37℃,脉搏80次/分,呼吸18次/分,血压130/70mmHg。神清,全身浅表淋巴结无肿大。双眼睑轻度水肿,结膜无苍白,扁桃体无肿大。两肺呼吸音清,未闻及干湿性啰音。心律齐,各瓣膜听诊区未闻及明显病理性杂音。腹平软,无压痛,肝脾肋下未及,双肾区无明显叩痛,双下肢无水肿,双侧Babinski征阴性。
辅助检查:血常规:白细胞(WBC)10.62 ×10 9/L,血红蛋白(HGB)103g/L,血小板(PLT)216 ×10 9/L;血沉(ESR)40mm/h;尿常规:潜血(BLD)+++,蛋白(PRO)+,红细胞997个/μl,80%为异形红细胞,白细胞49个/μl;尿蛋白定量3.42g/24h;生化系列:丙氨酸氨基转移酶(ALT)48U/L,白蛋白(ALB)33.7g/L,球蛋白(GLB)19.6g/L,尿素(UREA)10.1mmol/L,肌酐137μmol/L。
免疫学检查:B 因子(PFB)23.7mg/dl(19~50mg/dl);免疫球蛋白G(IgG)6.35g/L,免疫球蛋白A(IgA)1.57g/L,免疫球蛋白M(Ig M)0.8g/L,补体C3 为1.11g/L(0.79~1.52g/L),补体C4为0.33g/L(0.16~0.38g/L);抗中性粒细胞胞浆抗体(ANCA)阴性;抗核抗体(ANA)阴性,抗双链DNA(ds‐DNA)抗体阴性;抗GBM 抗体阴性[酶联免疫吸附法(ELISA)]。乙肝二对半及丙肝、梅毒、HI V 抗体阴性。
胸部CT:未见异常;双肾B 超:右肾130mm×50mm,左肾128mm×53mm,双肾皮质回声增强。
院前分析
患者青年男性,因蛋白尿、血尿合并肾功能损害入院。患者既往无肾脏病史,发病前两年曾体检,未见蛋白尿、血尿及肾功能受损,此次外院查B 超示肾脏大小正常,入院后复查B 超提示双肾体积稍增大,提示急性肾衰竭(表28‐1)。患者无肾前性及肾后性病因及相应临床表现,考虑急性肾衰竭为肾性因素引起。患者尿蛋白量大,血尿为肾小球来源血尿,提示肾脏病变集中在肾小球疾病上。应进一步考虑包括急进性肾炎、重症感染后急性肾小球肾炎、IgA 肾病、原发性小血管炎等。目前临床无法确诊,应尽快行肾活检,病理明确诊断。
肾脏病理:光镜(图28‐1):取材较好,14 肾小球,毛细血管襻明显增厚,伴系膜区基质增多,个别节段有系膜细胞轻度增生,其中约一半肾小球有大小不等细胞性新月体形成,肾小管部分有蛋白。
(表28‐1 引自王海燕.肾脏病学.第3版.2008,871[1])管型,少量肾小管灶性坏死、萎缩,伴有周围间质中等量炎症细胞灶性分布,肾血管未见明显病变。
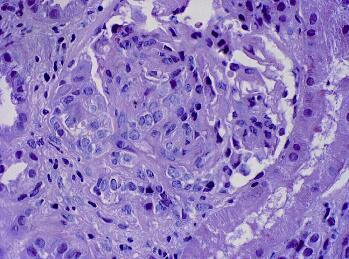
图28‐1 肾脏病理光镜表现HE×400
直接免疫荧光(图28‐2):IgG(+++)和C3(++)为主,呈线样沿毛细血管袢分布,IgA 弱阳性(±),IgM 阳性(+),Fib 阳性(+),C4 阴性,C1q 阴性。
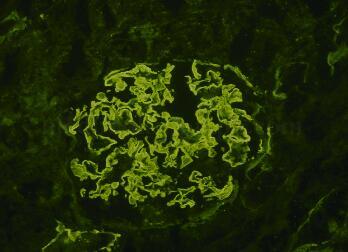
图28‐2 肾脏病理免疫荧光IgG×400
电镜:仅见肾小球一个血管袢,未见明显异常,肾间质内大量淋巴细胞浸润。
治疗经过
患者入院后第四天行急诊肾活检,病理提示抗基底膜型新月体性肾炎。但血清抗GBM 抗体阴性。于第十天开始给予甲泼尼龙500mg 静滴(隔日使用,连续三次)冲击一疗程,三次后再次给予甲泼尼龙320mg 静脉滴注,连续三天。其后给予泼尼松口服,每次50mg,每天一次。一周后加用环磷酰胺(CTX)0.8g 静脉滴注,治疗后水肿消退。入院后一周,患者出现发热、体温37.5℃左右,伴有咳嗽咳痰,为白色黏痰,痰中带少量血丝,无胸闷气急,无胸痛,查胸部CT 未见异常,抗炎治疗一周后咳嗽咳痰基本消失,体温正常。甲泼尼龙及CTX 治疗后出现药物性肝损害,给予保肝、对症治疗后好转。因患者要求,于2008年1月9日出院,出院时血清肌酐199μmol/L,尿隐血+++,尿蛋白+,尿红细胞170个/μl。
出院诊断:①抗GBM 病,Goodpasture 病,急进性肾炎综合征,Ⅰ型新月体性肾炎,急性肾衰竭;②肺出血。
讨论
此患者为青年男性,有吸烟史,以血尿、蛋白尿起病,有急性肾衰竭,但进展较缓,同时出现与肾功能不相匹配的贫血。入院后及时进行了急诊肾活检,发现有大量(50%)新月体形成,且新月体处于同一时期,均为细胞性新月体,直接免疫荧光可见IgG 及C3 沿毛细血管袢线样沉积,为典型的抗基底膜型肾炎的病理表现。入院后在肺部感染的诱因下又出现肺出血,表现为痰中带血。因此,该患者抗肾小球基底膜病,Goodpasture 病诊断明确。
抗肾小球基底膜(GBM)病是指循环中的抗GBM 抗体在脏器中沉积所引起的一组自身免疫性疾病。主要的受累脏器是肺脏和肾脏。病变局限在肾脏时称为抗GBM 肾炎;肺肾同时受累时表现为肺出血‐肾炎综合征(Goodpasture’s syndrome),可诊断 Goodpasture 病;也可表现为肺脏单独受累,此时常易误诊。该病确诊依赖外周血中可以检测到抗GBM 抗体,和(或)肾活检肾小球毛细血管袢上见到IgG 和C3 呈线样沉积[1]。本例患者虽然多次检测血清中抗GBM 抗体均阴性,但我们及时进行了肾活检病理检查,使患者得到了及时的诊断。
本例患者有以下几个特殊之处:①抗GBM 肾炎大多表现为急进性肾炎,肾功能迅速恶化,短期内(数周或数月)达到尿毒症,而该患者起病较缓慢,虽有蛋白尿、血尿等急性肾炎综合征的表现,但无典型的少尿、无尿及肾功能进行性恶化,一个月之内,血肌酐水平基本稳定。这种情况的发生,可能和疾病本身有关,临床表现为缓进型。此外,激素的使用可能也部分延缓了肾功能恶化的进程。②患者多次查血清抗GBM 抗体阴性,与肾脏病理结果不相符合。是诊断有误还是检测技术的问题?分别取血清送上海长征医院及北京大学第一医院,结果均提示抗GBM 抗体为阴性。因此,患者抗基底膜型肾炎的诊断仍值得进一步商酌。抗GBM病的首选治疗为血浆置换,临床上可以根据血清中抗体的情况监测疗效和决定是否停止治疗。由于多次检查外周血抗GBM 抗体(ELISA 法)为阴性,因此该患者未接受血浆置换治疗,仅给予激素冲击和环磷酰胺治疗后出院,门诊随诊。
第二次住院
出院后门诊治疗半年,患者一直口服泼尼松,逐渐减量至15mg,每天一次,每月定期给予静脉CTX(0.6~0.8g/月)治疗。同时给予血管紧张素受体拮抗剂(ARB)类药物减少尿蛋白。门诊定期复查,蛋白尿逐渐减至1.6g/24h,但血尿缓解不明显,血清肌酐(Scr)波动在100~200μmol/L 之间。为求进一步诊治于2008年7月24日收住北京大学第一医院肾内科。
体格检查:体温36.6℃,脉搏78次/分,呼吸16次/分,血压115/60mmHg。满月脸,双肺呼吸音清,未闻及干湿啰音。心律齐,未闻及杂音。腹软,无压痛,肝脾肋下未及,双下肢不肿。
辅助检查:血常规:WBC 8﹒31 ×10 9/L,HGB 103g/L,PLT 248 ×10 9/L;尿液检查:PRO ++,RBC 满视野,30%~40%正常,60%~70%变形;24小时尿蛋白定量:2.04g;尿蛋白电泳:小分子蛋白17.9%,白蛋白72.9%,大分子蛋白9.2%;生化系列:ALB 40g/L,血清肌酐(Scr)114μmol/L,尿素氮8.8mmol/L;内生肌酐清除率(Ccr)71.25ml/min,估计肾小球滤过率(eGFR)69.56ml/(min •1.73m 2);血清蛋白电泳:ALB52.5%,α1球蛋白3.6%,α2球蛋白12.2%,β球蛋白10.3%,γ球蛋白21.4%;血清免疫固定电泳:血中免疫球蛋白为多克隆性,未见单克隆免疫球蛋白区带;免疫学检查:血沉60mm/h,C 反应蛋白4.81mg/L;IgG 13﹒5g/L,IgA 1﹒89g/L,Ig M 1﹒28g/L,C3 1﹒3g/L,C4 0﹒35g/L;ANCA:间接免疫荧光法(IIF)阴性,ELISA 法MPO‐ANCA 阴性,PR3‐ANCA 阴性;血清抗GBM 抗体(ELISA 法)阴性。
胸片:两肺纹理增多;胸部CT:心包积液,纵隔未见明显肿大淋巴结,双侧后壁胸膜轻度肥厚;超声心动图:左房饱满,二尖瓣轻度反流,少量心包积液;腹部B 超:左肾13.1c m×5.8c m×4.7cm,肾实质厚度1.6cm,右肾13.4cm×5.5cm×4.3c m,肾实质厚度1.5cm,轮廓不清,实质回声增强。肝胆胰脾正常。
院前分析
患者入院后考虑抗GBM 病诊断明确,但是①血清学抗GBM抗体呈阴性,与肾脏病理表现不符;②病程进展较缓,属少见类型;③虽然经过强化免疫抑制治疗,但肾功能恢复不满意,仍有明显血尿、蛋白尿等肾脏受损的证据,需要尽快重复肾活检明确病理类型,指导治疗、判断预后。
重复肾活检:光镜(图28‐3):取材好,可见19个肾小球,肾小球系膜细胞和基质轻度弥漫性增生,局灶节段性中度加重伴嗜复红蛋白沉积,其中一个节段性纤维素样坏死,2个细胞性、1个纤维性、3个小细胞性、5个小细胞纤维性新月体形成。肾小管上皮空泡及颗粒变性,多灶性及片状萎缩。肾间质多灶性及片状淋巴和单核细胞浸润伴肾小管炎,小动脉管壁增厚。
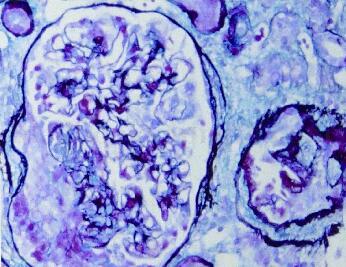
图28‐3 肾脏病理光镜表现PASM+Masson ×400
免疫荧光(图28‐4):IgG +++,IgA-,IgM+,C3 ++,C1q -,FRA-,Alb-;IgG 毛细血管壁线样沉积,IgM 系膜区颗粒样沉积,C3 节段性毛细血管壁、系膜区颗粒样沉积,少量肾小管壁IgG+。
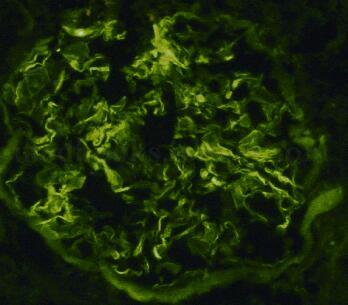
图28‐4 肾脏病理免疫荧光表现IgG×400
病理诊断:局灶增生坏死性肾小球肾炎伴部分新月体形成,符合抗GBM 肾炎。
治疗及转归
患者入院后重复行肾活检,病理符合抗GBM 肾炎。经过前期强化免疫抑制治疗,肾小球中新月体的比例已有明显减少。虽然外周血经过国际上通用的ELISA 法检测为阴性,但是鉴于患者肾小球毛细血管袢仍表现为IgG 线条样沉积,推测血清中仍存在抗GBM 抗体。经过以正常肾组织为底物的间接免疫荧光法证实患者外周血抗GBM 抗体阳性,滴度1 ∶16。说明抗GBM 病诊断无误。遂给予血浆置换治疗,每次3000ml,直至抗体转阴,共9次。继续应用泼尼松15mg 每天一次,并给予CTX 治疗(0.6g/月),总量约8g。治疗2周后复查尿蛋白定量0.31g/24h,1月后复查Scr 97μmol/L。出院后回到原转诊医院门诊随诊,目前血清肌酐(Scr)74μmol/L,尿常规:PRO 阴性,RBC 3个/HP。
讨论
该患者第一次肾活检后,考虑抗GBM 肾炎,给予大剂量激素冲击联合CTX 治疗,因没有发现血液中的抗GBM 抗体,给血浆置换带来很大的顾虑,同时,也给诊断蒙上一层阴影。第二次入院后,首先通过重复肾活检,进一步确定了该患者抗GBM 肾炎的诊断,同时,证实了前期的强化免疫抑制治疗具有明显的疗效,患者肾小球中新月体的比例已有明显减少,但目前肾脏病理中仍有纤维素样坏死及较多的细胞性新月体等活动病变,和患者临床上肾功能不恢复及明显的血尿是一致的,因此,为进一步的治疗提供了依据。此外,依靠北京大学肾脏病研究所的进一步检测发现应用间接免疫荧光法可以检测到患者血清中的抗GBM 抗体阳性,使诊断得到了进一步明确。同时也说明国际通用的商品化的检测抗 GBM 抗体的试剂盒也可能漏诊个别患者,而经典的间接免疫荧光法仍可在诊断上提供证据。
对于抗GBM 病的治疗,目前为止,血浆置换仍是唯一能够改善肾脏及肺脏预后的治疗方法。其疗效与患者的临床表现、开始治疗的早晚和治疗是否充分密切相关。循证医学研究指出血浆置换治疗应早期充分进行,才能达到清除抗体、改善预后的作用。进行充分的血浆置换,置换量应为每天50ml/kg(最多4L),共14天或置换至血清抗体转阴。置换液多为5%的白蛋白,因其并发症较少,但置换后应给予一定量新鲜冰冻血浆以补充凝血因子。对于有肺出血的患者,提倡用新鲜冰冻血浆作置换液。但是临床上出现少尿或无尿、血清肌酐(Scr)>600μmol/L 及肾活检中>85%的肾小球有大新月体形成是该病预后不好的指标[2]。对于这部分患者则不再建议应用血浆置换,除非出现肺大出血时用于挽救生命[3]。在进行血浆置换的同时应给予甲泼尼龙冲击治疗,7~15mg/(kg •d)(<1g/d)×3天,其后给予泼尼松60mg/d ×4周,每1~2周逐渐减量。同时给予环磷酰胺治疗,<55岁的患者,可给予3mg/(kg •d),>55岁的患者,则减为2mg/(kg •d),总量6~8g。
此患者前期已给予强化免疫抑制治疗,为促进肾功能的恢复,给予了血浆置换治疗。治疗过程中用间接免疫荧光的方法,动态监测血清中的抗体水平,直至抗体转阴。此后继续泼尼松和环磷酰胺的治疗。经过1年的随访治疗,患者肾功能恢复正常,血尿、蛋白尿基本消失。
该病例有以下特点:①病程进展较缓,肾功能损害较轻;②ELISA 法测血清抗GBM 抗体阴性,但间接免疫荧光法检测为阳性。
参考文献
[1]王海燕.肾脏病学.第3版.北京:人民卫生出版社,2008:871 .
[2]崔昭,刘玉春.抗肾小球基底膜抗体相关疾病的预后研究.临床内科杂志,2004,21(10):677‐680 .
[3]Jindal KK .Management of idiopathic crescentic and diffuse proliferative glomerulonephritis:evidence‐based recommendations .Kidney Int Suppl,1999,70:33‐40 .
(徐德宇 崔昭 赵明辉 乔青)
来源:《内科疑难病例.泌尿分册》
作者:杜新 齐卡
参编:陈光磊 余鹏程 徐德宇 毕礼明 刘伟
页码:283-297
出版:人民卫生出版社

















共0条评论