▌上海交通大学医学院附属仁济医院肿瘤科,上海交通大学胰腺癌诊治中心,上海市胰腺疾病重点实验室杨旭光 焦锋 王理伟
2016年1月,中国国家癌症中心主任赫捷院士等在《临床医师癌症杂志》(CA Cancer J Clin)杂志发布的《2015 年中国癌症统计》数据显示,我国胰腺癌占总体恶性肿瘤发病率和死亡率的第9 位和第6 位,并且呈快速上升趋势。美国的流行病学数据预计2016年胰腺癌死亡率列第4位,2030年将升至第2位。总体来说,全球范围内胰腺癌发病率逐年上升,预后极差。因此,为了更好地提高胰腺癌诊治水平,亟须转化医学以及临床研究的快速发展。本文就2016年胰腺癌研究进展进行回顾。
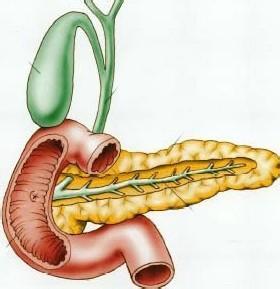
胰腺癌转化医学进展
1. 新的胰腺癌分型:胰腺癌是四种独立的疾病
2016年初,《自然》杂志发表重要研究,通过对7年中456份胰腺癌样本基因组测序分析,最终确定正常胰腺组织恶化过程关键的10条信号通路和32个基因,揭示四种胰腺癌亚型,即鳞型(Squamous)、胰腺祖细胞型(Pancreatic Progenitor)、免疫源性(Immunogenic) 和内外分泌异常分化型(ADEX)。研究提示胰腺癌可能是四种独立疾病,拥有不同的生存率、治疗方法和遗传学特征,鉴定不同的胰腺癌类型为胰腺癌精准医疗提供了依据,遗传机制的鉴定也为抗癌药研发提供了良好分子基础。
2. 新的胰腺癌进展观点:逐步积累还是一步爆发?
1996年,赫鲁本(Hruban)等提出促癌基因KRAS及抑癌基因CDKN2A 、TP53和 SMAD4等突变的逐步积累是胰腺癌进展基础。然而,2016年一项最新研究对此提出挑战。诺塔(Notta)等检测107例胰腺癌患者基因组,发现染色体碎裂事件可导致胰腺癌发生所必须的两个或者更多基因突变同时发生,而不是之前认为的顺次发生。然而,部分胰腺癌中染色体碎裂事件仍符合逐步进展模型,其中一例患者染色体碎裂导致单拷贝CDKN2A、TP53和SMAD4驱动基因同时失活,但仍存在5个重要突变不与这3个基因突变同时发生,表明胰腺癌进展中的一个步骤可能包括多种突变。研究为揭示胰腺癌起源和进展的分子机制提供了思路。
胰腺癌临床研究进展
1. 多学科综合诊治(MDT)理念
胰腺癌MDT诊疗模式,应以胰腺外科为中心,联合肿瘤内科、放疗科、消化内科、病理、放射诊断科、营养科、麻醉科、重症监护病房(ICU)等科室专家,在固定时间和地点,针对某一疾病,进行讨论并制定出治疗方案。MDT模式首先打破了“单打独斗”模式,避免由于单一、混乱的诊治而耽误病情的情况。
其次,MDT团队可充分利用现有医疗资源,制定出最合理方案,提高疾病治疗效果。
第三,通过MDT,患者可避免重复性医疗过程,节约住院时间的同时节约检查费用。
2. 精准医疗模式
胰腺癌的精准医疗模式,则可以在MDT多学科联合制定好方案后,根据患者的基因变化等数据,来判断治疗方案的敏感性、耐药性、预后等问题,以此对患者进行个体化的治疗,使得治疗更加精准有效。
目前来说,在MDT这种多学科合作、共同诊治的理念下,贯彻进行精准医疗的模式,是针对胰腺癌患者进行治疗的最佳方案。
3. 临床研究进展
■ 辅助治疗
ESPAC-4研究 吉西他滨(GEM)+卡培他滨(CAP)对比GEM单药用于胰腺癌根治术后辅助治疗的国际多中心、开放性、随机对照Ⅲ期临床研究。
2016年6月,美国临床肿瘤学会(ASCO)年会报道ESPAC-4研究结果。GEM+CAP组总生存(OS)显著长于GEM单药组(28.0个月对25.5个月);5年OS率为28.8% 对16.3%; GEM+CAP组不良反应多于GEM单药组,但总体可控,且不存在统计学差异,严重不良反应(SAE)发生率为24%对26%。GEM+CAP5年OS率高于之前ESPAC研究,包括无辅助化疗8.0%、放化疗10.8%和5-氟尿嘧啶(FU)/亚叶酸钙(FA) 15.9%。ESPAC-4研究结果提示,治疗晚期胰腺癌的药物用于辅助治疗,或许可为患者带来更大获益,所有胰腺癌患者均应参与随机对照临床研究,必须评估有效的生物标志物。GEM+CAP可成为胰腺癌术后辅助治疗新的标准方案。
JASPAC-01研究 比较胰腺癌术后辅助化疗替吉奥在生存期及生活质量方面是否非劣效于GEM。
2016年7月,《柳叶刀》(Lancet)杂志在线发表JSPAC-01更新数据,研究纳入的385例胰腺癌患者中,不仅达到了非劣效性,同时也达到了优效性终点(P<0.0001)。与GEM组比较,替吉奥中位OS期显著延长(46.5个月对25.5个月);死亡风险降低(HR=0.57);无复发生存(RFS)期也显著延长(22.9个月对11.3个月,HR=0.60)。其中,预后较差的局部复发和肝转移的风险也显著降低。GEM组与替吉奥组的5年OS率分别为24.4%和44.1%。对于亚洲人群,替吉奥单药也是胰腺癌辅助治疗好的选择。
■ 晚期一线治疗
MAESTRO研究 evofosfamide(TH302)+GEM对安慰剂+GEM治疗转移或局部进展不可切除胰腺导管腺癌,随机、双盲Ⅲ期临床研究。
2016年2月,ASCO胃肠肿瘤研讨会(ASCO GI)会议报道MAESTRO研究结果。TH302+GEM对Placebo+GEM中位OS为8.7月对7.6个月;1年OS率为34.2%对29.8%(P=0.059);中位无进展生存(PFS)期为5.5个月对3.7个月(P=0.002)。尽管MAESTRO研究主要研究终点OS期仅获得了边缘性的统计学差异,但TH302这个乏氧相关药物和胰腺癌标准治疗药物GEM联合仍对PFS和客观有效率(ORR)具有贡献,也未观察到新的安全性问题。
值得一提的是,该研究入组了123例(17%)来自日本和韩国的亚洲患者,这些亚组患者在联合治疗组的死亡风险较安慰剂组下降了42%,联合治疗组获得了12.0个月的OS期,而在安慰剂组OS期仅有8.5个月。
对比本研究中其他种族(欧洲和美国患者联合治疗组OS期均为7.4个月)的患者,亚洲患者的OS获益最大。这个亚组分析结果若能够得到进一步验证,或许能为亚洲的胰腺癌患者带来新的治疗突破。
■ 晚期二线治疗
NAPOLI-1研究 纳米脂质体伊立替康、5-FU/LV、纳米脂质体伊立替康+5-FU/LV三组比较,治疗GEM治疗后进展的转移性胰腺癌的Ⅲ期临床研究。
2016年2月,Lancet杂志在线发表NAPOLI-1更新数据,接受纳米脂质体伊立替康+5-FU/LV和5-FU/LV患者的OS期分别为6.1 个月和4.2个月(HR=0.67,P=0.012),但纳米脂质体伊立替康单药较5-FU/LV并不能明显改善生存(4.9个月对4.2 个月; P=0.94)。纳米脂质体伊立替康+5-FU/LV可作为GEM方案治疗后进展的转移性胰腺癌二线治疗选择。
结语
目前,胰腺癌转化医学和临床研究发展迅速,但仍须建立高效研究模式。2016年中国临床肿瘤学会(CSCO)年会主题为“精细管理,精准医治”,提示要合理综合各学科,加强基础研究,逐步了解胰腺癌发生发展机制;注重转化医学研究,并更好地将研究成果运用于临床;充分利用临床资源,合理设计临床试验,建立多学科综合诊疗模式,实现真正的精准医疗,最终达到攻克胰腺癌的目的。(编辑《中国医学论坛报》贾春实)














共0条评论