三、卵巢生殖细胞肿瘤
01. 卵巢成熟性畸胎瘤
定义
成熟性畸胎瘤是完全由两个或三个胚层(外胚层、中胚层和/或内胚层)来源的成熟组织形成的肿瘤。
ICD-O编码
9080/0 良性畸胎瘤
ICD-11编码
2F32.Y & XH3GV5 卵巢的其他特指型良性肿瘤&良性畸胎瘤
相关命名
可接收:成熟性囊性畸胎瘤
不推荐:皮样囊肿;成熟性实性畸胎瘤
亚型
富细胞性纤维瘤
部位
卵巢
流行病学
在病理学研究中,这些病例占卵巢肿瘤的20%。
临床特征
大多数病例发生于育龄期妇女。常见症状是腹痛或肿块;有些病例是偶然发现。罕见情况下,年轻妇女可表现为抗-NMDAR脑炎。大概10%的病例为双侧性。
译注:NMDAR:N-methyl-D-aspartic acid receptor,N-甲基-D-天冬氨酸受体
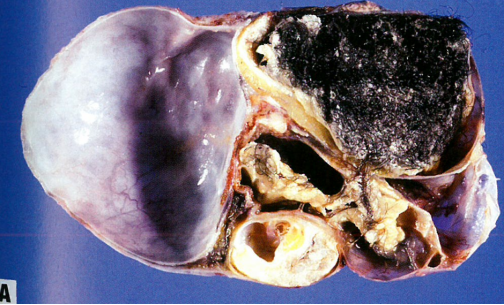
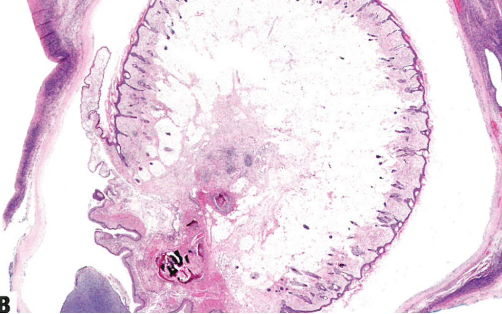
图1.100 成熟性囊性畸胎瘤。A 大体上呈多囊性。部分囊内充毛发和皮脂腺物质。B 成熟性囊性畸胎瘤常有实性结节(Rokitansky结节),该结节被覆有毛皮肤并含有皮肤附属器结构和脂肪组织。结节内也可见其他多种组织(如,神经胶质上皮、骨、软骨和内胚层组织)。
病因学
未知
发病机制
倾向于孤雌生殖理论,认为起源于原始生殖细胞。
大体检查
多为囊性(成熟性囊性畸胎瘤)但有些病例为实性。通常5-10cm,但在抗-NMDAR脑炎的妇女,肿瘤较小(平均1.9cm)。囊肿含有皮脂腺物质、毛发,有时有牙齿和软骨。囊壁常有被覆着有毛皮肤的结节(Rokitansky结节,俗称头节)。成熟性实性畸胎瘤为实性,有散在的囊肿。类似畸形人类胎儿者,称为胎儿状畸胎瘤。实性区域应广泛取材(理想情况下,实性区域取1块/cm)。

图1.101 成熟性囊性畸胎瘤:肿瘤的常见成分。A 鳞状上皮、皮脂腺和毛囊。B 气道型上皮和腺体。C 神经型组织。D 软骨和骨。

图1.102 成熟性囊性畸胎瘤。抗-NMDAR脑炎的患者,明显的伴有生发中心的淋巴组织围绕着神经胶质组织,这不是成熟性囊性畸胎瘤的典型表现。
组织病理学
外胚层衍生物包括鳞状上皮和皮肤附属器结构,以及神经内胚层(胶质细胞,室管膜,小脑)。中胚层衍生物包括脂肪、骨、软骨和平滑肌。内胚层衍生物包括胃肠道和气道/支气管上皮、甲状腺和涎腺。罕见前列腺、垂体、肾上腺和甲状旁腺。显微镜下可能发现极小灶未成熟性神经组织。常见脂肪坏死和针对角蛋白的异物巨细胞反应。抗-NMDAR脑炎的患者,有生发中心的淋巴组织围绕着神经胶质组织。
细胞学
无临床相关性。
诊断性分子病理学
无相关性。
诊断标准
必要标准:至少两个胚层的成熟组织。
分期
无临床相关性。
预后和预测
良性,除非并发恶性转变的罕见病例(见“畸胎瘤起源的体细胞型肿瘤”)和成熟性囊性畸胎瘤(伴囊肿破裂)部分切除后残余卵巢进展成未成熟性畸胎瘤的罕见病例。在成熟性畸胎瘤中,显微镜下发现极小灶未成熟性神经组织具有极佳的临床结局,不应过度诊断为未成熟性畸胎瘤。成熟性畸胎瘤妇女可能发发生腹膜胶质瘤病,对预后没有不利影响。
02. 卵巢未成熟性畸胎瘤
定义
未成熟性畸胎瘤是含有不成熟组织和多少不等成熟组织的畸胎瘤。
ICD-O编码
9080/3 未成熟性畸胎瘤NOS
ICD-11编码
2C73.3 & XH0N49 卵巢的恶性畸胎瘤&未成熟性畸胎瘤,恶性
相关命名
无
亚型
无
部位
卵巢
流行病学
在美国,这是第二常见恶性卵巢生殖细胞肿瘤,通常发生在30岁前。
病因学
未知
发病机制
可能以类似于成熟性囊性畸胎瘤的方式,在相同的发育阶段,通过一种涉及生殖细胞的共同起源,形成未成熟性畸胎瘤。
临床特征
未成熟性畸胎瘤通常表现为盆腔肿块。血清AFP升高者,应广泛取材,以排除卵黄囊瘤,但含有肝样成分者也可能AFP升高。
大体检查
肿瘤通常是单侧,体积大,肉样,灰褐色,囊实性,有出血和坏死。
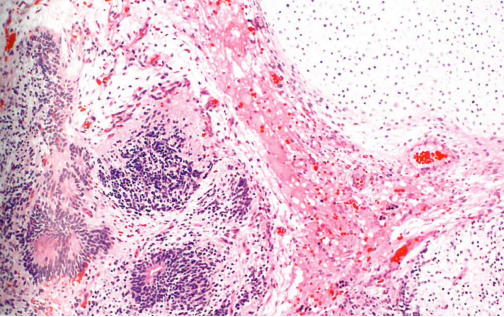
图1.03 未成熟性畸胎瘤。可见软骨附近的不成熟神经外胚层组织。
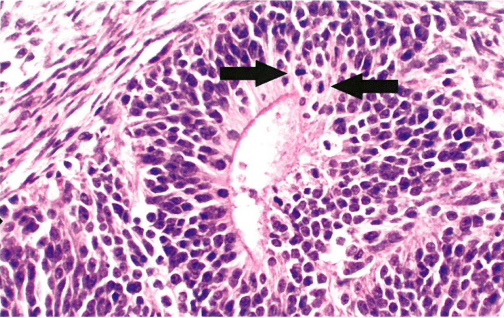
图1.04 未成熟性畸胎瘤。不成熟神经外胚层组织由菊形团组成,含有原始的核分裂象(箭)活跃的细胞,核质比升高,核深染。
组织病理学
数量不等的不成熟组织,最常见为神经外胚层小管和菊形团,夹杂着不同成熟程度的外胚层组织和内胚层组织。小管和菊形团由核分裂象活跃的深染细胞组成。也可能出现细胞丰富的、核分裂象活跃的神经胶质。不成熟的中胚层组织和少见的内胚层组织也可能出现。未成熟性畸胎瘤不应含有局灶性卵黄囊瘤,如果出现,应分类为混合性生殖细胞肿瘤;如果患者有明显的未成熟性畸胎瘤成分但血清AFP水平升高,应广泛取材以寻找卵黄囊瘤病灶/成分,这将促使肿瘤分类改变为混合性生殖细胞肿瘤。
免疫组化,不成熟神经外胚层和肠成分可能呈SALL4阳性。神经外胚层可能呈SOX2和glypican-3(GPC3)阳性。AFP可染不成熟胃肠型腺体。可能出现小梁状或巢状薄壁血管增殖,类似血管肿瘤。
根据任何一张切片中含有不成熟神经上皮的低倍镜视野(直径4.5mm)的合计数量,进行分级(表1.04)。未成熟性畸胎瘤的转移灶使用相同的分级标准;纯粹的腹膜胶质母细胞瘤病视为成熟性(0级)。

图1.105 未成熟性囊性畸胎瘤。不成熟神经外胚层组织主要是实性,很少区域形成菊形团。因为它在1张切片中占据>3个低倍视野,所以是3级。
细胞学
无临床相关性
诊断性分子病理学
无临床相关性
诊断标准
必要标准:含有不成熟神经外胚层组织的生殖细胞肿瘤。
分期
根据国际癌症控制联盟(UICC)TNM分类(见卵巢、输卵管和原发性腹膜TNM分期)和FIGO分期系统进行分期。尽管胶质母细胞瘤病代表3期疾病,其行为一般当作良性,应避免过度治疗。
预后和预测
原发肿瘤的分期和分级,转移性肿瘤(如果有)的分级,是主要的预后因素。5年部分生存率>90%。I期肿瘤,5年生存率接近100%。未成熟性畸胎瘤和胶质母细胞瘤病的最恰当的分期方法,目前是有矛盾的。目前证据提示,胶质母细胞瘤病是良性疾病,不需要化疗,有些病例发生于良性卵巢肿瘤或根本没有卵巢肿瘤的患者。这意味着种植灶必需由手术医生充分取样,病理医生必需仔细地全面地评估。UICC目前建议,当并存未成熟性畸胎瘤时,胶质母细胞瘤病应分期,但没有基于结局的证据支持这种建议。在缺乏这些证据时,许多临床医生和病理医生不愿意因为存在纯粹的胶质母细胞瘤病而上调这种卵巢肿瘤的分期,除非种植灶含有不成熟成分(即,1级或更高)。不论采取哪种方法,重要的是必需仔细地记录种植灶的性质,必需把诊断意义明确地传达给负责治疗的临床医生。化疗后,罕见患者可能形成纯粹的成熟性畸胎瘤组织的卵巢外沉积灶,这就是所谓的成长性畸胎瘤综合征。
03. 无性细胞瘤
定义
无性细胞瘤是一种原始生殖细胞肿瘤,肿瘤细胞未显示特异性分化。
ICD-O编码
9060/3 无性细胞瘤
ICD-11编码
2C73.1 卵巢的无性细胞瘤
相关命名
无
亚型
无
部位
卵巢
流行病学
无性细胞瘤是最常见的恶性生殖细胞肿瘤。约占所有卵巢恶性肿瘤的1%。
病因学
未知
发病机制
12号染色体异常,通常是等位染色体12p或12q扩增,见于80%的无性细胞瘤。KIT突变(外显子12,密码子816)见于30-50%的无性细胞瘤,KIT扩增见于30%的无性细胞瘤。性腺发育不全患者,无性细胞瘤可能起源于并发的性腺母细胞瘤(见“性腺母细胞瘤”)。
临床特征
无性细胞瘤发生于儿童和年轻妇女,以及某些性腺发育不全表型女性的个体。通常表现为腹痛或腹部肿块,血清LDH升高。罕见血清HCG升高,特别是出现合体滋养细胞巨细胞的肿瘤。也可能罕见副肿瘤性高血钙。大多数患者表现为I期疾病。肉眼可见双侧累及者约占10%。纯型无性细胞瘤患者血清AFP不升高。
大体检查
肿瘤通常约15cm大小,肉样,黄色或奶油色,实性,分叶状。可能出现囊性退变、出血和坏死。钙化区域可能提示肿瘤内的性腺母细胞瘤病灶。约20%为双侧,但对侧肿瘤可能肉眼检查不明显。
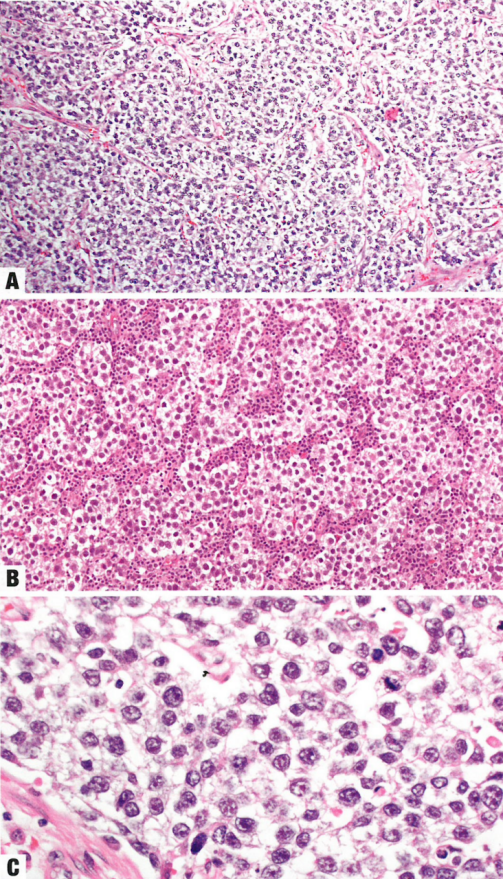
图1.106 无性细胞瘤。A 单一的肿瘤细胞排列成巢,被纤细的纤维性间质所分隔。B 肿瘤细胞聚集灶之间的纤维性间质含有多少不等的淋巴细胞。C 肿瘤细胞核通常成角或方形,有明显核仁。常见核分裂象。
组织病理学
成片和巢状单一性肿瘤细胞被纤细的含有淋巴细胞的纤维性间质所分隔。较少见模式包括条索、小梁、实性小管和假腺体。肿瘤细胞呈多角形,细胞边界清楚,有丰富的透明或嗜酸性胞质,核居中,有一个或两个显著核仁。核轮廓可能成角、方形,常见核分裂象。少数肿瘤出现散在的合体滋养细胞。周围间质可能含有不明显的肉芽肿,并可能遮盖肿瘤,特别是转移部位。罕见情况下,无性细胞瘤可能含有精母细胞瘤样细胞。免疫组化,无性细胞瘤呈SALL4、OCT4、LIN28、MANOG、KIT(CD117)和D2-40阳性。CK可能局灶阳性。EMA、CD30和glypican-3(GPC3)阴性。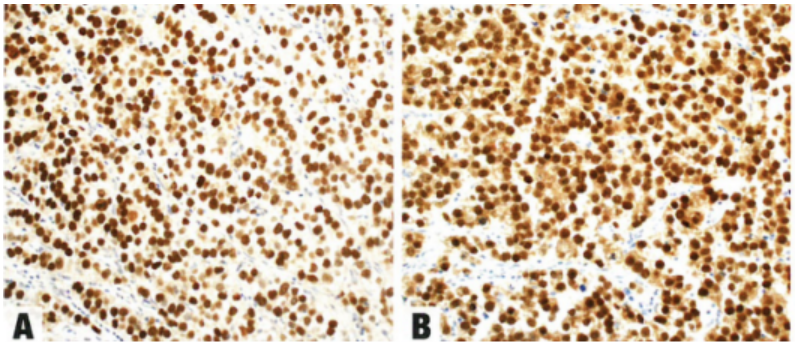
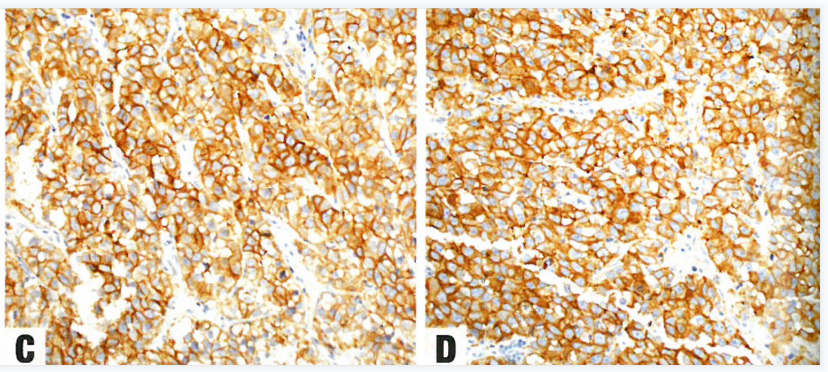
图1.109 无性细胞瘤免疫组化呈SALL4(A)和OCT4(B)核阳性,CD117(C)和D2-40膜阳性(D)。
细胞学
无临床相关性。
诊断性分子病理学
无临床相关性。
必要标准和理想标准
必要:无一的圆形原始生殖细胞伴透明胞质和大核仁,排列成巢或条索,被含有淋巴细胞的纤细的纤维性间质所分隔。
理想:免疫组化证实阳性染色:OCT4或SALL4、KIT(CD117)和/或D2-40。
分期
根据国际癌症控制联盟(UICC)TNM分类(见卵巢、输卵管和原发性腹膜TNM分期)和FIGO分期系统进行分期。
预后和预测
10年无进展生存率>90%。约10%病例复发,通常在初始发病2年内复发。分期是主要预后因素。
04. 卵黄囊瘤
定义
卵黄囊瘤(YST)是一种原始生殖细胞肿瘤,呈现多种模式,相当于内胚层胚外分化(后继于卵黄囊和尿囊)或较少见的内胚层躯体组织(肠、肝和间叶)。
ICD-O编码
9071/3 卵黄囊瘤
ICD-11编码
2C73.Y & XH09W7 卵巢的其他特指型恶性肿瘤&卵黄囊瘤
相关命名
不推荐:内胚窦瘤;原始内胚层肿瘤
亚型
无
部位
卵巢
流行病学
约占卵巢恶性生殖细胞肿瘤的20%。
病因学
未知
发病机制
大约75%的病例有12号染色体异常,最常见等位染色体12p异常。较年长患者,与卵巢的或子宫内膜的恶性肿瘤并发的YST,认为是体细胞肿瘤起源。
临床特征
最常见于10-30岁,表现为腹痛和/或盆腔肿块。大多数患者血清AFP明显升高。较年长患者,YST也可能与卵巢的或子宫内膜的恶性肿瘤并发。
大体检查
单侧,大肿块(平均15cm),实性和囊性,质脆易碎,出血,坏死。
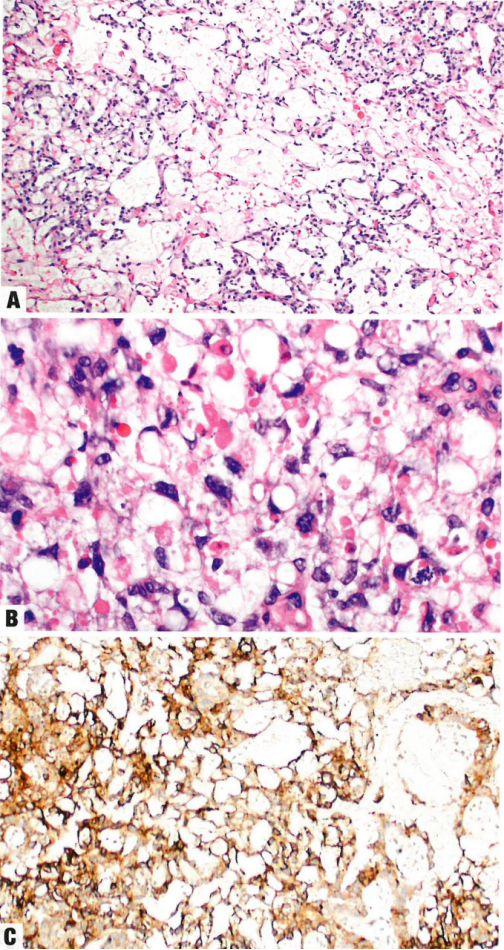
图1.111 卵黄囊瘤。A 网状/微囊模式,由被覆肿瘤细胞的相互交错吻合的腔隙和囊肿组成。B 卵黄囊瘤常见嗜酸性透明小球,但无肿瘤特异性。C GPC3阳性。
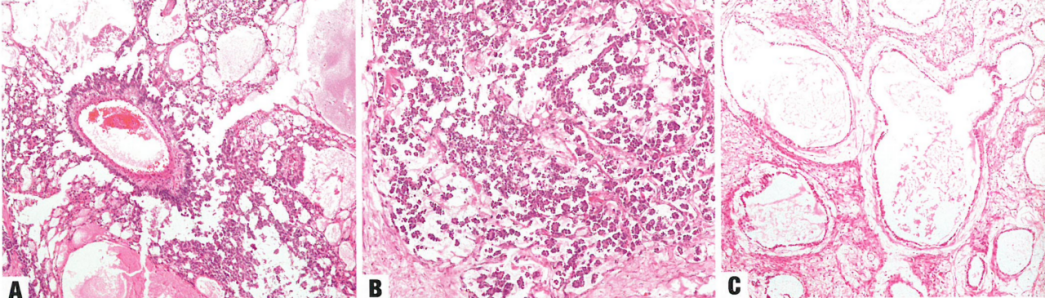
图1.112 卵黄囊瘤。A SD小体是被覆肿瘤细胞的乳头,中心为大血管,位于内胚窦模式的囊腔内。B乳头状模式。C 多泡卵黄囊模式由大量大小不一的空泡和微囊组成的蜂窝状模式,位于纤维性间质内。
组织病理学
常有多种模式,最常见网状/微囊模式:衬覆单层肿瘤细胞的腔隙和囊肿吻合成网。其他模式包括内胚窦模式(增殖的Schiller-Duval小体(SD小体),圆形或拉长的肿瘤细胞被覆的乳头,乳头中心具有大血管,伸入肿瘤细胞围绕而成的囊腔内)、乳头状模式、实性模式、花彩模式(复杂的缎带样或波浪起伏的条索状)和腺样模式(子宫内膜样或肠型)。少见模式包括多泡-卵黄囊模式(大量的空泡和囊肿,位于富细胞性间质内)、贴壁模式(肿瘤细胞埋陷于线性条索状基底膜物质内)、间充质样模式(肿瘤细胞散在分布于水肿性或粘液样结缔组织内)和肝样模式。肿瘤细胞的形态取决于生长模式,但通常呈现不同程度的异型性、透明胞质和透明小球。较年长患者,与卵巢的或子宫内膜的恶性肿瘤并发的YST,通常呈现网状模式。
阳性免疫组化标记物包括SALL4、LIN28、AFP(通常局灶弱阳性)、glypican-3(GPC3)和ZBTB16,以及肠型模式表达CDX2,肝样模式表达Hep Par-1,前肠/气道模式表达TTF-1。
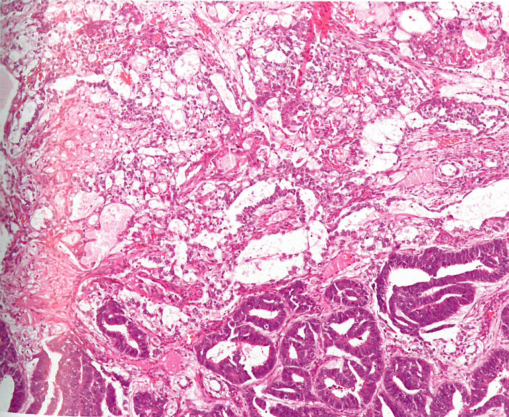
图1.110 卵黄囊瘤。常有多种模式:网状/微囊模式(图上)、内胚窦模式(图中)和子宫内膜样模式(图下)。
细胞学
无临床相关性。
诊断性分子病理学
无临床相关性。
必要标准和理想标准
必要:原始生殖细胞肿瘤,呈现内胚窦胚外模式或体细胞模式。
理想:免疫组化GPC3或AFP阳性。
分期
根据国际癌症控制联盟(UICC)TNM分类(见卵巢、输卵管和原发性腹膜TNM分期)和FIGO分期系统进行分期。
预后和预测
I-II期5年生存率>95%。约10%病例复发,III期为70%,IV期为50%。较年长患者,与卵巢的或子宫内膜的恶性肿瘤并发的YST,预后较差。
05. 胚胎性癌
定义
胚胎性癌是一种原始恶性生殖细胞肿瘤,呈现体细胞性分化或胚外分化。
ICD-O编码
9070/3 胚胎性癌
ICD-11编码
2C73.Y & XH8MB9 卵巢的其他特指型恶性肿瘤&胚胎性癌
相关命名
无
亚型
无
部位
卵巢
流行病学
纯粹的胚胎性癌罕见,1976年一项小样本临床病理研究中最常见表现为混合性生殖细胞肿瘤的成分之一。
病因学
未知
发病机制
常见12号染色体异常(等位染色体12p扩增)。
临床特征
纯型肿瘤发生于儿童和年轻妇女(平均年龄12-25岁),罕见于较年长成人。临床表现为腹腔肿块和腹痛。常见内分泌改变,包括性早熟和月经异常。血清HCG和AFP可能升高。
大体检查
肿瘤通常单侧性,平均大小约16cm,实性,出血和坏死。
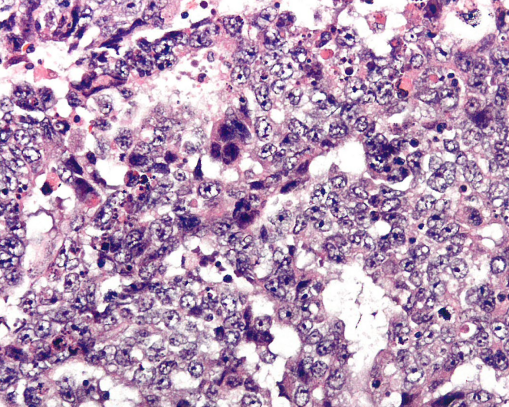
图1.114 胚胎性癌,腺样模式由多形性肿瘤细胞和合体滋养细胞巨细胞组成。
组织病理学
胚胎性癌由单一形态至多形性细胞组成,生长方式呈实性、巢状、腺样和乳头状模式,通常多种模式混杂。肿瘤细胞呈多角形,含有丰富的双嗜性或透明胞质,核分裂象活跃,核深染,重度异型性。可能出现合体滋养细胞巨细胞。卵巢胚胎性癌最常见表现为与其他恶性生殖细胞肿瘤成分相混杂,因此归入混合性生殖细胞肿瘤。免疫组化,胚胎性癌呈CD30、OCT4、SALL4、SOX2和LIN28阳性(见表1.03)。

图1.113 胚胎性癌,腺样和乳头状模式。
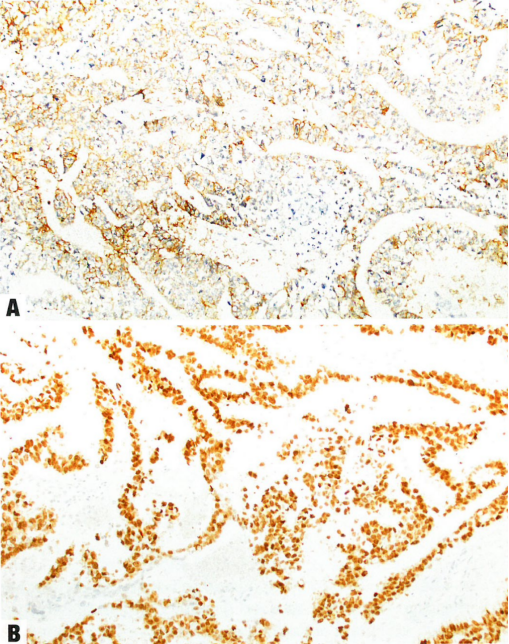
图1.115 胚胎性癌。A CD30呈膜阳性。B SOX2呈核阳性。
细胞学
无临床相关性。
诊断性分子病理学
无临床相关性。
必要标准和理想标准
必要:高级别原始恶性生殖细胞排列成腺样、乳头状和/或实性模式。
理想:免疫组化OCT4和CD30或SOX2阳性。
分期
根据国际癌症控制联盟(UICC)TNM分类(见卵巢、输卵管和原发性腹膜TNM分期)和FIGO分期系统进行分期。
预后和预测
纯型肿瘤只有很少临床结局数据,因为极罕见。早先的一项包括15例的免疫组化研究中,生存率为39%。当代研究都是混合型胚胎性癌(见“卵巢的混合性生殖细胞肿瘤“)。
06. 非妊娠性绒癌
定义
非妊娠性绒癌是一种非妊娠起源的、由细胞滋养细胞和合体滋养细胞组成的恶性肿瘤。
ICD-O编码
9100/3 绒癌NOS
ICD-11编码
2C73.Y & XH8PK7 卵巢的其他特指型恶性肿瘤&绒癌NOS
相关命名
无
亚型
无
部位
大多数发生于卵巢,但可能罕见累及附件周围或盆腔软组织。
流行病学
非常罕见,仅有少数病例报道,在所有卵巢肿瘤中占比<1%。
病因学
未知
发病机制
在儿童和年轻妇女,肿瘤为生殖细胞起源。发生于较年长妇女的罕见病例,表现为含有小灶绒癌的卵巢上皮性癌,这种绒癌病灶可能起源于体细胞肿瘤。短串联重复(STR)DNA基因检测,肿瘤呈等同于患者正常组织的等位基因模式。也可能见到等位基因失衡。
临床特征
肿瘤累及儿童和年轻妇女。患者表现为腹痛、盆腔肿块和阴道出血或(罕见)腹腔积血。血清HCG通常升高。多达半数患者有同性性早熟。罕见情况下,较年长妇女的卵巢上皮性癌含有小灶绒癌,后者可能是体细胞肿瘤起源而不是生殖细胞起源。
大体检查
肿瘤通常巨大,实性,出血和坏死。

图1.116 卵巢的非妊娠性绒癌。A 肿瘤由细胞滋养细胞和合体滋养细胞组成。B细胞滋养细胞和合体滋养细胞密切混合。
组织病理学
肿瘤含有混杂的单核细胞滋养细胞和多核合体滋养细胞,常有广泛的出血和坏死,并遮盖肿瘤细胞。有些肿瘤主要为单核滋养细胞。免疫组化,肿瘤呈HCG阳性。肿瘤可表现为纯型,也可为混合性生殖细胞肿瘤的成分之一。较年长妇女,小灶绒癌可能出现在卵巢上皮性癌中。
细胞学
无临床相关性。
诊断性分子病理学
STR DNA基因分型可用于区分非妊娠性绒癌与子宫或输卵管妊娠性绒癌,后者含有来自父方的非母方等位基因。
必要标准和理想标准
必要:双相肿瘤,由单核细胞滋养细胞和多核合体滋养细胞组成,非妊娠起源。
分期
根据国际癌症控制联盟(UICC)TNM分类(见卵巢、输卵管和原发性腹膜TNM分期)和FIGO分期系统进行分期。
预后和预测
较常见淋巴管扩散和腹腔内扩散,化疗敏感性不如妊娠性绒癌。伴有卵巢上皮性癌预后差。
07. 卵巢的混合性生殖细胞肿瘤
定义
混合性生殖细胞肿瘤含有两种或更多种恶性生殖细胞成分。
ICD-O编码
9085/3 混合性生殖细胞肿瘤
ICD-11编码
2C73Y & XH2PS1 卵巢的其他特指型恶性肿瘤&混合性生殖细胞肿瘤
相关命名
无
亚型
无
部位
卵巢
流行病学
占所有恶性生殖细胞肿瘤的10-20%。主要发生于儿童和年轻成人。罕见病例发生于异常核型患者,有时起源于性腺母细胞瘤。
病因学
未知
发病机制
许多肿瘤呈现12p或等臂染色体12p的获得。部分肿瘤起源于正常或异常核型患者的性腺母细胞瘤。
临床特征
腹痛、腹腔肿块和月经紊乱是典型的特征性临床表现。月经前期儿童可表现为假性性早熟。血清LDH、HCG或AFP可能升高,取决于肿瘤内出现哪种成分。
大体检查
肿瘤体积大,平均15cm,有实性和囊性区域。大体表现取决于所出现的肿瘤成分。无性细胞瘤呈褐色、肉样,卵黄囊瘤含有小囊肿和坏死灶。绒癌有出血和坏死。胚胎性癌含有坏死区。未成熟性畸胎瘤可能有骨或软骨而呈现沙砾感。
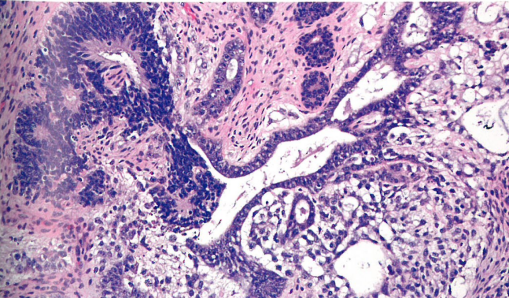
图1.117 混合性生殖细胞肿瘤,含有未成熟性畸胎瘤(原始细胞,神经外胚层菊形团)、胚胎性癌(高度异型细胞,腺样增殖)和卵黄囊瘤(微囊模式)。
组织病理学
大多数肿瘤含有两种或更多种恶性生殖细胞成分;少数肿瘤含有三种或更多成分。定性为混合性生殖细胞肿瘤所需的第二种成分最少占比,尚未定义。未成熟性畸胎瘤含有卵黄囊瘤或胚胎性癌病灶>3mm,归入混合性生殖细胞肿瘤。最常见组合是无性细胞瘤和卵黄囊瘤;其他成分可能包括胚胎性癌、绒癌和未成熟性畸胎瘤。每个成分的形态学和免疫组化特征等同于其对应的纯型肿瘤。这些成分通常密切混合,但也可能出现在肿块中的不同区域。
细胞学
无临床相关性。
诊断性分子病理学
无临床相关性。
必要标准和理想标准
必要:两种或更多种恶性生殖细胞成分。
分期
根据国际癌症控制联盟(UICC)TNM分类(见卵巢、输卵管和原发性腹膜TNM分期)和FIGO分期系统进行分期。
预后和预测
最重要的预后因素是分期。当代化疗,肿瘤成分对预后的影响小于以往,但因为多种成分的化疗敏感性各不相同,应当报告每种肿瘤成分在整个肿瘤中的百分比。































共0条评论