[导读] 编译整理:强子
随着肿瘤诊疗研究的不断进步,生物学标记物已成为病理报告中不可或缺的一部分。对于消化道恶性肿瘤来说,某些生物学标记物具有预测和预后意义。所谓预测意义,是指相关标记的结果可提示相应治疗对于某些治疗是否有效;所谓预后意义,则是相关指标的结果有助于该例病程及预后的判定。近日,美国贝斯以色列女执事医疗中心(Beth Israel Deaconess Medical Center)病理专家Rosenbaum和Gonzalez在《Semin Diagn Pathol》杂志发表综述,对于消化道恶性肿瘤中这一问题进行了详尽介绍。为帮助大家更好的了解并促进临床病理联系,我们将该文要点编译介绍如下。
食管及胃(一)
食管鳞状细胞癌中,已有诸多治疗获益生物学标记物的研究,但目前没有哪一项得到广泛认可。目前最常用的可能是PD-L1免疫组化检测。PD-1是一种位于淋巴细胞表面的免疫检查点蛋白,与某些细胞表面的PD-L1相互作用,导致淋巴细胞凋亡、免疫下调,阻止不希望出现的免疫相互作用,如自身免疫。因此,表达PD-L1的肿瘤细胞可以逃避免疫攻击;也正是因为这一点,所以应用PD-1抑制剂(如派姆单抗、纳武单抗)可以破坏这一相互作用,目前已证实具有治疗多种恶性肿瘤的作用。
病理医师评估PD-L1的免疫组化结果,确定具体相应肿瘤是否适合抗PD-1/PD-L1治疗。评估胃肠道癌中PD-L1表达情况的标准方法是联合阳性分数(Combined Positive Score,CPS)。其计算方法是:至少部分细胞膜着色的肿瘤细胞、肿瘤相关炎症细胞(巨噬细胞及淋巴细胞),除以评估区域内的肿瘤细胞总数(为充分评估,至少计数100个),然后乘以100。
鉴于该计算比较复杂,因此有研究称其组内相关系数(intraclass correlation coefficient)毫不意外的特别低;但另一PD-L1评估方法-肿瘤细胞阳性比例分数(Tumor Proportion Score,TPS)的观察者间可靠性较高。CPS一般是用克隆号22C3的抗体检测,预测派姆单抗的效果;而克隆号28-8的抗体预测的是纳武单抗的效果;不过,这两种克隆号的抗体在不同CPS阈值的情况下都具有较高的一致性。
食管鳞状细胞癌中常见PD-L1表达,且与预后差有关。根据KEYNOTE-180实验(改善总体有效率及有效的时间)和KEYNOTE-181实验(改善总生存时间),美国食品和药品管理局在2019年7月批准为了派姆单抗用于PD-L1的CPS≥10的食管鳞状细胞癌二线治疗,这种情况在食管鳞癌中的比例大约为28%。最近,2021年3月美国食品和药品管理局又批准了一线应用派姆单抗、联合化疗用于局部进展期、不可切除且不适合其他治疗方案的食管鳞状细胞癌,而不必考虑PD-L1的CPS结果。这一决策的依据是KEYNOTE-590实验中发现总生存时间和无进展生存时间都有改善。与其有点相似的是,2021年4月公布的Checkmate588研究中,结果表明手术切除后应用纳武单抗改善食管鳞状细胞癌的无病生存,而与PD-L1的表达无关;不过,事后分析(post-hoc analysis)表明,CPS≥5的恶性肿瘤中有效率更高。
食管鳞状细胞癌已常规进行免疫组化评估的标记物中,EGFR的前景可能最为乐观。食管鳞状细胞癌中EGFR的表达与预后差有关,但也有一项II期临床试验表明,免疫组化中EGFR高表达、或FISH检测中EGFR扩增,与EGFR酪氨酸激酶抑制剂埃克替尼效果增强之间有弱相关性。另一项II期临床试验报道中,EGFR抑制剂吉非替尼作为二线治疗取得了一定成功(modest success)、尤其用于鳞状细胞癌时,且相关结果表明在确定EGFR状态方面,免疫组化优于荧光原位杂交。最后,在一项EGFR抑制剂厄洛替尼的III期临床试验中,免疫组化中EGFR表达与预后改善有关。不过,目前还没有关于免疫组化EGFR的标准评分方案,在某一方案得到验证之前,不太可能得到广泛应用。
胃食管交界处和胃的腺癌在治疗上有很多相似之处,包括免疫组化标志物方面的问题也有相似之处,因此本文放到一起讨论。这类腺癌中,PD-L1的状态也可用CPS来确定。2017年9月,美国食品和药品管理局批准了派姆单抗用于CPS≥1的进展期胃食管交界处腺癌、胃腺癌的治疗,其根据是KEYNOTE-059研究。后续KEYNOTE-590和Checknate 577研究数据表明,PD-1抑制剂作为一线和二线治疗进展期胃食管交界处腺癌的效果和食管鳞状细胞癌一样有效。进一步研究表明,纳武单抗联合化疗改善了CPS≥5的胃食管交界处腺癌或胃腺癌患者的无进展生存、总生存(Checkmate649试验,美国食品药品管理局2021年4月批准);且研究表明,派姆单抗联合曲妥珠单抗及其他化疗药,改善了HER2阳性胃食管交界处腺癌、胃腺癌患者的总体有效率(KEYNOTE-811试验的中期数据,CPS相关资料尚不清楚,美国食品药品管理局2021年5月批准)。上述大量研究(CPS的具体情况不一)以及美国食品药品管理局的批准,都表明生物标记评估区域正在快速发展,病理医师解读PD-L1结果应注明所用克隆号(22C3、还是28-8)并报告CPS的数值,而不是仅仅报告为“阳性”、“阴性”。
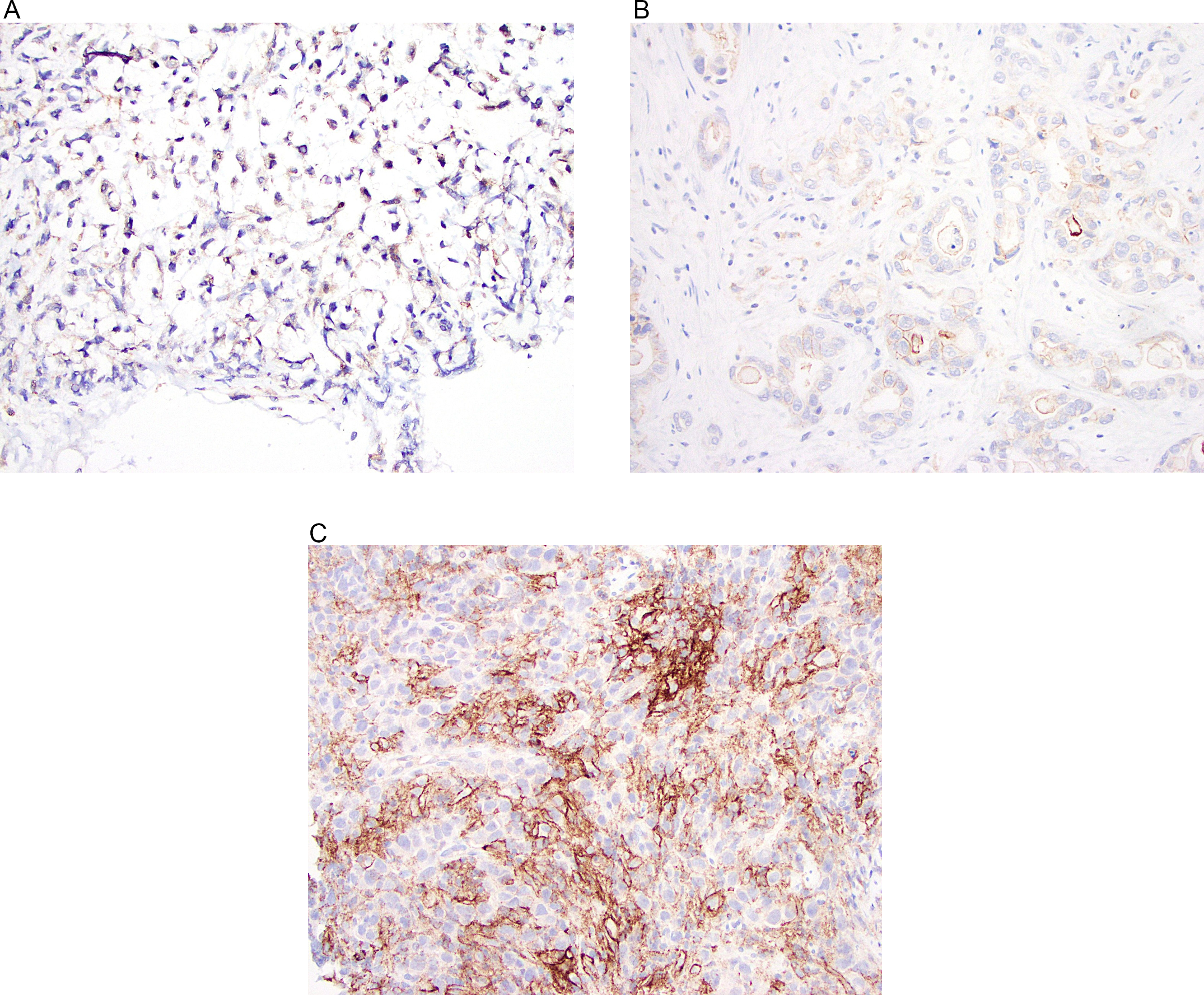
图1. (A)本例胃腺癌PD-L1免疫组化CPS结果小于1,表明可能对PD-1抑制剂无效。(B)本例胃腺癌PD-L1免疫组化CPS结果1-5;大量研究表明,这种情况下对PD-1抑制剂的效果不太一致。(C)本例胃腺癌PD-L1免疫组化CPS结果大于10,表明本例对于PD-1抑制剂获益的可能性较大。
未完待续
点击下载原文文献
参考文献
Rosenbaum MW, Gonzalez RS. Immunohistochemistry as predictive and prognostic markers for gastrointestinal malignancies. Semin Diagn Pathol. 2022;39(1):48-57.
doi:10.1053/j.semdp.2021.10.003














共0条评论