病例13 卵巢肝样癌
(hepatoid carcinoma of the ovary,HCO)
【病例介绍】
患者,女,63岁;因“绝经10年后阴道出现半月,腹胀不适1周,加重2日”来我院就诊,妇检子宫增大如孕2+月;盆腔MRI检查示盆腔肿块、腹水形成,倾向附件来源肿瘤;分段诊刮示子宫内膜增生期样改变;予剖腹探查术,术中见腹腔暗红色积血2400ml,肝、胆、胰、脾、双肾未及异常,大网膜、小肠、结肠、肠系膜、阑尾等表面及双侧结肠旁沟均未见肿瘤结节;右侧卵巢增大呈12*13*8cm,实性,分叶哑铃状,包膜色灰白,局部破裂伴活动性出血;左卵巢及双输卵管未及异常;子宫大小正常,腹膜后淋巴结不大;行全子宫双附件大网膜阑尾切除术。
【病理变化】
(1)巨检 右卵巢分叶状肿块,大小16.5*12.5*6cm,切面淡黄灰红色,多结节状,部分区囊性变,内含粘液,质中(图1);附输卵管及另送全子宫、左附件标本未及肿块。
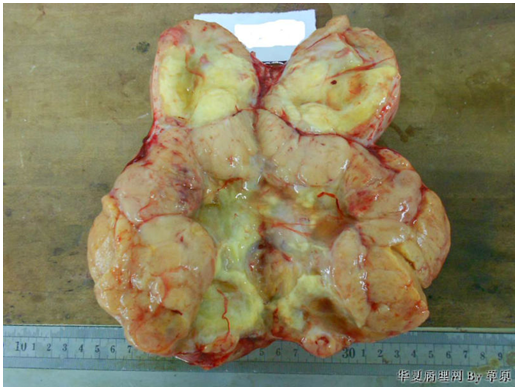
图1 卵巢肝样癌。
(2)镜检 低倍镜示肿瘤细胞部分区域排列呈实性片状、团巢状(图2A、2B),部分呈条索状、小梁状(图2C),其中实性区域主要有两种细胞形态组成,即胞质丰富嗜酸性区域(图2D)和胞质透亮区域(图2E),其中图2A示肿瘤境界相对清晰;高倍镜示胞质丰富嗜酸性区域细胞相对密集,体积较为均匀一致,细胞边缘清晰,成多角形或卵圆形,具有丰富嗜酸性胞质,部分细胞核周透亮,细胞核圆形或卵圆形,位于中央,核仁明显(图2F);胞质透亮区域细胞相对稀疏,细胞体积较大且大小不一,细胞边缘清晰,胞质透亮、似为黏液,细胞核位于中央或偏位呈“印戒细胞”样,大小不一,核膜不规则,部分核深染、部分呈泡状,可见核仁(图2G);肿瘤部分实性区域可见放射状血窦,似肝细胞癌排列方式(图2H);部分区域可见腺样结构,衬覆单层立方上皮(图2I);可见嗜酸性小体(图2J);两种区域均未见明确核分裂像。
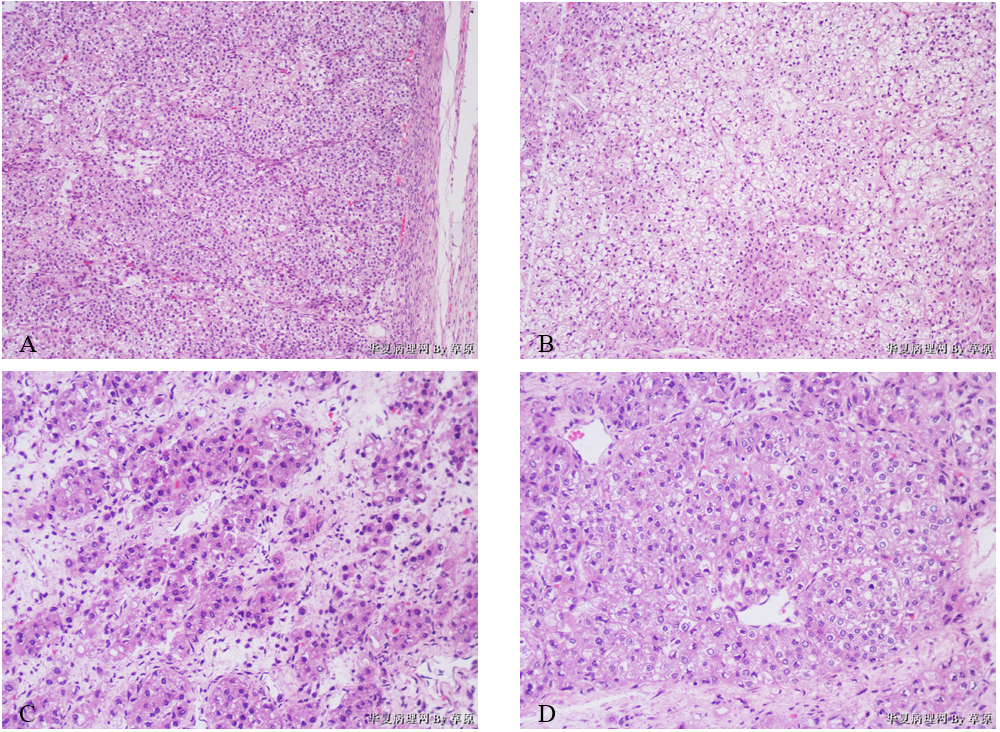
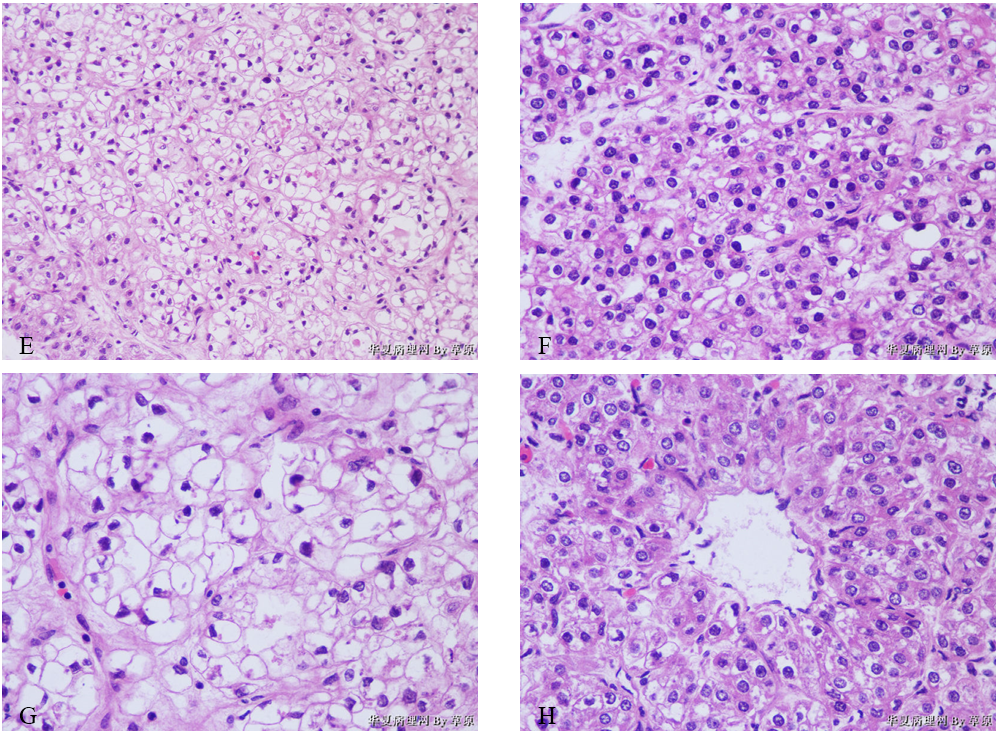
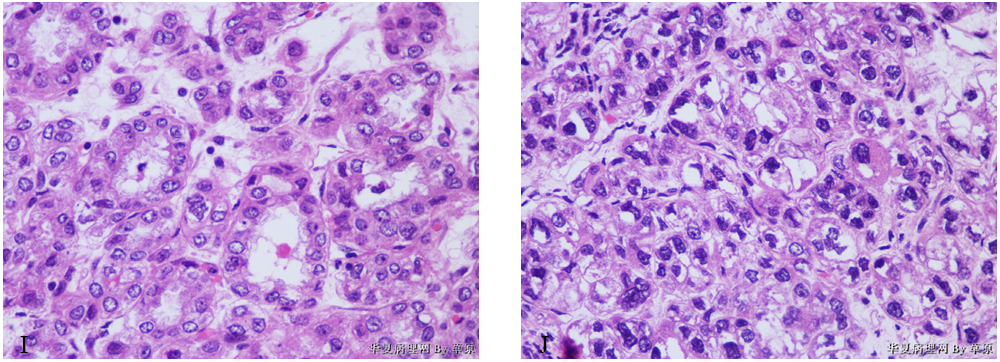 图2 卵巢肝样癌。A、B示肿瘤细胞排列呈实性片状、团巢状;C示肿瘤细胞排列呈条索状、小梁状;D示胞质丰富嗜酸性实性区域;E示胞质透亮实性区域;F示胞质丰富嗜酸性实性区域(高倍);G示胞质透亮实性区域(高倍);H示肝细胞癌样结构;I示部分区域呈腺样结构;J示嗜酸性小体。
图2 卵巢肝样癌。A、B示肿瘤细胞排列呈实性片状、团巢状;C示肿瘤细胞排列呈条索状、小梁状;D示胞质丰富嗜酸性实性区域;E示胞质透亮实性区域;F示胞质丰富嗜酸性实性区域(高倍);G示胞质透亮实性区域(高倍);H示肝细胞癌样结构;I示部分区域呈腺样结构;J示嗜酸性小体。
(3)免疫组化
阳性:AE1/AE3、EMA、CK7、LeuM1、AFP、Hepar-1;
阴性:Vim、α-inhibin、Calretinin、CD10、CD99、HMB45、S100、A103ER、AR、WT1、PAX8、HNF1β、CgA、HCG、CEA。
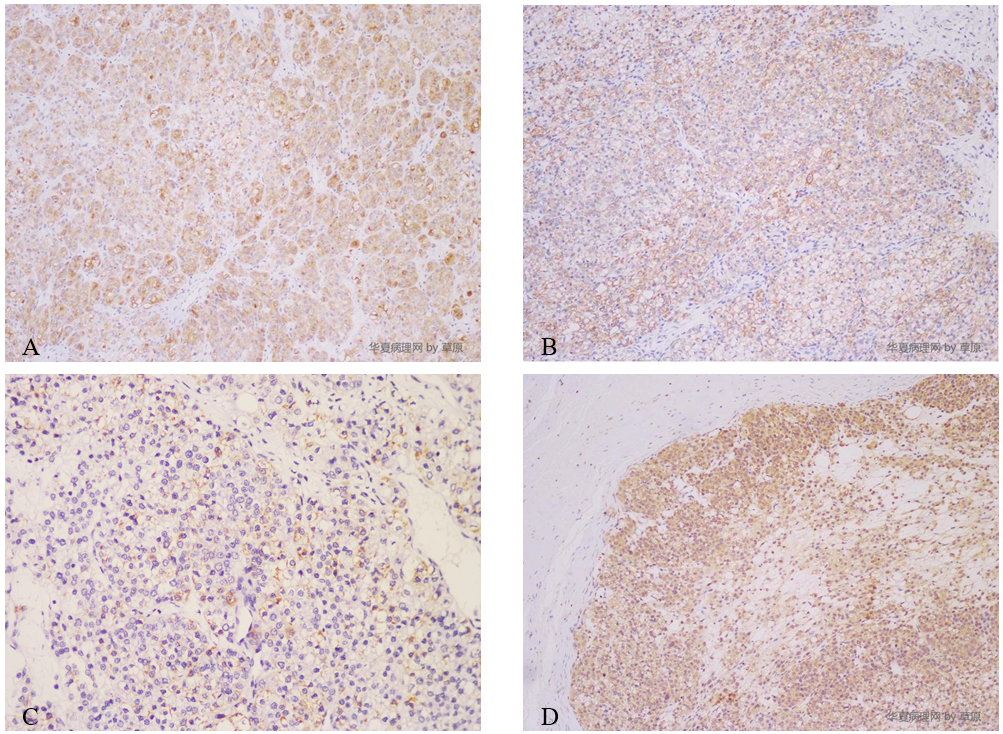
图3 卵巢肝样癌免疫组织化学。EMA阳性(A)、CK7阳性(B)、Hepar-1阳性(C)、AFP阳性(D)。
【讨论】
卵巢肝样癌(hepatoid carcinoma of the ovary,HCO)是指原发于卵巢、形态学上与肝细胞性肝癌和胃的肝细胞样癌相似且AFP阳性的肿瘤。卵巢肝样癌非常罕见,1987由Ishikura和Scully[1]首次描述并命名,之后国内外文献报道仅20余例,其中1例发生于35岁怀孕女性[2]。2003年WHO乳腺与女性生殖器官肿瘤病理学和遗传学分类中将其列为杂类肿瘤,ICO-D编码为8576/3。
HCO主要发生于绝经期后妇女,文献记载发病年龄35~78岁,平均年龄为56.9岁,偶见于生育期年龄的患者。主要症状多为与盆腔包块相关的非特异性症状,如盆腔内肿物,伴或不伴有疼痛、腹水、恶病质等,文献也偶有报道术前患者血清AFP及CA125值升高。
HCO多数累及单侧卵巢,体积变化较大,直径4-20 cm不等,呈卵圆形或不规则形,表面呈结节状,切面以实性或囊实性为主,分布不均,常伴有出血、坏死。在一些甲醛固定的标本中局部呈绿色,提示为胆汁[3]。
镜下示肿瘤细胞排列成片状、条索状或小梁状,细胞边界清晰,大小较均匀一致,呈多角形或卵圆形不等,富含嗜酸或透明胞质;核圆形或卵圆形、居中,核仁明显,核分裂象可见,有时众多可达10-50P/10 HPF,常有病理性核分裂象;在肿瘤的某些区域核的多形性可能相当显著,且可见到多核瘤巨细胞;肿瘤实质内常具有放射状血窦,颇似肝细胞癌排列方式,肿瘤细胞内、外可见PAS 抗消化阳性嗜酸小体和Hall染色阳性的胆色素,常伴有出血及坏死灶,有些病例混杂腺体衬覆柱状或立方上皮成分。部分病例具备典型肝细胞癌特征,呈板层样排列、癌细胞分泌黏液及胆色素。
HCO偶尔可以伴发浆液性腺癌或其他类型的卵巢表面上皮-间质肿瘤,也可以伴发性索-间质肿瘤,D'Antonio A等[6]报道了一例HCO伴Sertoli细胞肿瘤。
组织化学染色,部分病例中肿瘤细胞黏液卡红染色阳性,Hall胆色素染色阳性,嗜酸小体PAS 染色阳性。免疫组织化学染色,全部病例癌细胞AFP均应呈阳性表达,否则诊断不能成立。Senzaki[4]为进一步确定本癌有向肝细胞分化的功能,检测了AFP及PIVKA2 Ⅱ均呈阳性表达。一般CK7、8、18 及CA125呈阳性表达,提示本癌存在卵巢表面上皮癌成分。Sung JH等[5] 于2013年报道了世界首例具有HCO的典型组织学特征而AFP免疫组织化学染色阴性且血清AFP水平正常。
HCO应与具有肝样结构的卵黄囊瘤、类固醇细胞肿瘤、透明细胞癌、转移性肝细胞癌等鉴别,详见专家点评部分。
HCO为高度恶性肿瘤,预后极差,大多数患者于2年内死于肿瘤扩散。文献随访的12例患者中,7例于初诊后4个月-5年内死亡,2例在6-7个月后复发,范嫏娣[2]等报道的2例中1例术后1年死于肿瘤扩散,Ishikura等1987年报道的1例经术后盆腔放疗后存活2年。
【回帖精选】
1、www810910(3楼)回复:
诊 断:(右侧卵巢)考虑非特异性类固醇细胞瘤。
诊断依据:
1)、临床资料:非特异性类固醇细胞瘤多发生于育龄妇女,尤其是20-30岁,绝经后罕见,但也有文献报道;40%患者有渐进性男性化,少数有雌激素升高症状。本例患者,女,63岁,以“绝经10年后阴道出血半月,腹胀不适1周、加重2日”就诊;盆腔MRI示盆腔包块,腹水形成,倾向附件来源肿瘤;予剖腹探查术:术中见腹腔暗红色积血2400ml,右侧卵巢增大呈12*13*8cm,实性,分叶哑铃状,包膜色灰白,局部破裂伴活动性出血,余未见明显异常,行“全子宫+双附件+大网膜+阑尾”切除术。
2)、大体观察:几乎所有肿瘤都为单侧发生,瘤体一般为球形,少数可呈分叶状,界限清楚,多为实性,可局灶变性形成囊性变;瘤体大小不等,平均8.4cm;肿瘤颜色因瘤细胞内脂质和脂色素含量多少而异,从浅黄到棕红不等,较大肿瘤可有坏死、出血。本例送检分叶状肿块,大小16.5*12.5*6cm,呈膨胀性生长挤压周围组织(图1),界清,切面淡黄灰红色,多结节状,部分区囊性变,内含粘液,质中;附输卵管及另送全子宫左附件标本,未及肿块。
3)、镜下观察:低倍镜示肿瘤细胞弥漫排列呈片状、巢状或条索状,局部区域可见腺样结构,肿瘤细胞周边的间质细胞稀少,主要为薄壁窦状血管;高倍镜示肿瘤细胞密集,圆形或多边形,边界清楚,细胞大小较为一致,细胞胞质中等或丰富,呈嗜酸性颗粒状或透明空泡状,部分呈泡沫状;细胞核呈圆形或卵圆形,大小略为不一,核膜略不规则,染色质稍粗,染色偏深或呈空泡状,部分细胞可见居中核仁,核分裂相少见。
4)、免疫组化:α-inhibin、calretinin、Ckpan、EMA、vimentin、cD99、 ER、PR等。
鉴别诊断:
1)间质黄体瘤:肿瘤体积较小,直径0.5~3 cm。主要由结节状黄素化问质细胞构成,细胞形态酷似黄体细胞,核无异型性,瘤周常有卵巢间质包绕。
2)莱迪细胞瘤:主要位于卵巢门或卵巢系膜区及卵巢髓质,体积常较小,大部分病例可见典型的Reinke结晶。
3)透明细胞癌:除了片状排列外,可见其他管囊状、乳头状结构,组化染色示瘤细胞内糖原多,脂质少。
非特异性类固醇细胞瘤的恶性率不等,恶性者年龄往往较大、瘤体较大核分裂像多于2/10HPF,坏死、出血及核异型与恶性病程有关,但只有出现局部侵犯才能从形态学判读为恶性;本例根据病史、镜下形态倾向于良性非特异性类固醇细胞瘤的诊断,以上分析不当的地方敬请各位老师同行批评指正!
2、youxueye (51楼)回复:
诊 断:(右侧卵巢)肝样腺癌。
诊断依据:
患者老年女性,卵巢单侧肿瘤,大体呈分叶多结节状,伴囊性变,似有粘液;镜下肿瘤细胞呈假腺样、梁状、片巢状排列,细胞多角形,胞浆丰富,嗜酸或透亮,核位于中央,圆形或椭圆形,核膜清晰,可见明显核仁,部分区域可见瘤巨细胞;部分腺腔内可见嗜酸小体;细胞巢间见丰富血窦样裂隙。形似肝细胞性肝癌,故考虑。可行免疫组化AFP、CEA、CA125、ACT、AAT、PAS等协助诊断。
卵巢肝样腺癌是原发于卵巢,其组织学特征与肝细胞性肝癌类似的AFP阳性的肿瘤。本病较为罕见,主要发生于绝经期后妇女,平均年龄56.9岁,年龄跨度35-78岁,主要症状多为与盆腔包块相关的非特异症状,如盆腔内肿物或伴有疼痛、腹水和恶病质,血清AFP会有升高,多数病例CA125升高;大体肿瘤多为单侧,体积大小变化较大,直径从4-20cm不等;卵圆形或不规则,表面多呈结节状,切面囊实性兼有,常伴有坏死及出血;镜下癌细胞排列成片状、条索状、小梁状,其体积较为均匀一致,成多角形或卵圆形,具有丰富嗜酸性胞质,核圆形或卵圆形,位于中央,核仁明显,细胞边缘清晰,常伴有数量不等的单或多核瘤巨细胞,其组织结构与肝细胞癌相似;癌细胞内外可有数量不等的PAS抗消化阳性的嗜酸小体,部分细胞可含有粘液;核分裂像可见。免疫组化大部分成AFP和维生素K缺乏的抗拮抗剂II诱导蛋白阳性表达,提示其向肝细胞分化。AFP,ACT和CEA多数阳性表达,50%的病例CA125阳性,HCG在少数病例中亦有阳性表达。
鉴别诊断:
1)、卵巢卵黄囊瘤肝样型:多为幼儿或青少年,除肝细胞样分化外,还可见卵黄囊结构或内胚窦瘤结构。
2)、卵巢类固醇细胞肿瘤:有些类固醇细胞肿瘤胞质丰富且嗜酸,与肝癌相似,但其多显著异型性,组化AFP阴性,临床可有内分泌异常现象。
3)、转移性肝细胞癌:多有肝细胞癌病史,年龄多在40岁以下,有相应的症状及体征。
4)、卵巢未分化癌:癌细胞较小,AFP阴性。
【提供者单位及姓名】上海复旦大学肿瘤医院病理科 徐晓丽
【专家点评-徐晓丽老师】
IHC results:
Positive:AE1/AE3、EMA、CK7、LeuM1、AFP、Hepar-1;
Negative:Vim、α-inhibin、Calretinin、CD10、CD99、HMB45、S100、A103ER、AR、WT1、PAX8、HNF1β、CgA、HCG、CEA。
Discussion(讨论):
1、Rare primary ovarian carcinoma(罕见的原发性卵巢癌)。
2、Introduced by Ishikura and Scully in 1987 (Ishikura 和 Scully 在 1987年首次介绍)。
3、occurs almost exclusively in postmenopausal famales(几乎总是发生于绝经后妇女)。
4、Elevation of serum AFP and serum CA125(血清AFP和血清 CA125都升高)。
5、Most of the hepatoid carcinoma cases were clinically advanced tumors(大多数肝样癌病例为临床晚期)。
6、Large, polygonal, round or oval cells, abundant amounts of eosinophilic cytoplasm, distinct cell borders resembling hepatocellular carcinoma(细胞大、多角形、圆形或卵圆形,胞质丰富、嗜酸性,细胞边界清楚,类似肝细胞癌)。
7、Arranged in sheets, trabecular pattern(排列成片状、小梁状结构)。
8、May combine with other surface epithelial carcinomas, sex cord stromal tumor(可合并其他表面上皮癌、性索-间质肿瘤)。
9、Metastasis to lymph node, spleen, liver, lung, soft tissue, etc(转移到淋巴结、脾、肝、肺、软组织等)。
10、most likely a variant of common epithelial carcinoma by a process of neometaplasia or transdifferentiation(很可能是普通上皮癌的一种亚型,发生了肿瘤性化生或转分化)。
Differentiated diagnosis(鉴别诊断):
1、Steroid cell tumor /lipid cell tumor (类固醇细胞瘤/脂质细胞肿瘤)
1)、average age 43 (2-80) years(平均年龄 43 (2-80) 岁);
2)、average size 8.4cm, well circulmscribed, lobulated or multinodular, solid, yellow to brown (平均大小 8.4cm,边界清楚,分叶状或多结节状,实性,黄色到褐色);
3)、diffuse or cords pattern, >90% unilateral(弥漫或条索状结构,>90%为单侧性);
4)、medium to large cells with distinct cell membranes(中-大细胞,细胞膜清楚);
5)、granular eosinophilic or vacuolated cytoplasm(颗粒性嗜酸性胞质或空泡状胞质);
6)、round and centrally placed nucleus with single nucleolus(核圆形,中位,有单个核仁);
7)、frequently no cytologic atypia and<2 mictoses/10HPF(通常没有细胞学异型性,核分裂<2/10HPF);
8)、a delicate fibrovascluar stroma(纤细的纤维间质);
9)、malignant: 43%, >2 mitoses/10HPF, necrosis, >7cm, hemorrahage, high-grade nuclear atypia(恶性:43%, 核分裂>2/10HPF,坏死, >7cm,出血, 高度核异型性);
IHC features(免疫组化特征):
1)、Inhibin and calretinin + (Inhibin+,calretinin +);
2)、A103, CD10, CD56 and vimentin frequently+ (A103, CD10, CD56 和
vimentin 通常 +);
3)、S100 and HMB45 + in some cases(部分病例S100 +和 HMB45 +);
4)、Some tumors may stain for CK or CD99(部分肿瘤表达CK 或 CD99);
2、HCC metastasis(HCC 转移)
1)、high risk of HCC: chronic hepatitis B or hepatitis C infection, liver cirrhosis(HCC高危因素:慢性乙肝或丙肝,肝硬化);
2)、in china, young patients with HBV+ (中国,年轻患者伴HBV+);
3)、Liver lesions (肝脏发现疾病);
4)、Bilateral ovary (累及双侧卵巢);
5)、bile ductal differentiation (肝细胞分化);
6)、IHC: CK7-, EMA-,Hepar-1+, Arg+, AFP+。
3、Clear cell adenocarcinoma(透明细胞腺癌)
1)、Solid pattern, always show other architectural patterns, tubulocystic, glandular and papillary, hobnail cells are common (透明细胞腺癌:实体型,通常显示其他结构:管囊型、腺体和乳头,常见靴钉细胞);
2)、Clear or eosinophilic cytoplasm (透明或嗜酸性胞质);
3)、Adenofibromatous background and/or endometriosis (腺纤维瘤背景和/或子宫内膜异位症);
4)、IHC: PAX8+, HNF1β+, AFP-, Hepar-1-。
4、Hepatoid Yolk sac tumor( 肝样卵黄囊瘤)
1)、Mostly young (<20 yrs) (大多数年轻 ,<20 yrs);
2)、The most common is reticular and microcystic pattern (最常见网状和微囊结构);
3)、Pseudopapillary, hepatoid, glandular patterns (假乳头、肝样和腺样结构);
4)、Solid pattern, may predominate in recurrences (复发时可能主要为实性结构);
5)、Primitive cells display nuclei with prominent nucleoli and brisk mitotic activity (原始细胞核仁明显,核分裂活跃)。
感谢上海复旦大学肿瘤医院病理科徐晓丽老师提供病例,个人查阅文献整理相关内容,仅供参考学习!不当之处敬请批评指正!
【参考文献】
[1]Ishikura H, Scully RE. Hepatoid carcinoma of the ovary: a newly described tumor [J]. Cancer, 1987, 60(11): 2775-2784.
[2]范嫏娣,冬国友,王展宏.卵巢肝样癌的临床病理特点[J].诊断病理学杂志,2008,15(2):103-106.
[3]陈乐真.妇产科诊断病理学.北京:人民军医出版社,2010年:398-399.
[4]Senzaki H, Kiyozuka Y, Mizuoka H, et al. An autopsy case of hepatoid carcinoma of the ovary with PIVKA2 Ⅱ production:immunohistochemical study and literature review [J]. Pathol Int, 1999, 49(2): 164-169.
[5]Sung JH, Kim TH, Park HG, et al. Hepatoid carcinoma of the ovary without staining for alpha-fetoprotein [J]. Obstet Gynecol Sci, 2013, 56(1):41-44.
[6]D'Antonio A1, De Dominicis G, Addesso M, et al. Hepatoid carcinoma of the ovary with sex cord stromal tumor: a previously unrecognized association [J]. Arch Gynecol Obstet, 2010, 281(4):765-768.








 图2 卵巢肝样癌。A、B示肿瘤细胞排列呈实性片状、团巢状;C示肿瘤细胞排列呈条索状、小梁状;D示胞质丰富嗜酸性实性区域;E示胞质透亮实性区域;F示胞质丰富嗜酸性实性区域(高倍);G示胞质透亮实性区域(高倍);H示肝细胞癌样结构;I示部分区域呈腺样结构;J示嗜酸性小体。
图2 卵巢肝样癌。A、B示肿瘤细胞排列呈实性片状、团巢状;C示肿瘤细胞排列呈条索状、小梁状;D示胞质丰富嗜酸性实性区域;E示胞质透亮实性区域;F示胞质丰富嗜酸性实性区域(高倍);G示胞质透亮实性区域(高倍);H示肝细胞癌样结构;I示部分区域呈腺样结构;J示嗜酸性小体。








共0条评论