[导读] 编译整理:强子
肺癌主要病理类型为非小细胞肺癌(non-small cell lung cancer,NSCLC),约占全部肺癌的85%。目前靶向治疗已成为NSCLC患者治疗的重要组成部分,但前提是该病例具有相应的药物靶点,具体如ALK重排、EGFR突变、PD-L1表达等。NSCLC中ROS1重排的比例约为1-2%,大部分重排发生于不同染色体间,罕见情况下发生于同一染色体内;对应的融合基因有多种。具有ROS1重排的患者对于克唑替尼及其他ROS1相关治疗效果较好。2018年美国病理学家协会(College of American Pathologists,CAP)、国际肺癌研究协会(International Association for the Study of Lung Cancer)、美国分子病理学会(Association for Molecular Pathology)相关指南中已将ROS1确定为所有肺腺癌患者必需检测的项目之一。
从检测角度来说,有多种方法可用于确定ROS1状态。目前的金标准是荧光原位杂交(fluorescence in situ hybridization,FISH)。二代测序(next generation sequencing,NGS)也可用于ROS1融合检测,但美国FDA仅批准了一家公司的相关技术;第三种检测方法为逆转录-聚合酶链反应(reverse transcription–polymerase chain reaction,RT-PCR);第四种检测方法即临床病理常用的免疫组化,但这一方法检测的并非肿瘤细胞的遗传学改变、而是检测相关蛋白。这些检测方案中,目前商用的免疫组化ROS1检测一方面并无标准化的推荐检测方案,另一方面也无免疫组化结果与其他检测方案结果的大规模比较。有鉴于此,美国罗氏(Roche)公司Huang等人进行了相关比较,文章发表于CAP官方期刊《Archives of Pathology & Laboratory Medicine》
研究内容
该研究共计纳入122例既有免疫组化、又有FISH检测的标本。免疫组化检测所用抗体为克隆号SP384的ROS1抗体(Ventana公司产品),在罗氏公司的BenchMark免疫染色平台按照推荐染色步骤进行检测,显色方案为DAB试剂盒(Ventana公司产品)。相关对照及具体步骤等详见原文。122例标本的FISH检测结果有81例为Cancer Genetics Incorporated公司(已通过美国临床实验室改进法案修正案评审)所做,36例来自病理会诊报告,5例为US Biomax公司标准的FISH检测方案所做阳性结果。
经由注册病理医师对122例病例进行免疫组化评分,具体积分(H-score)方法为【1×(染色评分为1的细胞比例)+2×(染色评分为2的细胞比例)+3×(染色评分为3的细胞比例)】;且评分者并不知道FISH结果。对细胞核、细胞质、细胞膜均进行相关积分计算。对于ROS1的FISH及免疫组化结果不一者,均进行进一步分子检测,如RT-PCR、RNA的NGS和DNA的NGS。该处的不一致,具体到免疫组化而言是指大于30%的瘤细胞有胞质着色、且着色强度≥2+者视为免疫组化阳性;≤30%的瘤细胞胞质着色、且着色强度≥2+者视为阴性。详见表1。
研究结果
相关病例中ROS1免疫组化阳性大部分位于胞质,极少数位于细胞膜;1例为细胞核着色,且其积分为120。具体着色强度也有一定差异。详见图1、图2。
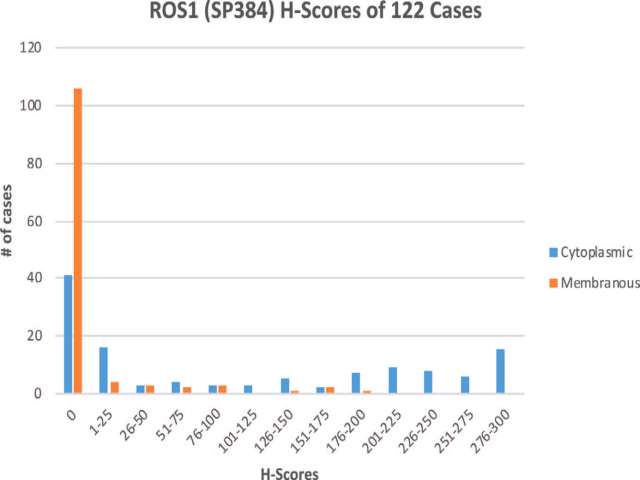
图1. 121例胞质及细胞膜着色病例的ROS1免疫组化积分结果。

图2. ROS1免疫组化着色强度示意图:第一列为阴性,第二列为1+,第三列为2+,第四列为3+。
对免疫组化结果与FISH结果进行分析,可见大于30%的瘤细胞有胞质着色、且着色强度≥2+者与FISH阳性之间的一致性最佳,详见表1。
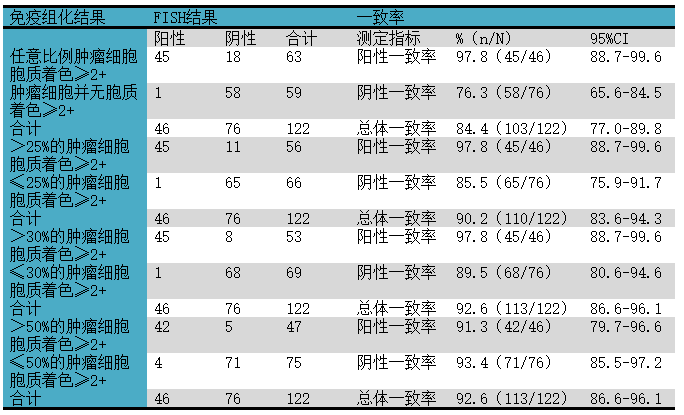
表1. ROS1免疫组化结果(克隆号SP384)与FISH结果统计分析
有9个病例的FISH结果与免疫组化结果之间出现了不一致,8例为FISH-/免疫组化+,1例为FISH+/免疫组化-。对这9个病例进行进一步分子检测的相关结果见表2。具体来说,免疫组化与最终结果一致者2例,免疫组化与最终结果不一致者6例,另有1例因核酸数量不足以进行检测而无最终结果。
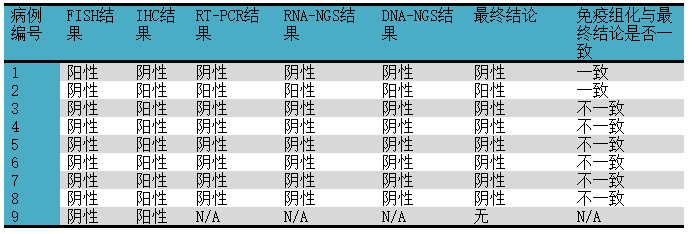
表2.ROS1免疫组化与FISH结果不一致病例进一步分子检测结果
N/A:由于核酸不足以进行检测,所以无结果。
小结
任何检测手段均有其优点及缺点。免疫组化确定分子标记物的主要优点在于便捷、耗时短、花费少,对于阳性率较低的分子标记物来说,可以作为初筛,显著增加分子检测的阳性率。FISH检测如所用探针为断裂探针,则检测融合基因更为特异,不过对于同一染色体内的重排就不是那么敏感了。RT-PCR对于检测特异性融合来说高度敏感,但对于具有诸多融合方式、或者尚未明确的融合来说,就难以检出所有重排可能。NGS由于其高通量,因此相对容易检出所有可能的融合方式,但目前来说耗资不菲、时间漫长。
本研究结果表明,按照本文提出的相关标准,即大于30%的瘤细胞有胞质着色、且着色强度≥2+者视为免疫组化阳性,则克隆号为SP384的ROS1抗体免疫组化检测结果与FISH结果之间高度一致。因此,对于目前正在研究中的诸多ROS1抑制剂来说,该方法可作为蛋白水平ROS1标记的标准检测方案。当然,对于真正临床应用是否可以以此而代替FISH检测,本研究结论尚显稚嫩;要解决这一问题,还需结合相关临床试验才能有真正可靠的结论。
点击下载英文文献
参考文献
Huang RSP,Smith D,Le CH,et al.Correlation of ROS1 Immunohistochemistry With Fusion Status Determined by Fluorescence In Situ Hybridization[J].Archives of pathology & laboratory medicine,2019.
DOI:10.5858/arpa.2019-0085-OA

















共0条评论