本文刊于《中华胃肠外科杂志》2018年第6期,2018,21(6) : 632-636
作者:钮东峰 薛卫成
作者单位:北京大学肿瘤医院暨北京市肿瘤防治研究所病理科 恶性肿瘤发病机制及转化研究教育部重点实验室
摘要
术前新辅助治疗在直肠癌中得到了广泛推广,术后规范化病理评估也逐渐引起广泛的关注。准确的病理学检查在直肠癌的诊治流程中发挥着"承前启后"的作用,既能评判新辅助放化疗及手术切除的效果,又能指导术后辅助治疗和评估患者预后。肿瘤退缩分级(TRG)的病理评估和TNM分期是直肠癌常规病理诊断的基础,与患者的生存预后息息相关。目前,针对新辅助放化疗后TRG评价方法主要有NCCN、AJCC、Becke、Mandard、Dowrak/Rödel、MSKCC及RCRG等标准,但尚无一个公认的最佳标准,实践工作中较常使用的分级为AJCC和NCCN的TRG分级标准。准确进行TRG分级的前提是详细、规范的病理学评估,包括大体标本评估和镜下评估。如何评价新辅助治疗后淋巴结转移灶的治疗反应以及如何提高病理医师间评估的一致性是目前仍待解决的问题。
近年来,随着我国人民生活水平的不断提高,饮食习惯和饮食结构的西化,我国结直肠癌的发病率和死亡率均保持上升趋势。在2012年确诊的全球136万例结直肠癌中,中国新发病例数达到25.3万,占全球结直肠癌新发病例的18.6%[1]。2015年新发病例上升至37.6万,死亡病例达19.1万,发病率和死亡率在所有恶性肿瘤中均位居第5位[2]。
解剖上,直肠上接乙状结肠,下沿肛门,前临子宫、阴道或者前列腺、精囊腺,后靠骶骨和尾骨。与结肠癌相比,因解剖位置、血供、淋巴引流等不同,直肠癌更易侵及盆壁和盆底,且根治性手术受限于骨盆的狭小操作空间,因此,其复发率比结肠癌更高。直肠癌治疗主要依赖于手术切除及放化疗,早期直肠癌(cT1N0M0)行内镜下切除或局部切除;术前分期cT2~4N0~2M0的肿瘤必须行根治性手术切除;T3和(或)N+的可切除直肠癌,推荐术前新辅助放化疗;T4或局部晚期不可切除的直肠癌,必须行新辅助放化疗,治疗后必须重新评价,经多学科讨论,若降低了肿瘤分期或者瘤体大小则行根治性手术切除。直肠癌术前新辅助治疗发挥着越来越重要的作用,可使相当一部分肿瘤发生不同程度的降期,显著降低局部复发率[3]。而术后病理学评估也至关重要,往往与肿瘤的恶性程度、患者的生存预后及后续治疗方案有着密切的关系。
一、 新辅助化疗后病理需要评估的内容
直肠癌的术后,完整规范详尽的病理诊断能够协助临床医生更准确地了解肿瘤的个体生物学特征,并预测患者的预后,协助外科医生评判手术的根治性,协助放疗科医生评估放化疗治疗的敏感性,协助化疗科医生制定术后化疗方案。此外,2011年美国国立综合癌症网(NCCN)指南全面引入了"预后和预测"评估体系,作为手术后判断肿瘤复发可能性以及预测治疗效果和预后的依据,如环周切缘阳性、有脉管浸润及神经周围浸润、新辅助治疗反应差、BRAF基因突变及微卫星稳定等都可以看作是高复发率、预后差的指标,这些指标同样也预示着术后需要更为积极且全面的辅助治疗措施。因此,局部进展期直肠癌,特别是接受新辅助放化疗后的直肠癌,根治术后的样本病理评估对判断预后及指导后续治疗具有至关重要的作用。
1.标本的肉眼评估:
直肠标本离体30~60 min内,沿肿瘤对侧剪开肠管进行标记、切开、固定等初步处理,将肠管铺平固定于木板或石蜡板上,标本完全浸没于4%甲醛溶液中充分固定,标本的固定时间为8~48 h。取材时记录肿瘤的特征,包括大体类型(蕈伞型、溃疡型及浸润型)、部位、大小、数目、浸润深度、肿瘤与两侧切缘以及环周切缘的距离。新辅助治疗效果较好者,标本无明确肿块,病变处仅存瘢痕,见图1。建议瘢痕处全部取材,还需要描述周围肠黏膜的改变,如溃疡、水肿,往往治疗反应较好的肿瘤,清扫淋巴结时会发现肠周围脂肪组织会变韧。切除标本若包含肛管和肛周皮肤,应描述肿瘤有无累及,皮肤有无改变,如湿疹样改变和息肉形成。淋巴结取材应按淋巴引流方向进行分组,一般分为肿块旁淋巴结、肠系膜淋巴结和尖淋巴结,记录淋巴结大小和数目。美国癌症联合委员会(AJCC)和NCCN都规定淋巴结检出数至少12枚,接受过术前治疗的患者淋巴结可以低于12枚[4]。
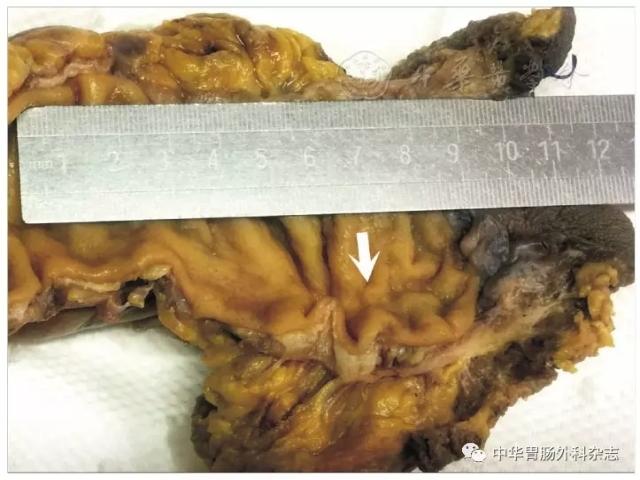
图1 直肠癌新辅助治疗后术后大体标本,可见肿物完全退缩,形成瘢痕(箭头)
2.标本的镜下评估内容:
病理报告镜下内容应包括组织学分级、浸润深度、有无脉管和神经束浸润、切缘情况(包括近切缘、远切缘、环周切缘)、淋巴结转移情况(包括具体分组)、癌结节情况、新辅助治疗后肿瘤退缩分级(tumor regression grading,TRG)、淋巴结转移灶有无化疗反应及ypTNM分期。其中TRG分级及ypTNM分期与患者后续治疗密切相关,临床最为关心。
二、 新辅助放化疗后肿瘤退缩分级的病理学评估
患者接受新辅助治疗后,肿瘤细胞退缩可出现多种组织学改变,如肿瘤细胞坏死凋亡、纤维组织增生、炎症细胞浸润、泡沫细胞聚集、无细胞黏液产生并形成黏液池以及钙化灶形成等,见图2。但不是所有的肿瘤治疗后都会产生以上各种退缩反应,纤维组织增生和炎症细胞浸润是最常见的组织学退缩改变,为了评估肿瘤临床治疗效果,肿瘤退缩需定量分级。TRG是对新辅助化疗后切除的肿瘤进行病理学评估,以明确化疗或靶向药物对肿瘤的治疗效果的定量分析,并预测患者术后复发转移情况。其最早被用于食管癌同期放化疗后的疗效评估[5];后逐渐用于直肠癌的疗效评估。现行对放化疗后样本的评估主要依据残留肿瘤成分以及纤维化的比例来进行病理学退缩的分级。目前针对新辅助放化疗后TRG评分方法主要有NCCN、AJCC、Becker、Mandard、Dowrak/Rödel、期隆-凯特琳癌症中心(MSKCC)及直肠癌消退分级(RCRG)等标准[4,5,6,7,8,9,10],见表1。


图2 直肠癌新辅助化疗后肿瘤退缩反应组织学改变 2a.肿瘤细胞坏死凋亡;2b.纤维组织增生;2c.炎症细胞浸润;2d.泡沫细胞聚集;2e.无细胞黏液产生并形成黏液池;2f.钙化灶形成
Mandard分级标准于1994年提出并应用于食管癌同期放化疗后疗效的病理学评估,将反应分级分为5级:TRG1,无癌细胞残留;TRG2,癌细胞极少量残留;TRG3,纤维化反应超过癌细胞;TRG4,癌细胞超过纤维化反应;TRG5,几乎无反应[5]。后将TRG2和TRG3合并为TRG2,TRG4和TRG5合并为TRG3,即形成三级标准[7]。Becker三级分级标准与Mandard三级分级极为相似,Becker分级中的TRG1b归入TRG2,即为Mandard三级分级[8]。Dowrak/Rödel五级标准是以纤维化区域25%和50%为节点,分为TRG0~4级,无反应为TRG0级,< 25%的肿瘤区域纤维化为TRG1级,25%~50%的肿瘤区域纤维化为TRG2,>50%的肿瘤区域纤维化为TRG3级,完全缓解为TRG4级[9]。与Dowrak/Rödel三级标准类似的还有MSKCC提出的标准,以85%为分级点,分为TRG1~3级[10]。2011版NCCN指南四级评估标准中,0级表示无癌细胞残留,1级表示仅见单个癌细胞或癌细胞簇,2级为纤维化反应超过残余癌细胞,3级为几乎无纤维化,可见大片癌残留。AJCC四级分级中TRG2级较NCCN 2级更为宽泛,囊括了AJCC-TRG3级的一部分。各种TRG分级对于患者生存预后有独立预测作用,疗效反应佳的患者预后较好,较少发生局部复发、远处转移,总生存期也更长[3]。例如,Dworak/Rödel五级分级可以判断局部晚期直肠癌患者术前放化疗患者预后,TRG 4、3、2、1和0级患者3年无病生存率分别为100%、85%、82%、66%和33%(P < 0.01)[11]。有研究通过对各系统的评价结果进行比较,发现AJCC-TRG系统要优于其他系统,可以更准确地预测直肠癌远处转移的发生,是总生存、无病生存、无局部复发生存及无远处转移生存的预后影响因素[12]。但总体来说,目前仍无一个公认的最佳TRG评分方法,实践工作中较常使用的分级为AJCC和NCCN的TRG分级标准。
三、新辅助放化疗后评估肿瘤ypTNM分期
AJCC第八版(2017年)结直肠癌TNM分期中,T代表浸润深度、N代表检出及转移淋巴结数目、M代表远处转移[4]。直肠癌T分期因其解剖结果的特殊性,与结肠癌存在着较大的差异。直肠根据与盆底腹膜反折的关系,分为上、中、下3段,分别被划分为腹膜内位、腹膜间位、腹膜外位器官。上段延续乙状结肠;中段直肠前壁有腹膜覆盖,而侧壁和后壁由脏层筋膜所覆盖;下段直肠远侧位于肛管内,其固有肌层内环行部分向肛侧延续形成的肛门内括约肌,故组织学为平滑肌,外侧包绕的外括约肌则为骨骼肌。上段直肠癌T分期与结肠癌相同,而中下段直肠癌的则因其特殊的解剖结构较为复杂:T2为癌累及固有肌层或其向下延伸的内括约肌;T3为累及中段的直肠系膜,以及下段的外括约肌,但未侵透;T4a为累及直肠中段前壁浆膜,而无浆膜覆盖的下段不存在T4a分期;T4b期则为侵透中段直肠系膜,以及侵及下段的肛提肌或侵透外括约肌达肛周脂肪组织,肿瘤位于肛管内累及肛提肌要引起注意。由于肛提肌和外括约肌组织学上均为骨骼肌,镜下组织学是无法分辨的,因此,病理取材时要注意大体的仔细检查,临床也要详细标注说明。
N分期中,Nx为区域淋巴结不能评估;N0无区域淋巴结转移;N1可分为N1a(仅1枚区域淋巴结转移)、N1b(2~3枚区域淋巴结转移)及N1c(肿瘤沉积);N2可分为N2a(4~6枚区域淋巴结转移)和N2b(7枚或更多区域淋巴结转移)。
M分期中,M0为影像学无远处转移,例如:在远隔部位或器官无肿瘤证据(此分类不由病理医师评估);M1分为M1a(一个部位或器官转移,无腹膜转移)、M1b(两个或以上部位或器官转移,无腹膜转移)和M1c(腹膜表面转移,伴或不伴其他部位或器官转移)。
四、仍未解决的问题
肿瘤退缩评估都是通过肿瘤原发灶纤维化程度和残余肿瘤的比例进行分级,无论以上叙述的哪一种评分标准都只考虑了肿瘤原发灶的退缩情况,对于伴有淋巴结转移灶者,转移癌的退缩情况常常被忽视。而淋巴结转移情况是TNM分期的重要组成部分,与患者的预后密切相关,ypⅡ期患者的5年无病生存率明显高于ypⅢ期患者[13]。因此,一些研究提出了反映淋巴结转移情况的新的分级系统(new tumor regression grade,NTRG),同样根据淋巴结纤维化程度和残余肿瘤的百分比定义不同的分级标准[13]。研究发现,NTRG是影响新辅助放化疗后直肠癌患者5年局部复发率、远处转移率和无病生存率的独立危险因素[14,15]。2017版AJCC以及我国结直肠癌诊疗规范(2017年版)都要求病理报告中说明新辅助放化疗术后结直肠癌的淋巴结转移灶的化疗反应,但具体如何量化评估未做规定[2,4]。淋巴结转移灶新辅助治疗后的组织学改变较少产生纤维化,故淋巴结癌转移灶的评估不能完全套用原发灶TRG评估标准。此外,肿瘤细胞退缩出现的组织学改变除最重要的纤维化外,还有炎症细胞浸润、泡沫细胞聚集、无细胞黏液产生以及钙化灶形成。为了提高TRG分级的客观性,如果在TRG病理评估中增加这些评估指标,势必会更加详尽地了解肿瘤的治疗反应效果。但融入了这些指标,极有可能使病理医师间评估的可重复率下降。
脉管癌栓和神经侵犯在各恶性肿瘤中代表肿瘤的侵袭性和预后[16]。直肠癌也不例外,我国结直肠癌诊疗规范(2017年版)规定要在病理报告中体现神经侵犯和脉管侵犯情况(V代表血管,V1为镜下血管浸润,V2为肉眼血管浸润;L代表淋巴管),并建议尽量区分血管与淋巴管侵犯,但没有对侵犯情况做出具体量化[2]。日本"大肠癌临床病理规范(第8修订版)"中对血管癌栓及淋巴管癌栓进行了量化分级,血管癌栓分级为V0(无)、V1(轻度)、V2(中度)和V3(重度),淋巴管癌栓分级为ly0(无)、ly1(轻度)、ly2(中度)及ly3(重度)[17]。由于没有对各侵犯程度做出具体量化,在实际工作中,病理医师之间的主观性存在较大差异,评估结果也存在着较大的差异。因此,对一些标准的规定,要尽可能详细数字化,尽量避免使用少量、大量癌细胞退缩等用语;但对于阈值范围十分窄的也不可取,如TRG1级为癌细胞残留5%~10%,病理医师之间很难达到较高的一致性。近年来,电子信息化取得了巨大的进步,人工智能技术逐渐应用于各行各业,人工智能与医学影像学结合在图像识别领域不断取得了突破性进展。如果这些技术应用于直肠癌新辅助化疗后病理学手术切除标本的TRG分级,并可融入其他化疗反应组织学改变及各个预后指标的评估,势必会更客观地反应直肠癌新辅助后的疗效,以避免病理医师间评估的差异性。
五、未来展望
对于局部进展期直肠癌,术前新辅助放化疗联合全直肠系膜切除术仍然是目前最常用的治疗方式。术前临床影像学分期诊断是科学制定直肠癌初始治疗方案的先决条件,术后规范化的病理诊断评估则成为评价新辅助治疗疗效、指导后续辅助治疗、判断预后的重要依据。新辅助直肠癌病理学评估的一些标准尚存在问题,希望病理医务工作者在今后的工作中不断进步,更好地配合临床,给其提供更多、更有意义的病理信息,更好地服务于直肠癌患者。
参考文献(略)
















共0条评论