[导读] 本文作者:宁青青
血管免疫母细胞性T细胞淋巴瘤
☆成熟T/NK细胞淋巴瘤
T细胞幼淋巴细胞白血病
T细胞大颗粒淋巴细胞白血病
慢性NK细胞淋巴增殖性疾病*
侵袭性NK细胞白血病
儿童系统性EBV阳性T细胞淋巴细胞增生性疾病
水疱痘疮样淋巴瘤
成人T细胞白血病/淋巴瘤
结外NK/细胞淋巴瘤(鼻型)
肠病相关性T细胞淋巴瘤
单型上皮肠道T细胞淋巴瘤*
消化道惰性T细胞淋巴细胞增生性疾病*
肝脾T细胞淋巴瘤
皮下脂膜炎样T细胞淋巴瘤
蕈样肉芽肿
Sezary综合征
原发皮肤CD30阳性T细胞淋巴细胞增生性疾病
△淋巴瘤样丘疹病
△原发皮肤间变性大细胞淋巴瘤
原发皮肤γδT细胞淋巴瘤
原发皮肤侵袭性亲表皮CD8阳性细胞毒性T细胞淋巴瘤*
原发皮肤肢端CD8阳性T细胞淋巴瘤*
原发皮肤CD4阳性小中T细胞淋巴细胞增生性疾病*
外周T细胞淋巴瘤,非特指性(NOS)
血管免疫母细胞T细胞淋巴瘤
滤泡T细胞淋巴瘤*
伴TFH表型的结周T细胞淋巴瘤*
间变性大细胞淋巴瘤,ALK阳性
间变性大细胞淋巴瘤,ALK阴性
乳房植入物相关的间变大细胞淋巴瘤*
☆成熟T细胞和NK细胞肿瘤分类更新
1、儿童系统性EBV阳性T细胞淋巴瘤(更名)
2、 系统性慢性活动性EBV感染, T和NK细胞型(新增)
3、种痘水泡样淋巴增殖性疾病(更名)
4、严重蚊虫叮咬过敏反应(新增)
5、肠病相关T细胞淋巴瘤(重新归类)
6、单形性亲上皮性肠道T细胞淋巴瘤(重新归类)
7、胃肠道惰性T细胞淋巴增殖性疾病(新增)
8、原发性皮肤末稍CD8+ T细胞淋巴瘤(新增)
9、原发性皮肤CD4+小至中等大小T细胞增殖性疾病(更名)
10、滤泡性T细胞淋巴瘤(新增)
11.伴滤泡辅助T细胞表型结内外周T细胞淋巴瘤(新增)
12、乳腺植入相关性间变性大细胞淋巴瘤(新增)
外周T细胞淋巴瘤( PTCL)是指起源于胸腺后成熟T细胞/NK细胞的肿瘤,较为罕见,有高度异质性,占非霍奇金淋巴瘤(NHL)的10%~ 15%,PTCL由外周T细胞淋巴瘤(PTCL), 非特指性、血管免疫母细胞性T细胞淋巴瘤(AITL)、间变性大细胞淋巴瘤(ALCL), ALK阳性、ALCL, ALK阴性、肠病相关性T细胞淋巴瘤(EATL)、单型性亲上皮性肠道T细胞淋巴瘤(MEITL)、伴有TFH表型的淋巴结外周T细胞淋巴瘤(PTCL,TFH)、滤泡T细胞淋巴瘤(FTCL)多种亚型组成。其中AITL是PTCL的一种常见亚型。
一、定义
血管免疫母细胞性T细胞淋巴瘤(AITL)是一种起源于滤泡辅助T细胞的外周T淋巴细胞肿瘤。临床上呈系统性疾病过程,全身多器官、组织受累,以瘤细胞的多形性,高内皮血管和树突状网状细胞的明显增生为组织病理学特征。
二、发病机制
AITL的发病机制尚不明确,多数学者认为其与EB病毒感染密切相关,EBV阳性患者有发展为B细胞淋巴瘤的可能,特别是发展为弥漫性大B细胞淋巴瘤。
三、临床特征
AITL的中位发病年龄在62~68岁。AITL典型的临床表现是全身多发外周淋巴结肿大,常伴有B症状(发热、盗汗、体重减轻),结外症状以皮疹、肝脾肿大较常见,骨髓侵犯也比较常见(约30%~70%),胃肠道、肺、神经系统侵犯则相对罕见。此外,患者可伴有自身免疫紊乱,表现为Coombs试验、多克隆免疫球蛋白血症和嗜酸性粒细胞增多,部分可见类风湿因子、抗核抗体阳性等。
四、组织病理学
(1) 淋巴结结构至少部分破坏。
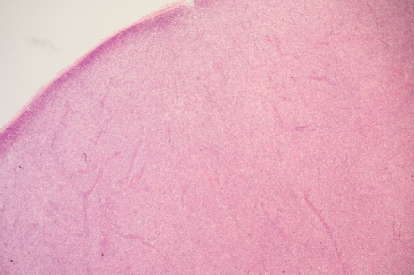
(2)高内皮静脉增生(经常不规则)

(3) 成簇的透亮细胞
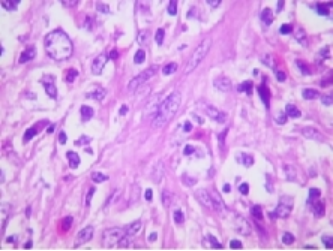
(4) 背景:多种炎细胞反应(淋巴细胞,组织细胞,浆细胞,嗜酸性粒细胞)
病变的早期淋巴滤泡常增生,随着肿瘤的进展,淋巴结结构不同程度地被破坏,但被膜下窦常见。滤泡间区增生,高内皮血管呈树枝状增生,遍布于病变的淋巴结。淋巴滤泡套区细胞消失,仅见少量滤泡中心细胞和增生的树突状网状细胞,即所谓生发中心“烧光"(burn out) 现象。可见不等量的嗜酸性无结构物质沉着。多数瘤细胞体积小或中等大小,胞质淡染或透明,细胞核为圆形、卵圆形或不规则形,核染色质细腻而均匀分布。瘤细胞多呈小簇状分布,沿增生血管分布,在低、中倍镜下呈特征性的斑驳样图像。常可见一些胞质嗜碱性的免疫母细胞呈簇状分布或存在于血管内。可见R-S样细胞(免疫表型检测呈CD30+、CD15+、CD20+/-、EBER+)。易见核分裂象。随着肿瘤的进展,瘤细胞的数量逐渐增加,成片分布。该肿瘤的形态学特征之一是滤泡外高内皮血管周围树突状细胞增生而形成粉染的细胞稀疏(hypocellular)区。背景中还可见不等量的浆细胞、嗜酸性粒细胞和组织细胞散在分布,部分病例可见上皮样细胞簇或肉芽肿。可见B免疫母细胞增生伴EBV阳性,甚至继发大B细胞淋巴瘤等。
形态学可分为三种模式:第一种模式为肿瘤细胞围绕增生的滤泡(有生发中心,但缺乏套区),此型与反应性增生鉴别困难;第二种模式为可见缩小的残存滤泡,在扩大的滤泡间区中,肿瘤细胞容易被识别;第三种模式为淋巴结结构完全或大部分被破坏,仅能在皮质区边缘看到残存的生发中心。
五、免疫表型
(1)瘤细胞表达T细胞分化抗原,如CD2、CD3和CD5。多数病例之瘤细胞为CD4+。
(2)其肿瘤细胞特征性地表达滤泡辅助T细胞型:CD10,BCL-6,PD-1,CXCL-13,ICOS
(3)滤泡树突网增生证据:CD21 ,CD23,CD35
(4)EBER:80%-95%+
(5)Ki-67 指数较高
(6)病变组织中增生的B免疫母细胞表达CD20抗原。
约90%的病例可检出T细胞受体基因的克隆性重排。
20%左右的病例存在免疫球蛋白基因的克隆性重排。
常见的突变发生在基因TET2、RHOA、IDH2和DNMT3A。
常见的细胞遗传学异常是3号染色体三体、5号染色体三体和外加一X染色体。
六、鉴别诊断
①富于T细胞和(或)组织细胞的大B细胞淋巴瘤;
②经典型霍奇金淋巴瘤;
③非特指外周T细胞淋巴瘤;
④淋巴结不典型T区增生。
七、预后
不同的患者,该肿瘤的临床过程、预后及对治疗的反应差异较大,50%的患者用泼尼松治疗可达完全缓解,约30%的患者可获长期无病生存,但平均生存期少于3年。
参考资料
[1]陈杰,步宏主编:临床病理学(第2版),人民卫生出版社,2021.
[2]刘彤华主编:刘彤华诊断病理学(第四版),人民卫生出版社,2018.
[3]李倩;苑静怡;周佳奇;赵敏;王珂.以肺部影像学改变为首发表现的血管免疫母细胞性T细胞淋巴瘤1例报告及文献复习[J].吉林大学学报(医学版),2022,48(03):796-800.
[4]黄城;黄慧强.血管免疫母T细胞淋巴瘤的诊断和治疗进展[J].中华转移性肿瘤杂志,2022,05(01):88-91.
[5]NCCN临床实践指南: T细胞淋巴瘤(2021.V1)
【6】NCCN临床实践指南: T细胞淋巴瘤(2019.2版)

















共0条评论