[导读] 作者:慧海拾穗
弥漫性大B细胞淋巴瘤的病理诊断和鉴别诊断(二)
【骨髓DLBCL的形态学】
大约10~25%的DLBCL患者在初始诊断时表现为骨髓受累。骨髓受累可能是一致的(原发部位和骨髓均表现为DLBCL),也可能是不一致的,即骨髓表现为低级别淋巴瘤。受累形式不同,从间质性、结节性、小梁旁到弥漫性(图14.11)。纯结节型在DLBCL中不是典型形态,在EBV+ DLBCL中更常见。

【免疫表型】
DLBCL通常表达CD45和全B细胞抗原,如CD19、CD20、CD22、CD79a、BOB1、OCT2和PAX5。PAX5在早期B细胞祖细胞和随后的B细胞分化阶段直到浆细胞阶段均可表现为核阳性,在浆细胞阶段它被下调(大约30%的浆细胞肿瘤是PAX5+)。终末分化的DLBCL,如免疫母细胞或浆母细胞性淋巴瘤,和使用抗CD20抗体(利妥昔单抗)治疗后的DLBCL可能缺乏CD20的表达。BCL2是一种参与凋亡控制的蛋白,在40~50%的DLBCL中可以观察到BCL2的表达(图14.12),BCL2阴性、CD10、BCL6、CD43阳性的DLBCL需与伯基特淋巴瘤(Burkitt lymphoma, BL)鉴别,BCL2、CD10强表达的DLBCL需与高级别B细胞淋巴瘤鉴别。生发中心细胞分化的分期特异性标志物BCL6和CD10,在DLBCL的一个亚群中表达(BCL6阳性率约60%,CD10阳性率约40%)。CD30在14%~21%的DLBCL中表达,并与独特的基因表达谱、非生发中心起源和良好的预后相关。原发性纵隔(胸腺)大B细胞淋巴瘤(PMBL)和间变性DLBCL通常都是CD30+。~40%的病例表达MUM1。一小部分DLBCL(<10%)表达CD5(原发CD5+DLBCL)或CD43(20%)。当无B-CLL/SLL病史且无BCL1/t(11;14)证据时,可诊断为原发CD5+DLBCL(通过免疫组化或细胞遗传学/荧光原位杂交)。罕见DLBCL可表现出CD56的异常表达。它们通常共同表达CD10。少数DLBCL病例异常表达CD3或CD7(图14.13)。

在>50%肿瘤细胞表达MYC蛋白的病例中,80%的病例具有MYC基因重排,在<50%的肿瘤细胞表达MYC蛋白的病例中,只有13%的病例具有MYC基因重排。据报道,极少数的DLBCL病例表达BCL1(cyclin D1),不表达SOX11且无CCND1重排或t(11;14)。这些病例通常是CD5-和MUM1+。
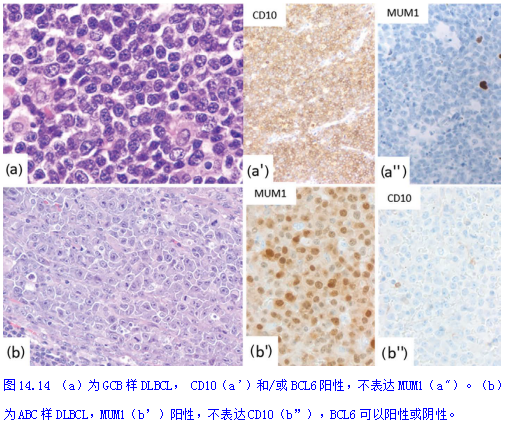
根据CD10、BCL6和MUM1/IRF4的表达,将DLBCL通过Hans算法分为生发中心样(Germinal Center B-cell-like,GCB)和非生发中心样(non-GCB)或活化B细胞样(Activated B-cell-like,ABC)两个亚组(图14.14)。CD10+(阈值为> 30%的细胞表达)和BCL6+/MUM1-(无论CD10表达如何)均视为GCB样,其余均为非GCB样。表14.1显示了ABC样DLBCL和GCB样DLBCL的主要区别。

【流式细胞术】
在流式细胞术(FC)分析中,与高级别淋巴瘤类似,由于肿瘤细胞的选择性退出(selective drop-out),FC可能无法检测到克隆B细胞群体或显示活性成分的优势,而只有少量的克隆性群体(图14.15)。在少量肿瘤细胞(如T细胞/组织细胞丰富DLBCL)或伴有明显纤维化(如原发性纵膈DLBCL)的DLBCL病例中,FC结果可能是假阴性。在一个成功的分析中,FC显示了一个前向散射增加(increased forward scatter)的克隆B细胞群体,并且经常伴有CD71表达(图14.16)。图14.17显示另一例具有GCB样表型的DLBCL。克隆B细胞显示的高正向散射有助于其与低级别滤泡性淋巴瘤(FL)的鉴别。鉴别诊断包括高级别FL、BL和高级别B细胞淋巴瘤。在FC分析中CD19和CD20的表达是不一致的。在Johnson等人的一系列报道中,272个样本中,共有43个(16%)的样本通过FC降低了CD20的表达;其中35例(13%)CD19表达明显。后者在使用环磷酰胺、阿霉素、长春新碱和泼尼松(CHOP)或利妥昔单抗-CHOP(R-CHOP)治疗时生存率明显较低。


未完待续
--------------------------------------往期回顾----------------------------------------------
弥漫性大B细胞淋巴瘤的病理诊断和鉴别诊断(一)



















共0条评论