[导读] 编译整理:强子
对于胃肠道早期肿瘤来说,内镜下黏膜切除术(endoscopic mucosal resection,EMR)和内镜黏膜下剥离术(endoscopic submucosal dissection,ESD)是比较先进的治疗技术。通过这类技术,可以切除局限于黏膜或黏膜下的肿瘤,使得患者免于更加激进的手术治疗。EMR和ESD手术中,会在病变下方注射溶液、使得病灶抬举起来,且形成一个液体填塞区使得黏膜下层和固有肌层分离开来,从而利于手术操作。以往使用的液体是混有染液的盐水。尽管这类液体无毒、价廉,但却可以被周围组织快速吸收,导致填塞作用丧失,较长时间、较复杂操作中需要重复注射。此外还有很多其他制剂用于这一目的,如透明质酸、琥珀酰明胶、羟乙基淀粉、葡萄糖水。尽管这些物质相比盐水染液来说有了一定改进,但目前都没有被广泛用于相关操作的金标准。
近年来,美国食品药品监督管理局批准了合成的黏膜下注射剂用于临床,具体有Eleview、ORISE。其中Eleview是这类产品中第一个获批的,其组成成分复杂,包括了水、氯化钠、填充和结构剂、乳化剂、对比和增强剂、油性成分;ORISE的组成成分类似。虽然这些合成制剂的价格昂贵,但初步研究表明其黏膜下抬举的时间更长、较少需重复注射、操作时间更短。不过,尽管临床应用逐步增加,但关于这类物质在人体内的组织学表现却报道甚少。科罗拉多大学病理专家Westbrook收集所在单位应用ORISE约六个月内的相关标本,对相应组织学表现的特征进行观察并报道于《Am J Clin Pathol》。为帮助大家更好的了解相关问题,避免实际工作中遇到时误诊误判,我们将该文中报道的病例要点编译介绍如下。
病例展示
病例1为70岁男性,肠镜检查发现结肠较大息肉,拟行内镜下切除。镜下在升结肠发现一70mm无蒂息肉。总计注入106ml的ORISE凝胶、病变充分抬举后进行EMR,将该息肉分段、完全切除,切缘进行烧灼。
标本组织学检查为管状绒毛状腺瘤,无高级别异型增生。值得注意的是,黏膜下可见术前注入的大量ORISE凝胶,HE切片中表现为淡染、灰蓝色黏液样物质。特殊染色黏液卡红为阳性,而PAS、PAS-D、阿辛兰染色均为阴性,Masson三色无特殊。
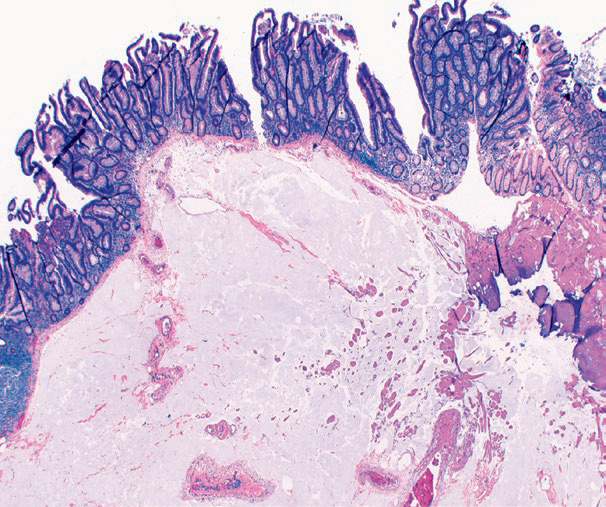
图1. 病例1病理检查所见,该例为注射后立即EMR:HE染色切片中表现为黏膜下黏液样物质。
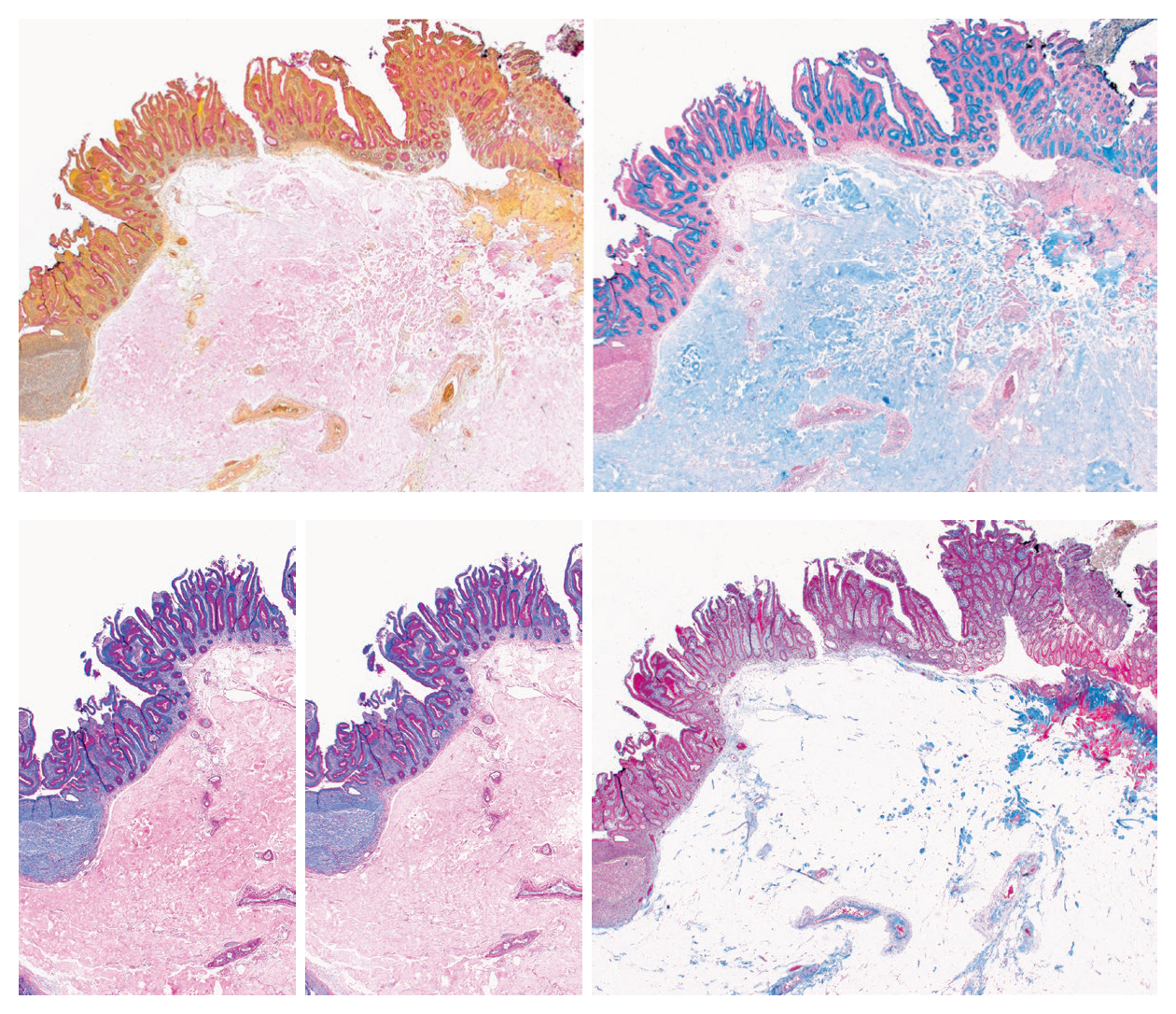
图2. 病例1特殊染色结果:黏液卡红染色有一定阳性表现(左上)。阿辛兰染色中,该凝胶呈微弱蓝色(右上),但与杯状细胞中明亮的蓝色相比,还是应视为阴性。PAS染色(左下)、PAS-D染色(下中)及Masson三色染色(右下),均无特殊所见。
病例2为64岁男性,内镜下贲门近食管鳞柱状交界处见息肉状肿物,活检证实为腺癌。病变处注射ORISE凝胶,但中央部分未能抬举,因此未进行EMR。后续未行新辅助治疗。约2个月(64天)后,行食管胃切除术。
标本组织学检查,证实为中分化腺癌,侵及黏膜下层。病变区域有大量嗜酸性、无定型、无极化表现的物质,伴大量异物型巨细胞反应。这些嗜酸性物质存在于黏膜下层、固有肌层,局灶外膜也有这类物质。
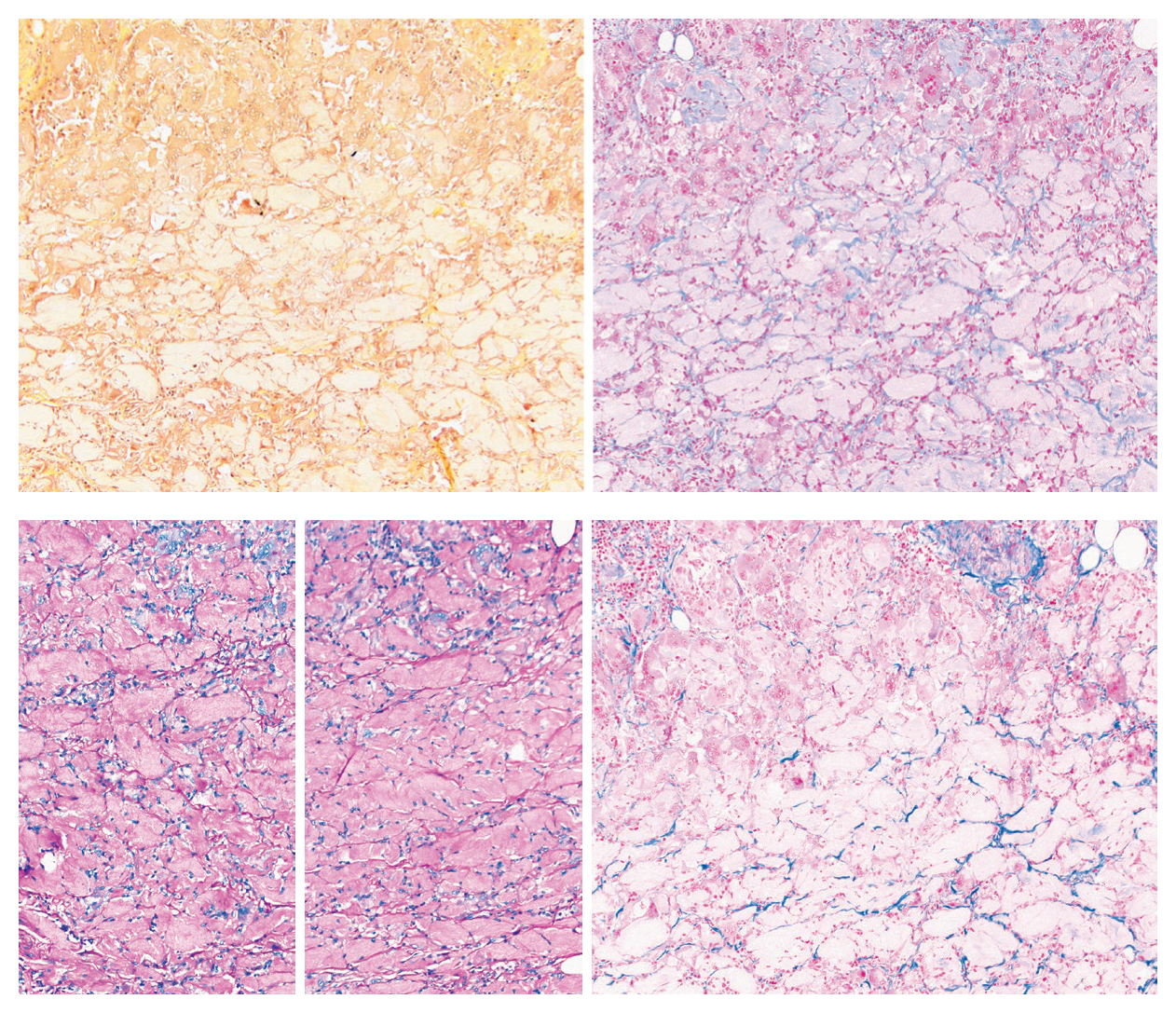
图3. 病例2的HE染色所见:低倍镜下,黏膜下可见嗜酸性物质(左上);高倍镜下可见老化的凝胶,具体表现为嗜酸性、无定型物;散在多核巨细胞并有混合型炎症细胞浸润(右上)。固有肌层(左下)、部分外膜(右下)可见类似表现。
特殊染色检查,这些物质黏液卡红、PAS、PAS-D、阿辛兰染色均阴性,Masson三色中有少许蓝色着色,刚果红染色阴性。

图4. 病例2特殊染色所见:黏液卡红(左上)、阿辛兰(右上)、PAS(左下)、PAS-D(中下)染色均为阴性,Masson三色(右下)中呈少许蓝色着色。
病例3为55岁女性,活检证实为直肠管状腺瘤、伴高级别。内镜下为35mm无蒂息肉。注入ORISE凝胶后,仅部分自固有肌层抬举起来。由于部分区域未能抬举起来,因此行ESD手术。组织学证实为管状腺瘤、伴高级别异型增生。黏膜下有大量灰蓝色无定型凝胶,与前述病例1所见相似。
ESD后约2个月(66天)时内镜随访,直肠处未见息肉残余,但有10mm的黏膜切除术后瘢痕。瘢痕处活检,组织学检查未见异型增生残余,但一处组织碎片中在黏膜下可见淡染、无定型物质,伴多核巨细胞。
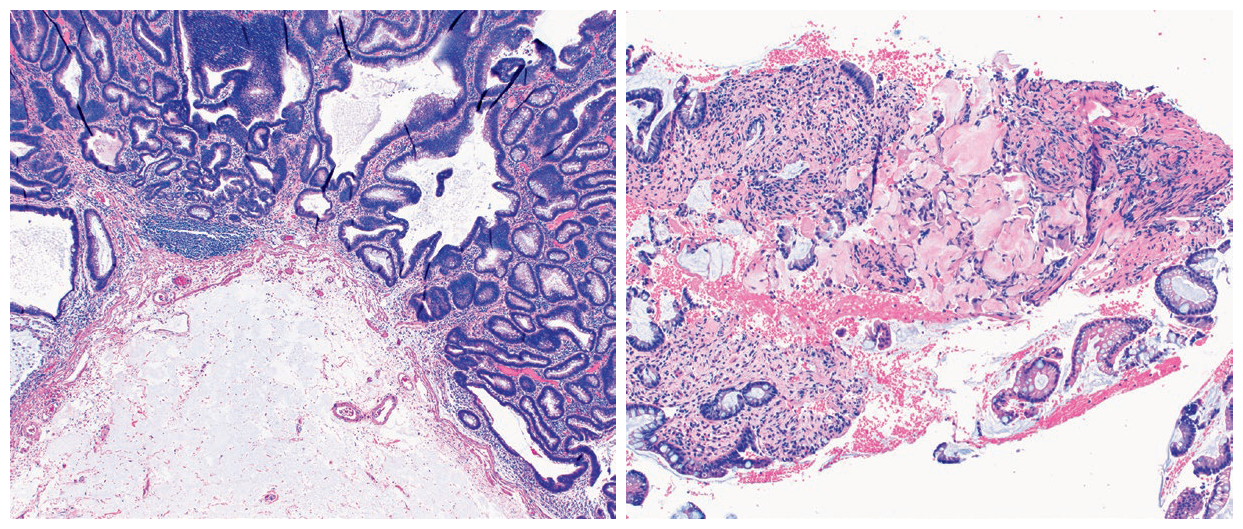
图5. 病例3首次术后标本病理检查所见(左),在黏膜下可见淡染、灰蓝色黏液样表现的ORISE凝胶;病例3注射ORISE凝胶66天后活检标本所见(右),可见有凝胶残余。
病例4为73岁女性,活检证实为结肠腺癌。内镜下乙状结肠可见20mm息肉,以ORISE凝胶作为黏膜下抬举剂,行ESD治疗。组织学检查证实为中分化腺癌,发生于伴高级别异型增生的管状腺瘤。腺癌至少侵及黏膜下层,底部切缘及周围切缘可见恶性肿瘤细胞。标本中除前述凝胶外,还有肿瘤产生的黏液湖:尽管二者在HE切片中颜色相似,但ORISE凝胶为无定型表现,而肿瘤黏液呈条索状。本例也做了特殊染色,残留的凝胶仅有阿辛兰染色阳性;肿瘤产生的黏液在阿辛兰染色、黏液卡红染色、PAS染色、PAS-D染色均为强阳性。
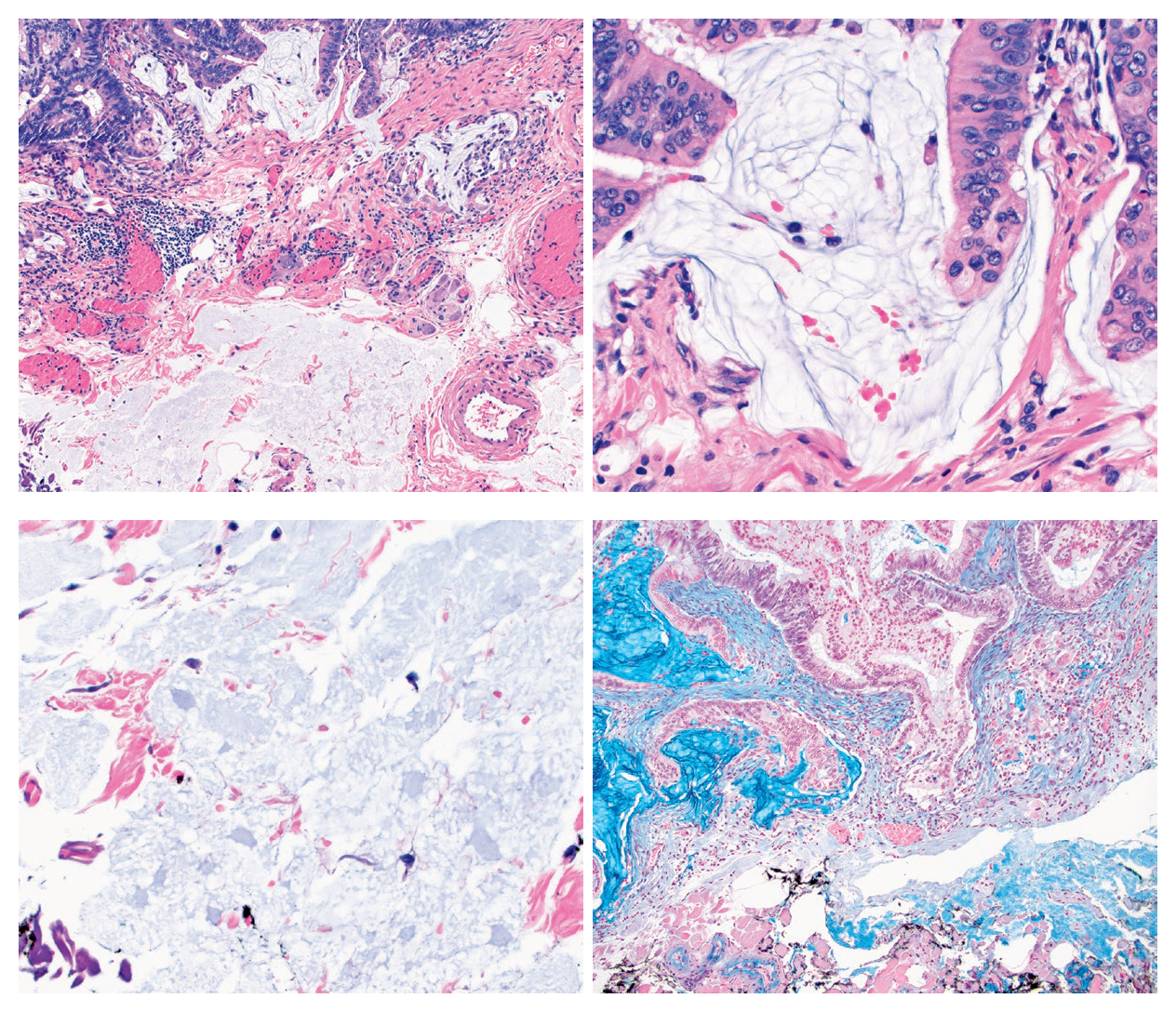
图6. 病例4病理检查所见:(左上)图中上半部分为肿瘤内的黏液成分,下半部分为ORIGE凝胶;高倍镜下,肿瘤黏液呈条索状(右上),而ORISE凝胶呈无定型表现(左下)。(右下)特殊染色,肿瘤黏液在阿辛兰染色呈强阳性(该图中左上角、右下角),而ORISE凝胶为淡蓝色(阴性)。
小结
据本文原作者所述,这是文献中第一次报告ORISE凝胶的组织学特点。尽管本文并未涉及FDA批准的另一同类物质-Eleview,但由于二者组成成分相似,因此推测后者的组织学表现应该与本文所述类似。
根据本研究所见,ORISE凝胶注入黏膜下后立即切除,组织学检查中的表现类似黏液。不过,如果间隔一段时间后再切除,则这些凝胶表现出更强的嗜酸性,类似透明样变,且可以出现异物型巨细胞反应,作者将其称之为“抬举剂肉芽肿”(lifting agent granuloma)。
了解相关病史、熟悉相关组织学表现,可以避免病理诊断中的误诊误判,如本文中所述与黏液的鉴别、与淀粉样物的鉴别等。鉴于间隔一定时间的情况下,组织学可以表现为肉芽肿,因此还应注意鉴别其他原因导致的肉芽肿,如食物肉芽肿(pulse granuloma)、缝线肉芽肿。不过,后两者具有独特表现的异物。具体如食物肉芽肿来说,是由于溃疡或穿孔、食物进入肠壁内或腹膜而引起的异物肉芽肿。食物肉芽肿形态一般更圆,且较为局限,不会有不规则、浸润性表现,而ORISE凝胶所致肉芽肿由于是注射所致,所以可能不规则、形似浸润表现。

图7. 抬举剂肉芽肿(左)与食物肉芽肿(右)形态学特征比较:二者有一定程度的相似性,如均为无定型嗜酸性物质,伴异物型巨细胞反应。不过,结合临床病史及相关物质在组织内的分布特点,有助于鉴别。
关于食物肉芽肿的更多问题,我们曾经有过相关介绍-《读书,必会有所得-降结肠食物肉芽肿一例》,详见本网站链接http://news.ipathology.cn/article/4713.html。
点击下载原文文献
参考文献
Westbrook LM, Henn PA, Cornish TC. Lifting Agent Granuloma. Am J Clin Pathol. 2020;153(5):630-638.
doi:10.1093/ajcp/aqz204



















共0条评论