[导读] 来源:陈世昌(台湾 台中荣民总医院)
导管原位癌
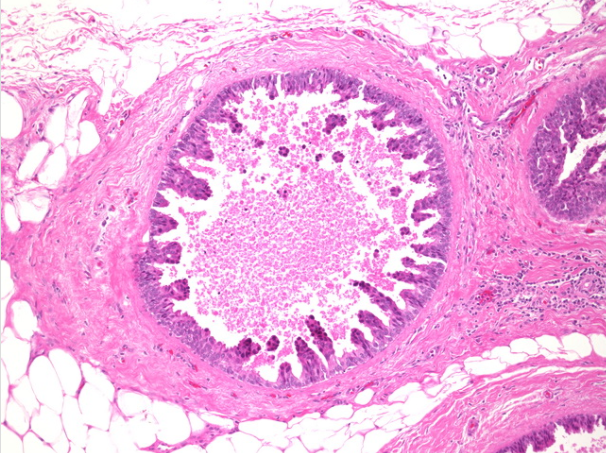
DCIS的微乳头变体显示出细长的上皮叶状突起进入腺腔。这些预测是坚实的,缺乏真正的纤维血管核心。它们由核级中等的肿瘤细胞组成。
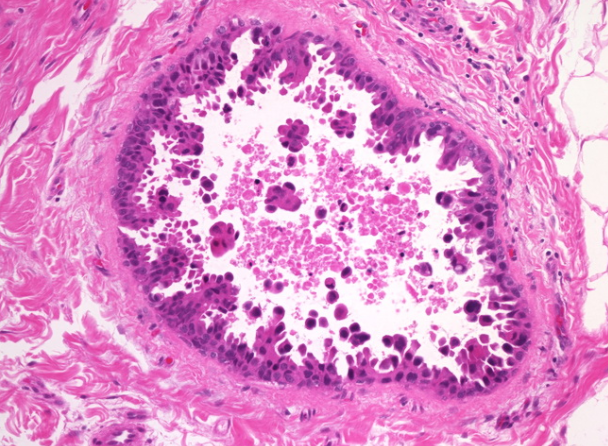
在这种情况下,微乳头DCIS的乳头范围从肿瘤细胞的小隆起或丘陵到细长的乳头结构。核等级很高。伸入内腔的一些乳头状叶可能会被横向切开,从而导致内腔中出现细小分离的不规则簇状肿瘤细胞(如此处所示)。内腔中也存在细胞碎片,通常是高核级病例的特征
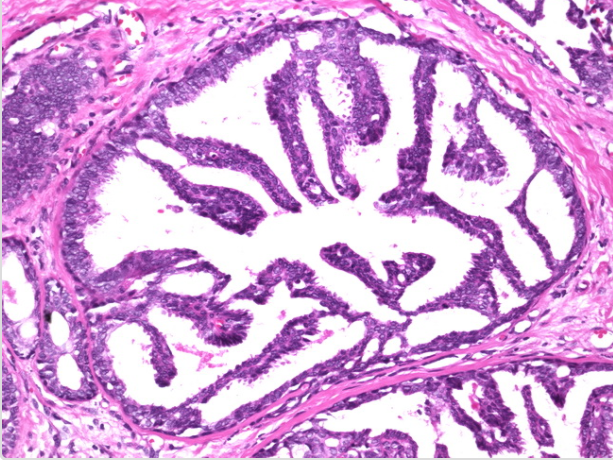
在本例的微乳头DCIS中,乳头结构显示出其尖端的球状扩张。一些相邻的乳头状叶已合并形成罗马桥拱。当相邻叶状体之间的融合广泛时,会导致筛状结构的形成。 DCIS的微乳头状和网状形式通常并存

在筛状DCIS中,在腺体中发现了圆形窗孔。这些空间在大小,形状和分布上越规则,病变就越有可能是恶性的。 cribriform DCIS在表面上类似于腺样囊性癌和胶原性球菌病,不应将其误认为是这些实体。
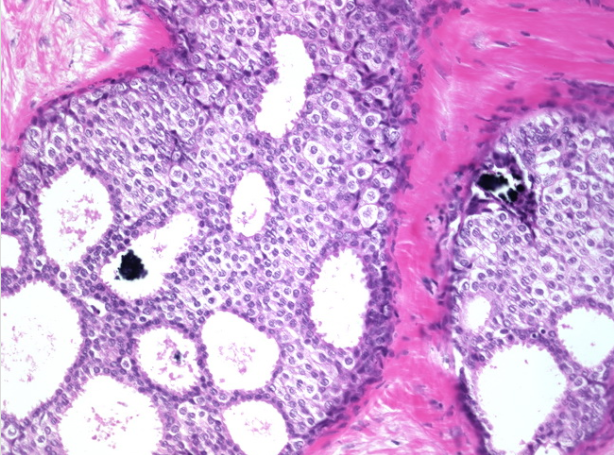
筛状DCIS的高倍镜显示微钙化。
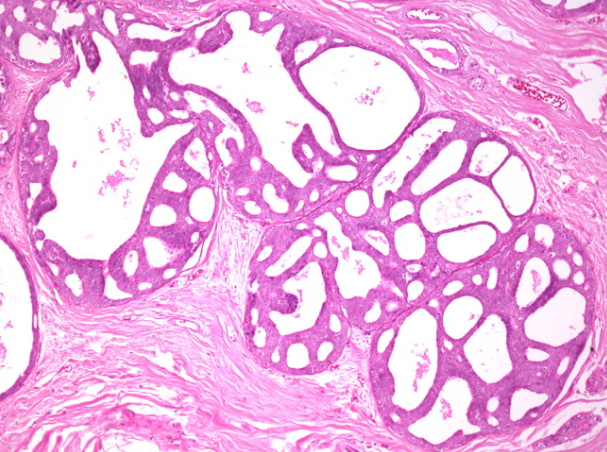
一例筛状DCIS显示开窗,罗马桥和小梁
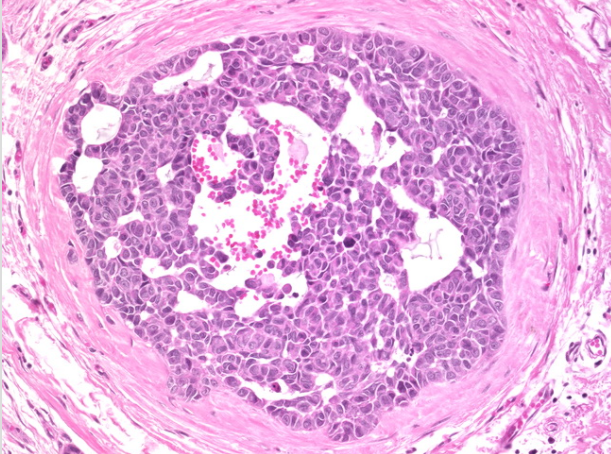
在本例的DCIS中,具有高核级的肿瘤细胞几乎充满了管腔。胞质边界被清晰地划定。
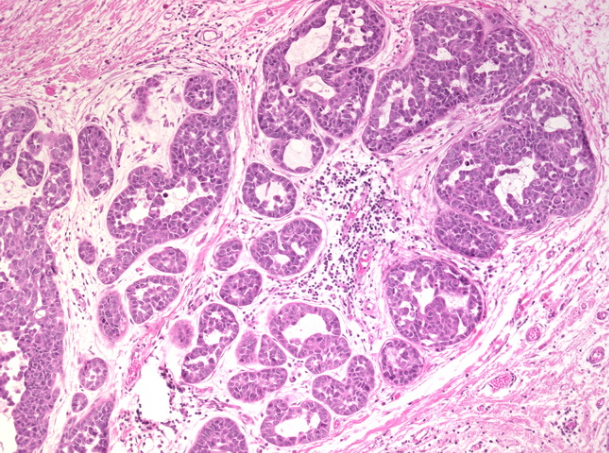
癌细胞存在于结构清晰可见的小叶中。该小叶是它与DCIS的参与大大扩展。肿瘤细胞具有高核级。小叶癌变的现象进一步支持了末端导管-小叶单位这一概念,它是许多导管内癌的起源部位。
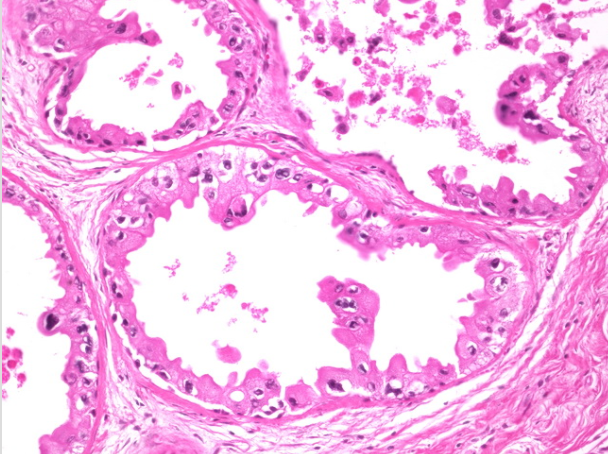
此例DCIS显示出载脂蛋白型细胞学,癌细胞具有丰富的嗜酸性粒细胞质和多形核。建筑模式是紧贴型的。
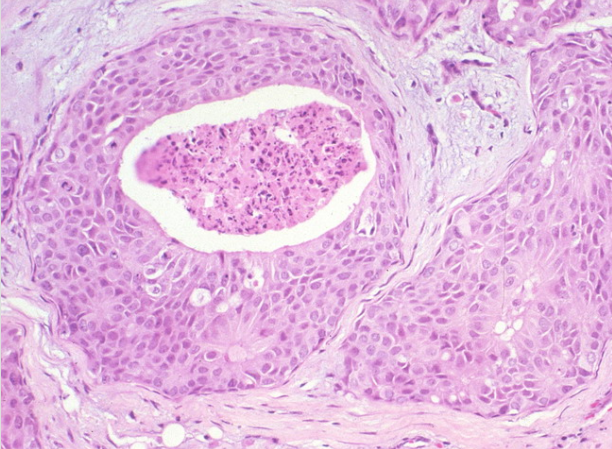
在患有粉刺坏死的DCIS中,受累导管沿导管周围显示出稳定的生长,并具有高核级。有丝分裂活动活跃,内腔中总是存在坏死。坏死中可能存在粗大的钙化。导管周围组织显示纤维化和血管生成的证据。
小叶原位癌
小叶原位癌(LCIS)通常是偶然发现,最常见于上部外部象限和上部内部象限。在大约70%的病例中是多中心的,在30%到40%的病例中是双侧的。
的小叶被扩展和通过圆形的均一群体,小到中型的肿瘤细胞完全充满。但是,小叶增大和管腔的完全缺失并不是绝对的诊断要求。通常不存在非典型性,核多型性,有丝分裂活性和坏死-除了一小部分称为多形 LCIS的病例。肿瘤细胞失去凝聚力。分散的印戒细胞经常出现。肿瘤细胞可能表现为page状扩散到邻近的末端导管 ; 但是,佩吉特病几乎从未见过。
对于渍粘蛋白是积极在集装箱检查系统的情况下约75%。免疫组织化学分析显示,LCIS缺乏E-钙黏着蛋白和β-连环蛋白,且对高分子量细胞角蛋白(核周围模式) 呈阳性,这有助于将其与DCIS区别开来。
LCIS作为危险因素:大约20%至30%的LCIS患者会发展为浸润性乳腺癌,可能是小叶型或导管型。 LCIS病变发展的情况下,风险更大。风险是不取决于LCIS的数量。风险增加适用于两个乳房。 LCIS患者可以得到安全的随访。在乳腺癌家族史丰富的患者,忧郁症患者或广泛纤维囊性疾病患者中,可以考虑进行治疗性干预(例如单纯乳房切除术)。
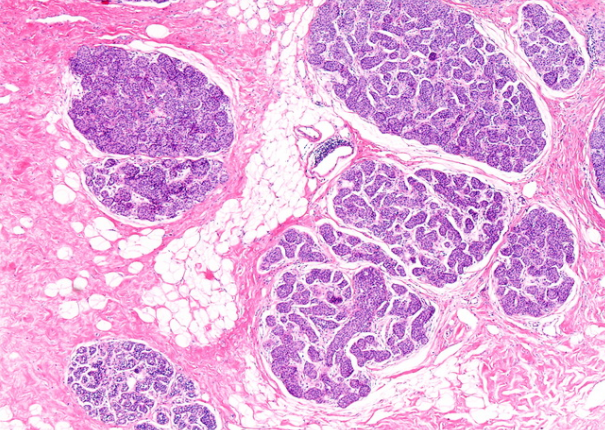
原位小叶癌(LCIS)是不可触及的病变,通常是由于其他原因而切除的乳房中的偶然发现。在70%的病例中是多中心的,在30%到40%的病例中是双侧的。的小叶胀得具有均匀圆形或椭圆形,中等大小的细胞。原子核是均匀的和常色的。此图显示了涉及几个小叶的LCIS。左下角可见小叶。
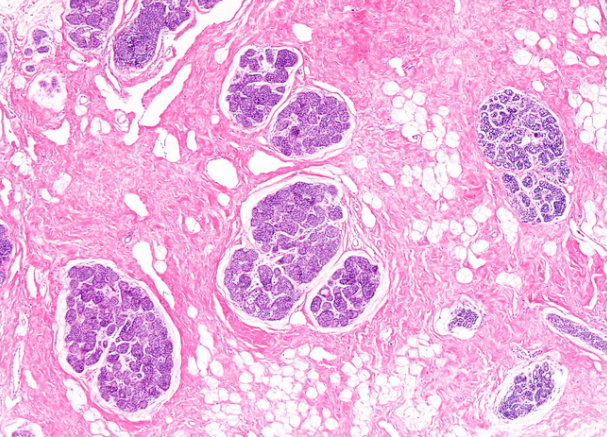
原位小叶癌(LCIS)是不可触及的病变,通常是由于其他原因而切除的乳房中的偶然发现。在70%的病例中是多中心的,在30%到40%的病例中是双侧的。的小叶胀得具有均匀圆形或椭圆形,中等大小的细胞。原子核是均匀的和常色的。此图显示了涉及几个小叶的LCIS。在右侧可以看到一些未参与的小叶。
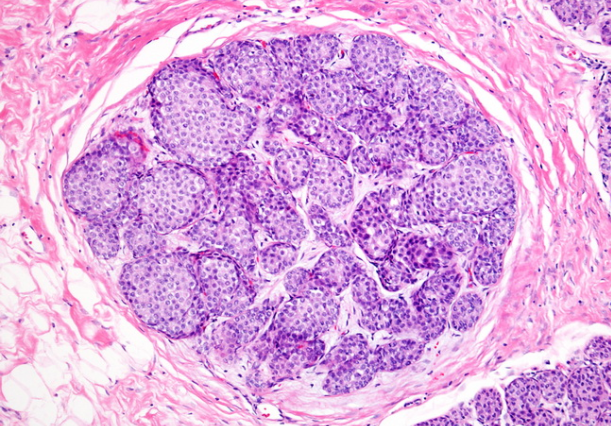
LCIS的诊断应用于细胞增殖导致形成实体巢并扩大整个小叶的情况。但是必须强调的是,小叶扩张不是绝对的标准,尤其是在绝经后的女性中。
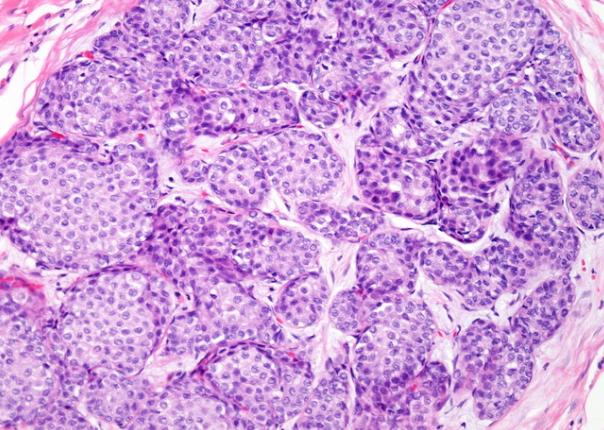
该小叶膨胀并通过圆的均一群体,小到中型的肿瘤细胞完全充满。但是,小叶增大和管腔的完全缺失并不是绝对的诊断要求。通常不存在非典型性,核多态性,有丝分裂活性和坏死-除了一小部分称为多形 LCIS的病例。
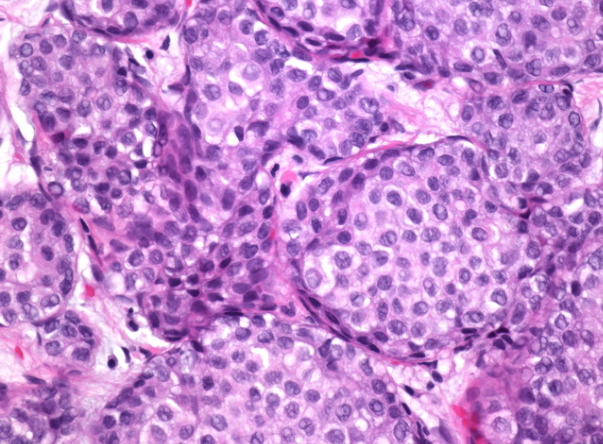
在诊断为LCIS后,约20%至30%的患者将在没有治疗的情况下发展为浸润性癌。尽管在诊断性活检方面这风险更大,但是这两种风险都适用于两个乳房。浸润性癌可以是小叶型或导管型。
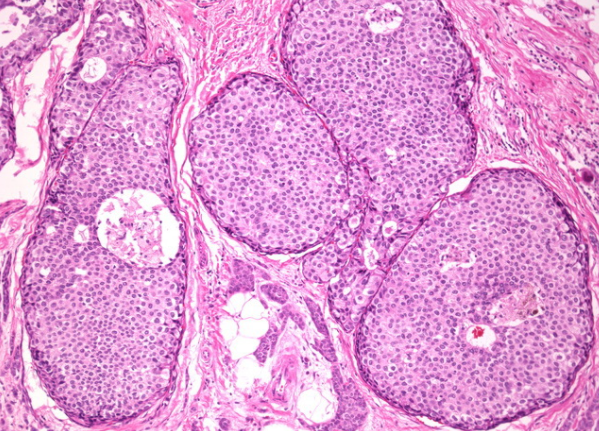
LCIS典型病例顯示無異型,核多型性,有絲分裂活動增加或壞死。單獨或組合使用這些功能中的任何功能均會導致指定多形LCIS。
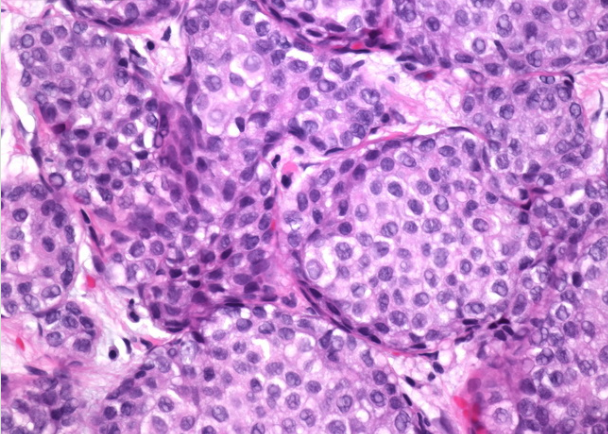
LCIS典型病例显示无异型,核多型性,有丝分裂活动增加或坏死。单独或组合使用这些功能中的任何功能均会导致指定多形LCIS。
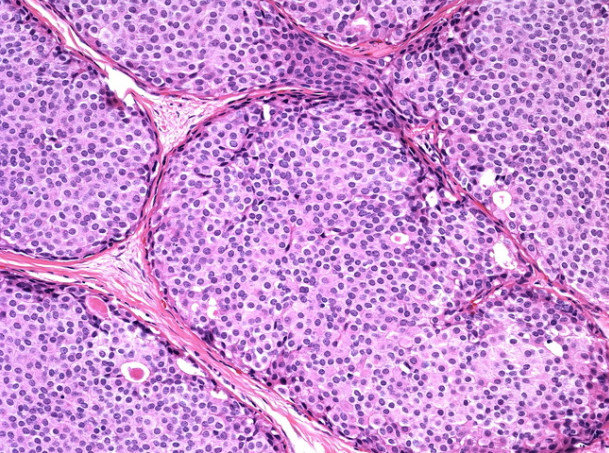
LCIS典型病例显示无异型,核多型性,有丝分裂活动增加或坏死。单独或组合使用这些功能中的任何功能均会导致指定多形LCIS。
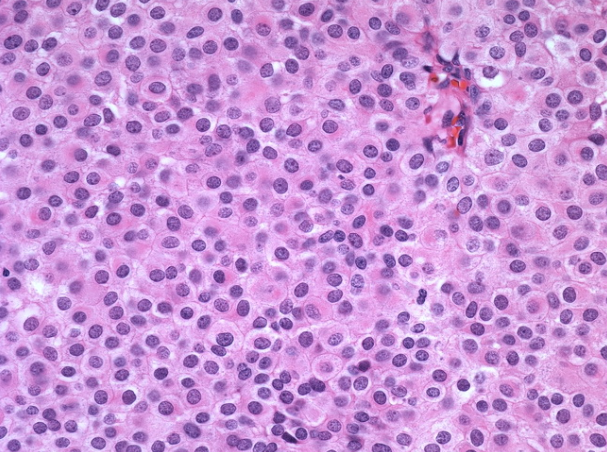
高倍视图显示在LCIS的典型情况下缺乏多态性。
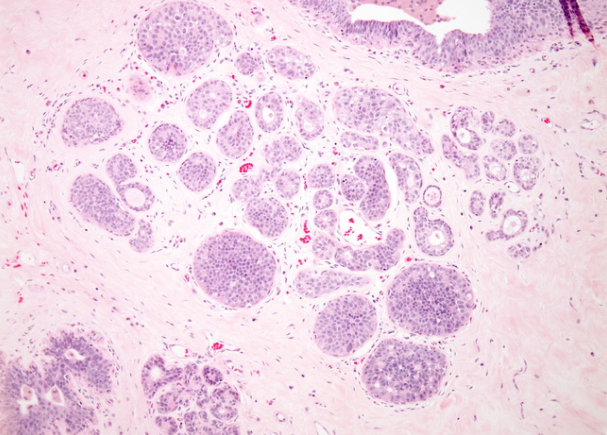
当增殖性改变导致小巢被实巢明显扩张时,将使用术语LCIS。在不典型的小叶增生(ALH)中,小叶大小正常,仍包含可识别的腔。但是,小叶增大不是LCIS的绝对诊断标准。同样,对于LCIS的诊断,完全不需要内腔。此图显示了从ALH到LCIS的发现范围。
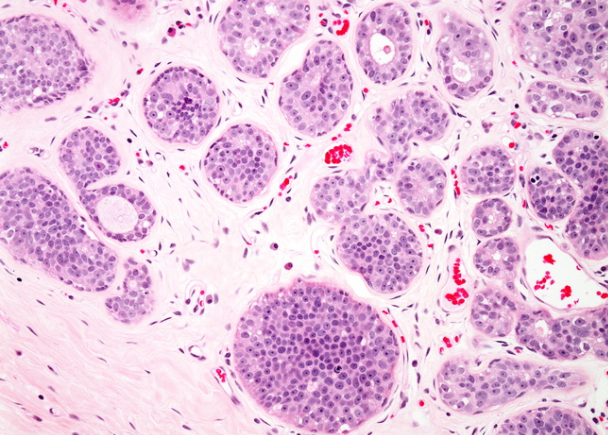
当增殖性变化导致小巢被实心巢明显扩张时,将使用术语LCIS。在不典型的小叶增生(ALH)中,小叶大小正常,仍包含可识别的腔。但是,小叶增大不是LCIS的绝对诊断标准。同样,对于LCIS的诊断,完全不需要内腔。此图显示了从ALH到LCIS的发现范围
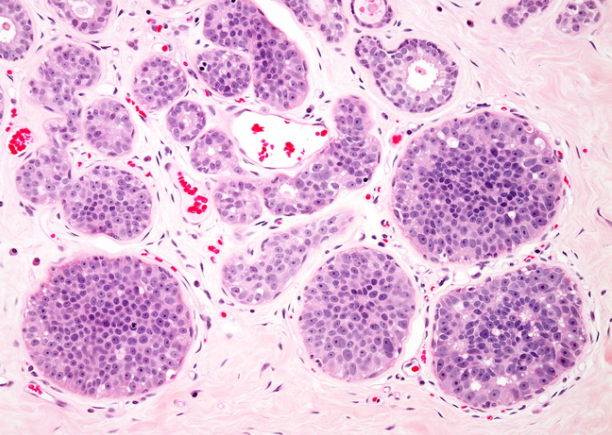
增殖性变化导致小巢被实心巢明显扩张时,将使用术语LCIS。在不典型的小叶增生(ALH)中,小叶大小正常,仍包含可识别的腔。但是,小叶增大不是LCIS的绝对诊断标准。同样,对于LCIS的诊断,完全不需要内腔。此图显示了从ALH到LCIS的发现范围。
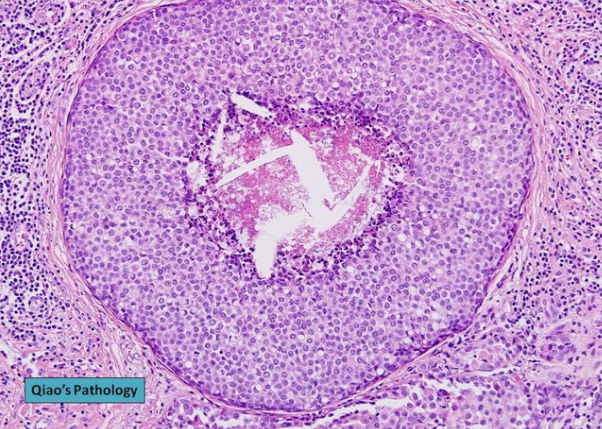
显微照片显示单调的肿瘤细胞,带有少量分散的印戒细胞和中央肿瘤坏死。
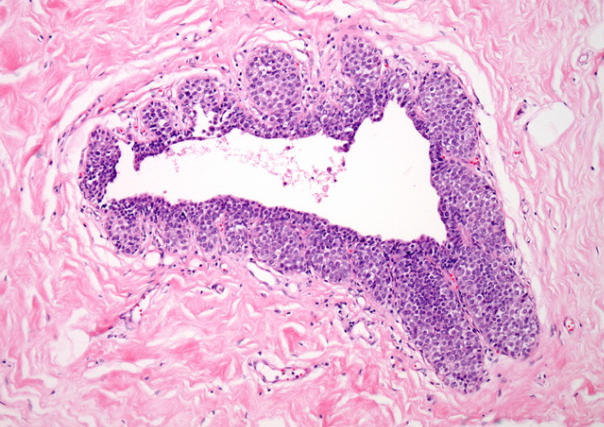
在LCIS中,肿瘤细胞可能显示出页面状扩散到邻近的末端导管中。但是,佩吉特病几乎从未见过。
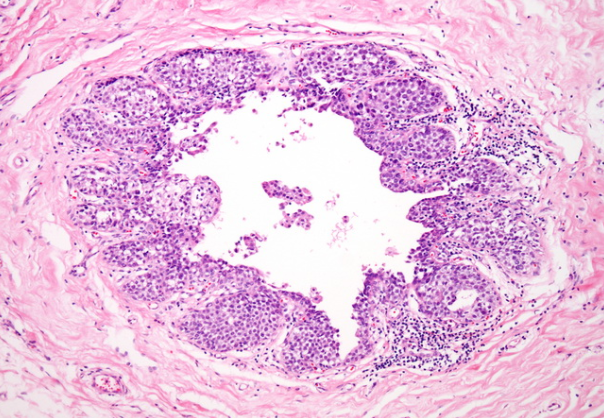
在LCIS中,肿瘤细胞可能显示出页面状扩散到邻近的末端导管中。但是,佩吉特病几乎从未见过。
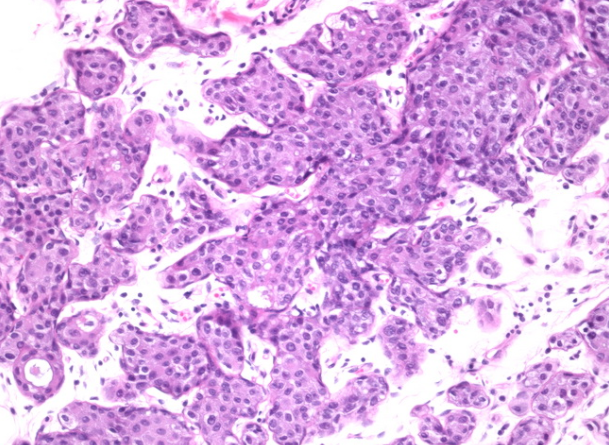
LCIS可能存在于良性增生性病变中,例如纤维腺瘤,乳头状瘤,放射状硬化性病变和硬化性腺病(如图所示)。当存在于硬化性病变中时,LCIS会扭曲小叶构型,很难排除这种病灶的侵袭。然而,在硬化性病变中,腺体被基底膜,肌上皮细胞和基质包围。这些成分可以通过网状蛋白染色,层粘连蛋白和IV型胶原蛋白的免疫染色以及肌上皮标记物来突出显示。胞浆粘蛋白的存在支持LCIS。此外,LCIS将显示出E-钙黏着蛋白的丧失 -这是前面提到的良性增生性病变所不具有的特征。
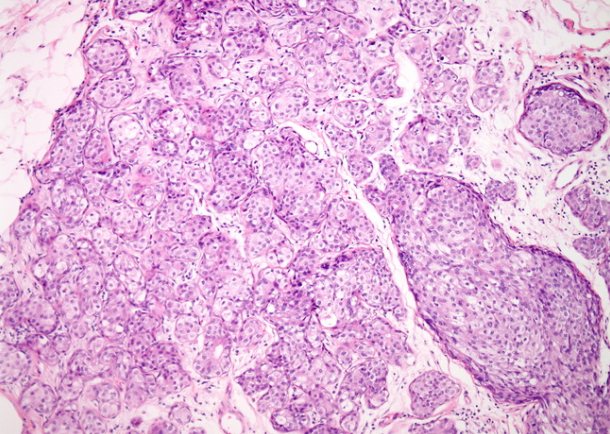
LCIS可能存在于良性增生性病变中,例如纤维腺瘤,乳头状瘤,放射状硬化性病变和硬化性腺病(如图所示)。当存在于硬化性病变中时,LCIS会扭曲小叶构型,很难排除这种病灶的侵袭。然而,在硬化性病变中,腺体被基底膜,肌上皮细胞和基质包围。这些成分可以通过网状蛋白染色,层粘连蛋白和IV型胶原蛋白的免疫染色以及肌上皮标记物来突出显示。胞浆粘蛋白的存在支持LCIS。此外,LCIS将显示出E-钙黏着蛋白的丧失 -这是前面提到的良性增生性病变所不具有的特征。
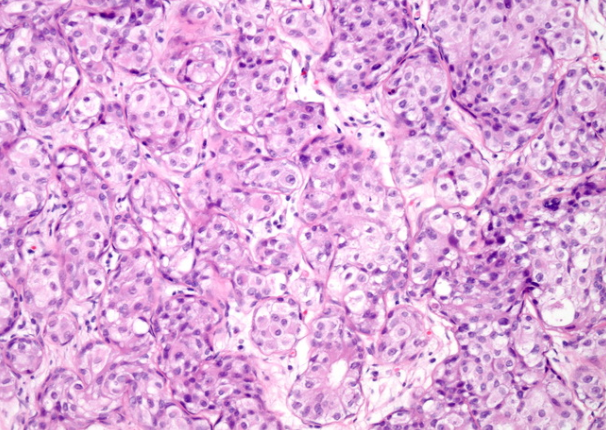
LCIS可能存在于良性增生性病变中,例如纤维腺瘤,乳头状瘤,放射状硬化性病变和硬化性腺病(如图所示)。当存在于硬化性病变中时,LCIS会扭曲小叶构型,很难排除这种病灶的侵袭。然而,在硬化性病变中,腺体被基底膜,肌上皮细胞和基质包围。这些成分可以通过网状蛋白染色,层粘连蛋白和IV型胶原蛋白的免疫染色以及肌上皮标记物来突出显示。胞浆粘蛋白的存在支持LCIS。此外,LCIS将显示出E-钙黏着蛋白的丧失 -这是前面提到的良性增生性病变所不具有的特征。
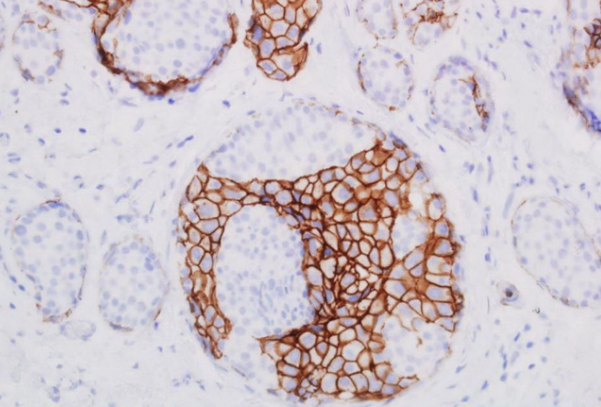
显微照片显示DCIS和LCIS混合病变。 DCIS对E-钙粘蛋白呈阳性,而LCIS对E-钙粘蛋白呈阴性。一个导管对DCIS和LCIS都具有混合染色。 IHC染色。
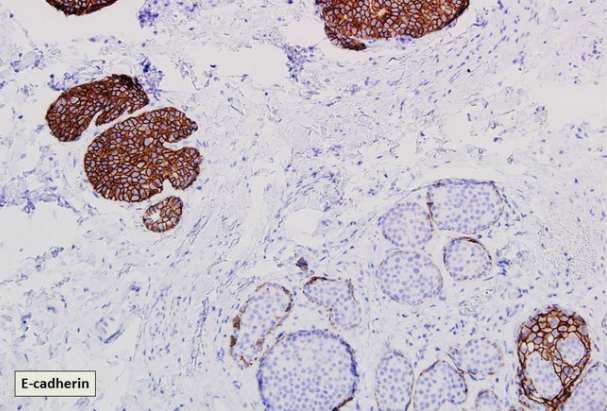
显微照片显示DCIS和LCIS混合病变。 DCIS对E-钙粘蛋白呈阳性,而LCIS对E-钙粘蛋白呈阴性。一个导管对DCIS和LCIS都具有混合染色。 IHC染色。
乳頭狀癌

乳头状癌占女性乳腺癌的1%至2%。患者通常比其他乳腺癌患者年龄更大(平均年龄63至67岁)。在原位乳头状癌的囊内变体中,肿瘤表现为由扩张导管形成的囊性空间内的壁结节。在某些情况下,可能还会看到侵入性成分。
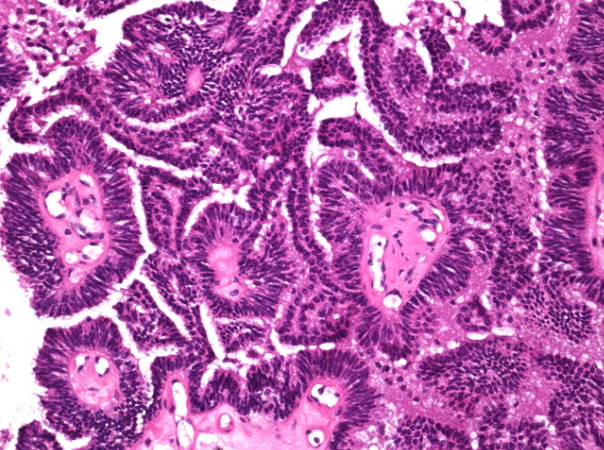
一例的高倍镜显示了几个具有纤维血管核心的乳头状结构。有利于癌变的特征是上皮细胞大小和形状的均匀性,肌上皮细胞的缺乏,核增生,核增大和有丝分裂活性高。邻近乳房缺乏良性增生性改变也有利于癌变。

囊内乳头状癌的另一个例子。缺乏或间质的基质(如此处所示)有利于乳头状癌。但是,偶尔的病例可能在乳头状结构中有发达的间质。由于乳头状癌经常出现在乳房的中央部位,因此乳头溢液或出血是常见的临床发现。
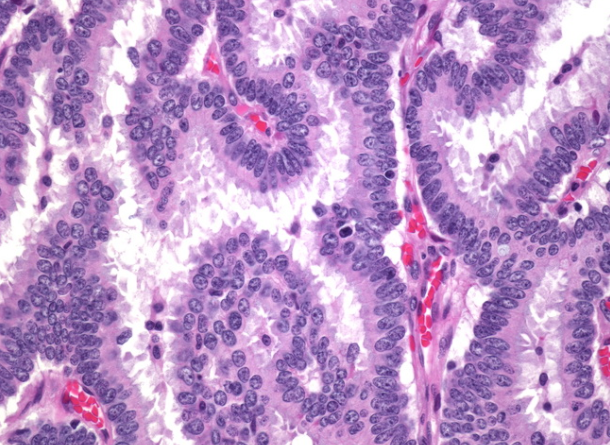
上一张图像的高倍视图。肿瘤细胞的形状和大小均一,并垂直于导管轴排列。肌上皮细胞不存在。基质很少
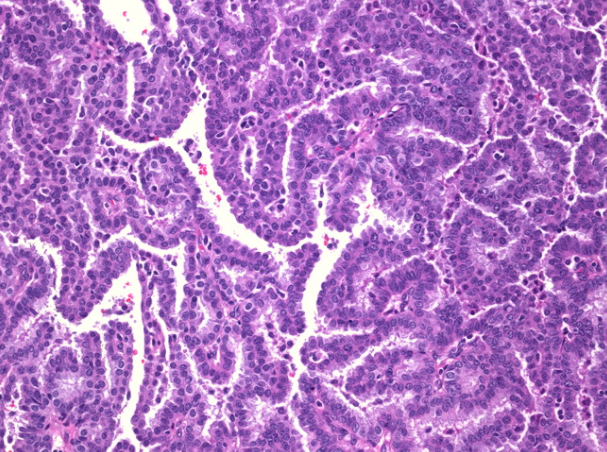
在大多数乳头状癌病例中,上皮细胞增生会填充相邻纤维血管基质核之间的空间,从而导致乳头状,腺体结构和实心区域复杂。
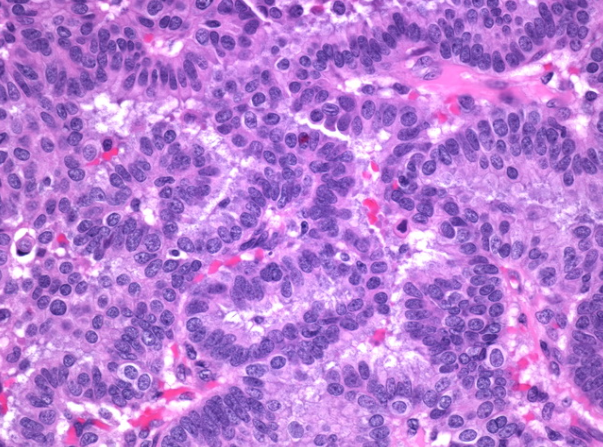
该图像显示了散布的大细胞,具有淡淡的嗜酸性细胞质(图像底部)。它们是对GCDFP-15具有免疫反应性的所谓球状细胞或透明细胞。他们不应被误认为是肌上皮细胞。
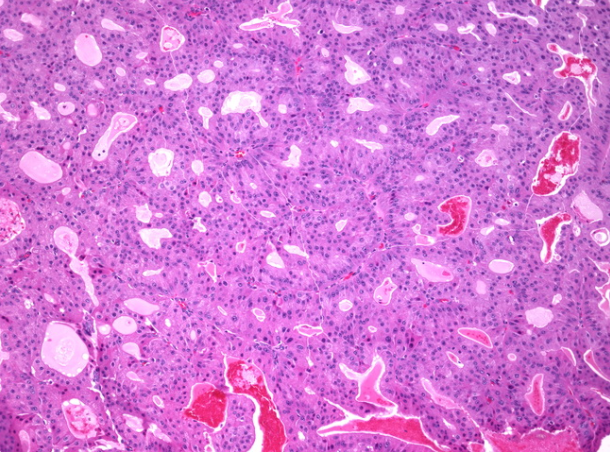
乳头状癌可能会出现泌乳腺上皮化生。
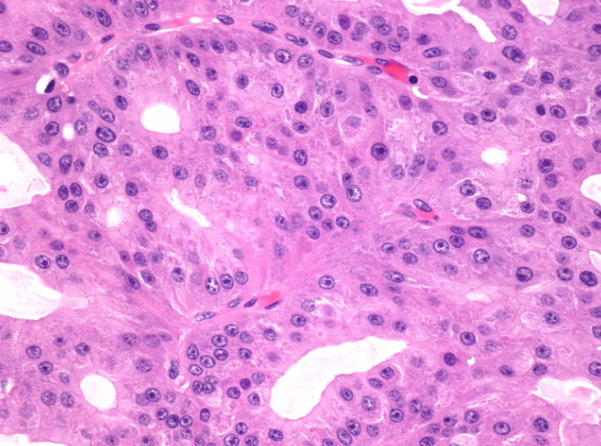
在乳头状乳癌中遇到的顶泌区显示出与肿瘤其他部位相似的细胞学异型性。细胞核扩大,囊泡突出
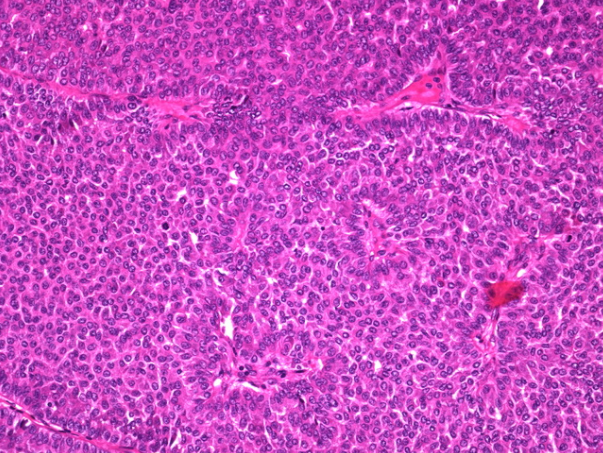
在乳头状癌的实体变型中,囊肿形成极少或不存在。肿瘤几乎完全由固体,非叶状形成的上皮组成。细小的纤维血管基质索使人们可以将其识别为乳头状癌。
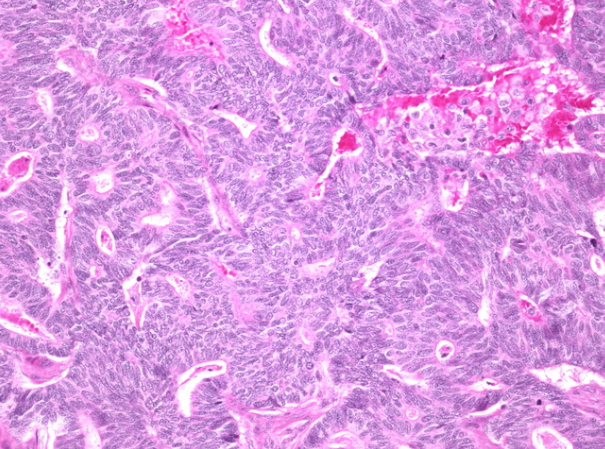
这是乳头状乳癌实体变体的另一个例子。在这种情况下,肿瘤细胞显示出刺刺。
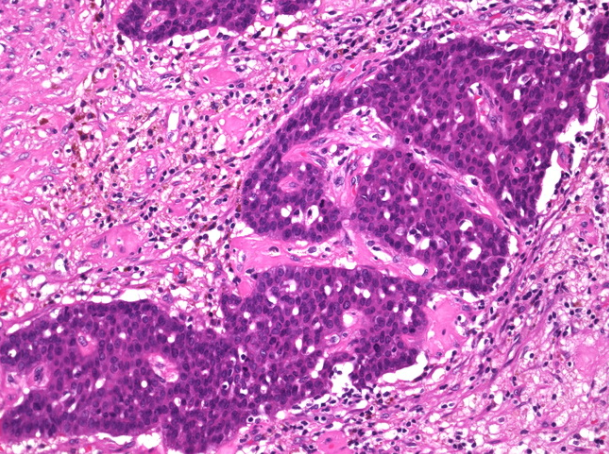
诊断乳头状乳头状癌可能非常困难。许多病例有纤维化,近期或偏远出血,发炎或对以前的穿刺活检程序有反应的区域。癌的扩展超出肿瘤边界和增生基质反应通常支持侵袭的存在(如该图所示)。
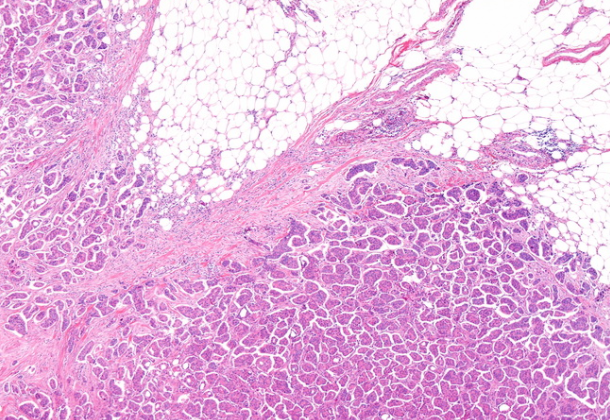
癌(MPC)是导管癌的一种侵略性变体,类似于其他主要部位(例如卵巢,肺,胰腺和膀胱)的微乳头状癌。纯MPC 很少见,占所有乳腺癌的1.5-2.5%。
它通常表现为可触及的肿块在外上象限的乳房。乳房X线照片显示高密度的不规则肿块,边缘有针刺。通常会出现微钙化。大小范围是几毫米到几厘米,通常大于导管癌NOS。经常出现转移到多个腋窝淋巴结。
肿瘤细胞排列在微乳头状,肾小管-肺泡状或桑树状簇中,周围被腔隙或透明空间包围。
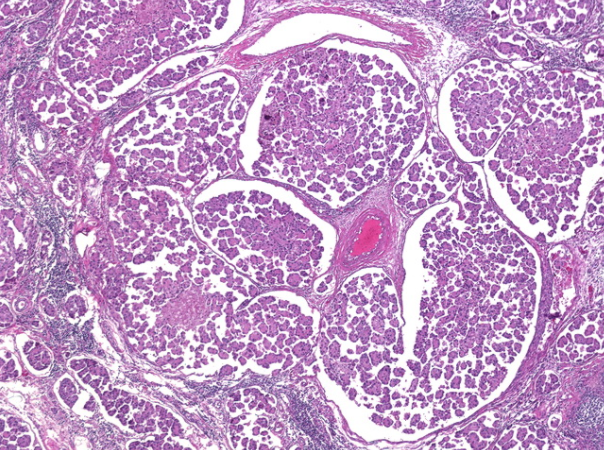
乳腺微乳头状癌:微乳头状簇存在于较大的囊性空间内。
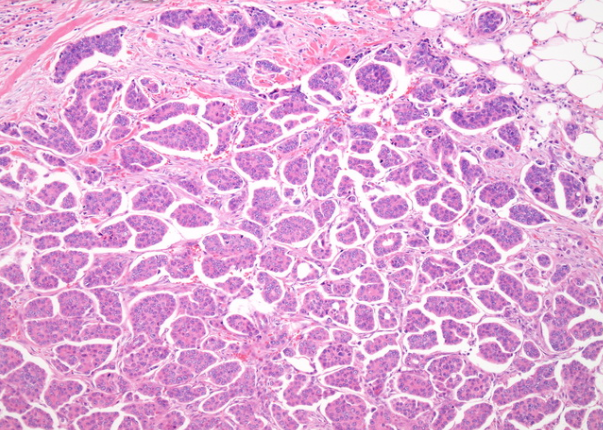
乳头微乳头状癌:肿瘤细胞排列在微乳头状,肾小管-肺泡状或morular簇中,周围被腔隙或透明间隙包围。微乳头状叶缺乏纤维血管核心。腔可能会产生淋巴管侵犯的印象。确实存在真正的淋巴血管浸润。肿瘤细胞具有中等数量的嗜酸性细胞质和高级核,且有丝分裂频繁。微乳头簇中的细胞具有相反的极性
顶端表面极化到外部并与基质接触。该基质通常是结缔组织增生。通常存在微乳头和筛状类型的DCIS。微钙化是常见的。
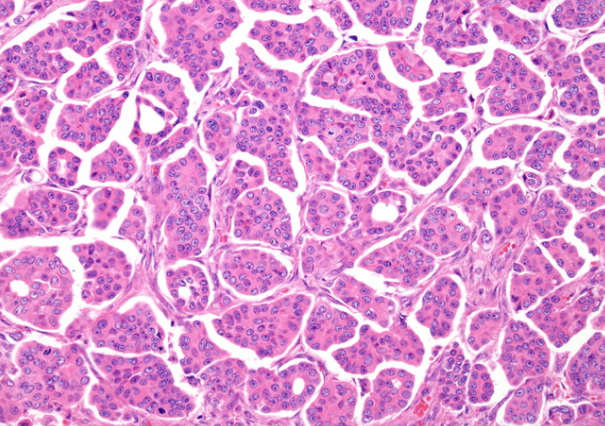
头微乳头状癌:肿瘤细胞排列在微乳头状,肾小管-肺泡状或morular簇中,周围被腔隙或透明间隙包围。微乳头状叶缺乏纤维血管核心。腔可能会产生淋巴管侵犯的印象。确实存在真正的淋巴血管浸润。肿瘤细胞具有中等数量的嗜酸性细胞质和高级核,且有丝分裂频繁。微乳头簇中的细胞具有相反的极性
顶端表面极化到外部并与基质接触。该基质通常是结缔组织增生。通常存在微乳头和筛状类型的DCIS。微钙化是常见的。
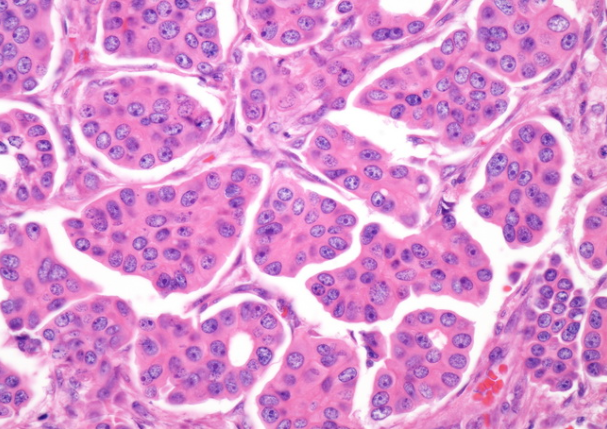
乳头微乳头状癌:肿瘤细胞排列在微乳头状,肾小管-肺泡状或morular簇中,周围被腔隙或透明间隙包围。微乳头状叶缺乏纤维血管核心。腔可能会产生淋巴管侵犯的印象。确实存在真正的淋巴血管浸润。肿瘤细胞具有中等数量的嗜酸性细胞质和高级核,且有丝分裂频繁。微乳头簇中的细胞具有相反的极性
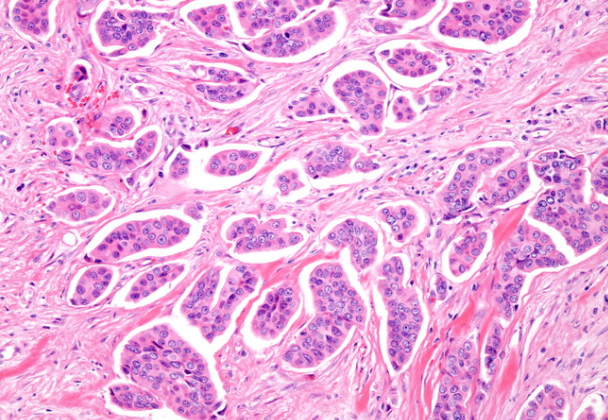
乳腺癌微乳头状癌:该图像显示微乳头状簇被腔隙所包围,并通过增生基质浸润。
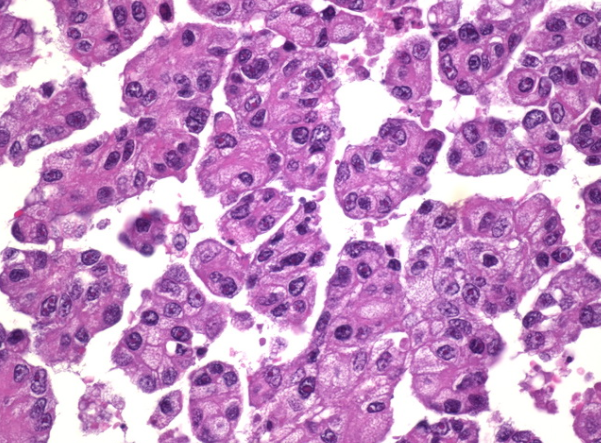
乳腺微乳头状癌是一种侵袭性癌症,由于其倾向于淋巴管浸润,广泛的腋窝淋巴结受累,局部复发和远处转移,因此具有较高的复发率和较短的无病生存期。浸润性粘液癌有时与MPC 共存。必须排除卵巢,肺,胰腺和膀胱原发灶转移至乳腺癌的微乳头状癌。





























































共0条评论