[导读] 作者:慧海拾穗
【前 言】
Glypicans是一个硫酸乙酰肝素蛋白多糖家族,通过糖基磷脂酰肌醇锚定与质膜的胞外表面结合。通过使用硫酸乙酰肝素链,它们可以刺激或抑制生长因子活性,从而接管肝素结合生长因子的共感受器功能。由于glypicans在发育过程中主要以细胞和组织特异性的方式表达,因此在形态发生中起着至关重要的作用。迄今为止,已在哺乳动物中鉴定出glypican基因家族(GPC1-GPC6)的6个成员。
Glypican-3(GPC-3)首先是在Simpson-Golabi-Behmel综合征患者中被发现,这是一种罕见的X连锁疾病,其特征是由GPC-3基因突变引起的产前和产后过度生长。进一步的研究强调了GPC-3在正常发育过程中对细胞增殖和凋亡的调节作用。在一些恶性肿瘤中,包括卵巢癌、胆管癌、间皮瘤和乳腺癌,GPC-3下调(down-regulated )是GPC-3启动子甲基化的结果。由于GPC-3蛋白产物在正常卵巢、乳腺和间皮细胞中高表达,GPC-3被认为是这些器官中的一个抑癌基因。与之相反,其他恶性肿瘤如肝细胞癌(HCC)、胚胎性肿瘤和结肠癌与相应的正常组织相比,GPC-3高表达。因此,GPC-3的功能似乎以组织依赖的方式有所不同。
【肾上腺皮质癌表达glypican-3:潜在的诊断陷阱】
本文报告一例肾上腺皮质癌(ACC)因组织学及GPC-3阳性而误诊为肝癌的病例。患者,男性,52岁,表现为皮质醇升高、全身性高血压、低血钾和高血糖。CT显示实性多叶肿块,增强不均匀,累及右肾上腺和右肝叶。病人接受肾上腺和肝段切除术,手术标本送检。病理组织学申请表没有提供任何临床信息。大体检查发现肿瘤最大径15厘米,部分包裹并浸润肝和肾上腺实质。显微镜下,肿瘤由多角形细胞呈巢状和小梁状分布,胞质嗜酸性或透亮,由纤维血管网分隔。可见广泛出血、坏死区及许多非典型核分裂象(图1a和b)。免疫组化显示肿瘤细胞呈GPC-3(图1c)和HSP-70(图1d)阳性,不表达CK7、谷氨酰胺合成酶、HepPar-1和AFP。根据形态学和免疫表型诊断为肝细胞肝癌。内分泌医生收到病理报告后,转述了他们对肾上腺功能性肿瘤的怀疑。因此,进一步进行免疫组化染色,显示Syn(图1e)、calretinin和α-inhibin(图1f)弥漫阳性,melan-A局灶性阳性,EMA、广谱角蛋白和CgA阴性。根据这些免疫组化结果和所收到的临床资料,该肿瘤最终被诊断为ACC。
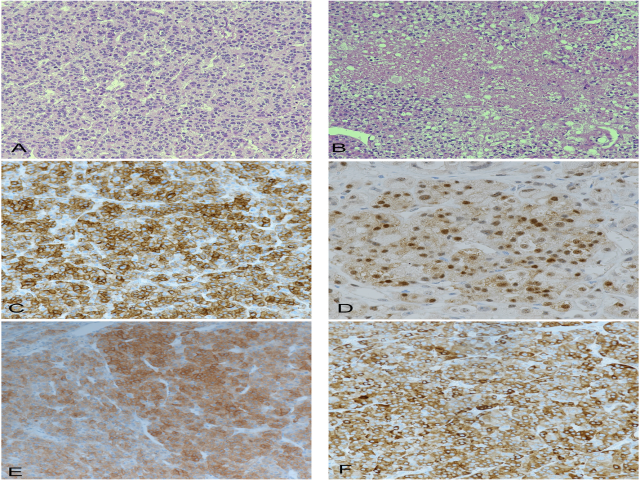
图1:肿瘤由多角形细胞呈巢状和小梁状分布,胞质嗜酸性或透亮,由纤维血管网分隔。可见广泛出血、坏死区及许多非典型核分裂象(A和B)。瘤细胞GPC-3胞质弥漫阳性(C)、 HSP-70核质阳性(D)、 Syn(E)和α-inhibin(F)弥漫阳性。
ACC可起源于异位于肝脏的肾上腺皮质组织,但也可能直接从右肾上腺延伸到肝脏,甚至转移到肝脏。在所有这些情况下,ACC需要与HCC区别开来。仅根据组织病理学发现,鉴别诊断可能具有挑战性。事实上,两种肿瘤都可能显示肿瘤细胞具有核异型性和胞质嗜酸性/透亮,呈小梁状排列。在本例中,单纯以肝癌为靶点的免疫组化和GPC-3的阳性进一步误导,导致肝癌的首次诊断。本例因Syn、α-inhibin和melan-A染色呈阳性而最终得到了正确的诊断。一般来说,GPC-3可在肾上腺皮质腺瘤(6/10)中表达,很少或罕见ACC病例表达。然而,尽管不常见,但ACC能表达GPC-3的可能性应该被记住,以避免因依赖免疫组化结果而错误诊断。需要提醒的是,除了免疫组化结果的陷阱外,病理医生还要关注临床信息。对于申请单空白现象在很多医院都可能存在,病理医生不能因此而“凭空想象”。
【参考文献】
[1] Immunohistochemical expression of glypican-3 in adrenocortical carcinoma: A potential cause of diagnostic pitfalls.2018.
[2] Three cases of adrenocortical tumors mistaken for hepatocellular
carcinomas/diagnostic pitfalls and differential diagnosis.2017.














共0条评论