[导读] 2018年,在结直肠癌(CRC)的药物治疗领域,虽无能够改变临床实践的重大研究发布,但在药物治疗和围手术期治疗等方面也看到了进步。本文将以大型会议的报道及重要期刊上的文献作为基础,梳理2018年在CRC治疗领域的进展。
文丨王正航 王晰程 李健 沈琳 北京大学肿瘤医院消化肿瘤内科
来源丨医学界肿瘤频道
一线治疗
免疫治疗
目前缺乏免疫检查点抑制剂在错配修复蛋白功能缺失(dMMR)/微卫星高度不稳定(MSI-H)CRC一线中的疗效,另外,纳武利尤单抗+Ipilimumab联合方案因不良反应大而可能会影响这一策略的推广。
Checkmate-142研究探索了一线使用纳武利尤单抗(Nivolumab)+Ipilimumab的疗效[1]。本研究客观缓解率(ORR)为60%,疾病控制率(DCR)为84%,中位无进展生存期(PFS)和总生存期(OS)均未达到,12个月PFS和12个月OS分别为为77%和83%。3-4级不良反应发生率为16%。肠癌一线联合免疫治疗的ORR较为可观,但对生存期的影响仍需要继续观察。
特别强调的是,传统双药联合(Ipilimumab 3mg/kg q3w)治疗的3-4级不良反应发生率为30%-40%,而本研究将Ipilimumab的剂量下调为1mg/kg q6w,发现3-4级不良反应的发生率降为16%(与纳武利尤单抗单药发生率类似)。这一剂量调整在保证疗效的同时,大大减少了不良反应的发生,使其临床应用成为可能。
但dMMR/MSI-H仅占转移性CRC(mCRC )的5%;对于剩下的95%的错配修复蛋白功能完整(pMMR)/微卫星稳定(MSS)患者,单药免疫治疗几乎无效。那么,免疫治疗联合其他治疗是否可能有效?
前期的机制研究证明,免疫治疗联合抗血管内皮生长因子(VEGF)治疗或MEK抑制剂尚能改善免疫抑制状态,提高免疫治疗的疗效。但MODUL研究证明阿特珠单抗(Atezolizumab)联合贝伐珠单抗+化疗在一线治疗中不优于贝伐珠单抗+化疗[2];IMBlaze370研究同样未能证明阿特珠单抗+MEK抑制剂在三线治疗中获益[3]。这两项临床研究的失败,使MSS结直肠癌免疫治疗之路更为艰难。
化疗联合靶向治疗
对于不适合免疫治疗的患者,一线治疗应该如何选择?FOLFOXIRI(5-氟尿嘧啶+奥沙利铂+亚叶酸钙+伊立替康)+贝伐珠单抗在ORR、PFS和OS方面优于FOLFOX(5-氟尿嘧啶+奥沙利铂+亚叶酸钙)或FOLFIRI(5-氟尿嘧啶+伊立替康+亚叶酸钙)联合贝伐珠单抗[4]。但这些研究并未严格设计一线进展后的二线治疗方案,因此,“初始三药是否优于序贯两药”还没有答案。
TRIBE2研究对比了初始使用三药联合化疗与按计划依次使用三药的疗效[5](下图)。A组(FOLFOX联合贝伐珠单抗进展后,应用FOLFIRI联合贝伐珠单抗)和B组(FOLFOXIRI联合贝伐珠单抗)的一线PFS和二线PFS分别为9.9月 vs 12月(P<0.001)和5.5月 vs 6.0月(P=0.120),PFS2[随机至疾病进展(PD)2的时间]分别为16.2月 vs 18.9月(P<0.001),ORR分别为50% vs 61%(P=0.005)。但≥3级腹泻、中性粒细胞减少和中性粒细胞缺乏伴发热(粒缺发热)在B组中更高。
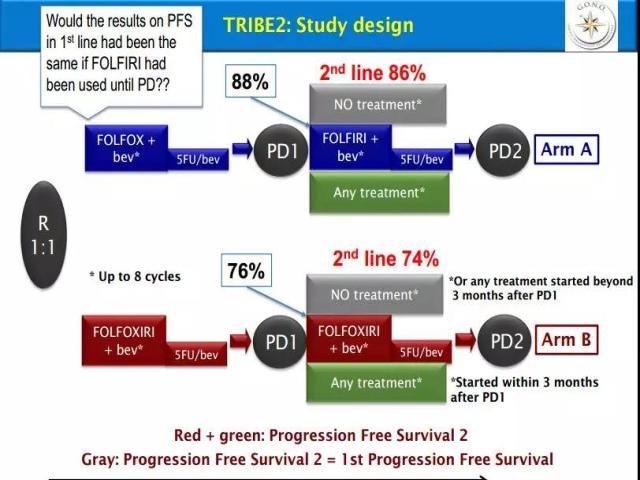
图1:TRIBE2研究设计
三药联合抗表皮生长因子受体(EGFR)治疗尚缺乏数据。VOLFI研究则探索了FOLFOXIRI+帕尼单抗(帕尼单抗组)对比FOLFOXIRI (对照组)一线治疗RAS野生型CRC的疗效与安全性[6]。
在左半CRC中,帕尼单抗组和对照组的ORR分别为90.6% vs 68%(P=0.02);而对于右半结肠,虽然病例数很少,未见统计学差异,但有效率仍有明显提高;BRAF突变型患者,帕尼单抗组ORR也明显提高。
但值得注意的是,对于不可切除的患者以及BRAF突变的患者,两组的PFS分别为9.0月 vs 10.7月(P=0.35)和6.5月 vs 6.1月(P=0.57)。3-5级不良事件在两组中分别为81.3% vs 66.7%。
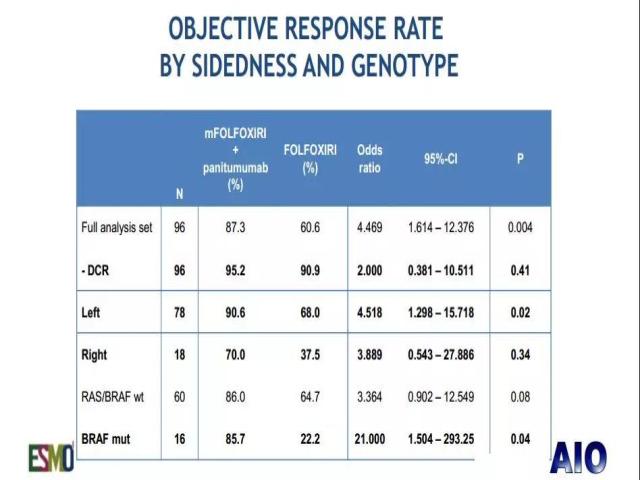
图2:VOLFI研究中,不同侧和基因型CRC的ORR
三药化疗联合靶向治疗高效但也带来高毒性,所以在临床实践中,这样强力的治疗方案仅被用于身体状况很好、耐受性较强的特定人群,如需要转化治疗或肿瘤负荷大的患者。对于该人群,降低肿瘤负荷是争取手术机会和改善生活质量的主要手段,可以考虑首选这些ORR高的方案[6]。
而对于以控制疾病、延缓肿瘤进展为目的的姑息治疗而言,需要考量毒性和生存期的平衡。对于BRAF突变的患者,因为其生物学行为差,故建议予以强烈治疗;肿瘤负荷量很大、发展迅速者,可以考虑上述三药化疗联合EGFR单抗,来迅速控制肿瘤、减轻症状;但由于生存状况没有改善,所以需要慎重考虑,目前欧洲肿瘤内科学会(ESMO)共识建议予以FOLFOXIRI±贝伐珠单抗。今年在Annuals of Oncology上发表的TRIBE的回顾性分析发现,BRAF突变的右半CRC也许更能从三药+贝伐珠单抗治疗中获益[7]。
抗EGFR治疗后的维持治疗
对于一线抗EGFR治疗失败的患者,如何选择后续治疗?仍缺乏证据。MACRO2 TTD研究(II期)证明西妥昔单抗不劣于西妥昔单抗+化疗(未分左右半)[8];VALENTINO研究证明帕尼单抗劣于帕尼单抗+化疗(无论是左半CRC还是右半CRC)[9];另一项研究证明西妥昔单抗等同于贝伐珠单抗(未分左右半)[10]。
对于一线使用抗EGFR治疗未PD的患者,目前有三种维持治疗策略:(1)继续使用抗EGFR+化疗维持,(2)换用抗VEGF+化疗维持,(3)单纯化疗维持,(4)暂停治疗。现有证据较少,且均为来自于西方人群的数据,因而临床实践中尚未推荐使用EGFR单抗作为常规维持治疗,最优的维持方案仍需要进一步的探索。
二线及后线的靶向治疗选择
贝伐珠单抗失败后的选择
对于一线贝伐珠单抗失败后,UNICANCER PRODIGE18研究发现继续使用贝伐珠单抗比换用西妥昔单抗有延长PFS和OS的趋势[11]。E7208研究发现联合使用伊立替康+西妥昔单抗+雷莫芦单抗在PFS方面优于伊立替康+西妥昔单抗[12]。另一项研究发现帕尼单抗在OS方面优于西妥昔单抗[13]。
REVERCE研究针对未使用抗EGFR治疗的人群,探索了抗VEGF和抗EGFR的优先次序(共96%-98%患者使用过贝伐珠单抗)[14]。研究并未明确具体的治疗线数,但从“使用过3种化疗药”的入组条件推断,应该大多数患者为≥3线治疗。发现R-C组(瑞戈非尼-西妥昔单抗)和C-R组(顺序相反)的OS分别为17.4月和11.6月(P=0.029),R-C组OS的优势主要来源于PFS2(5.2月 vs 1.8月)。原因可能为西妥昔单抗治疗后基因突变率明显升高——这可能与肿瘤生物学行为的恶化有关[15]。
对于RAS/BRAF野生型的患者,贝伐珠单抗进展后靶向治疗的选择始终缺乏定论。继续使用贝伐珠单抗还是换用瑞戈非尼,抑或使用抗EGFR单抗,目前的研究数据较少,且缺乏左右半亚组的前瞻性分析,因此对于临床实践的指导价值有限。我们期望更多的临床数据和基础研究能够阐明抗EGFR和抗VEGF治疗的究竟应如何使用。
抗EGFR失败后的选择
抗EGFR失败后能否以及何时再次使用抗EGFR治疗尚无定论。
一项研究通过检测ctDNA,发现停用抗EGFR后,RAS突变克隆和EGFR突变克隆(二者均为耐药克隆)呈指数衰减[16]。这些结果提示,当使用抗EGFR治疗进展后,间隔的使用时间可能为10-15月。
另一项研究探索了三线再次使用伊立替康+西妥昔单抗的疗效[17],结果显示:25人的ctDNA是可评估的,12人为RAS突变。部分缓解(PR)患者中,均未检测到RAS突变。RAS野生型者PFS(4.0月)明显长于RAS突变者(1.9个)。
这些结果提示,对于使用抗EGFR治疗进展的患者——无论是已停用抗EGFR治疗还是治疗中进展,在再次使用之前,需考虑ctDNA或再活检来检测RAS状况来协助指导治疗决策。
少见靶点的治疗策略
抗HER2治疗
HER2扩增患者不到mCRC的5%。并非所有HER2扩增的患者均能从抗HER2治疗中获益。
HERACLES的研究者发现,无论是组织还是ctDNA,基于新一代基因测序技术(NGS)检测出的HER2基因拷贝数较高的人群更容易从治疗中获益[18]。
NTRK基因融合
随着诊断技术和药物研发的进步,也有很多少见变异成为了CRC的治疗靶点。
2018年,LOXO-101(Larotrectinib)被FDA批准用于NTRK基因融合的实体瘤。在全体实体瘤中的有效率为75%,其中共纳入4例结肠癌患者,其中2人病情稳定(SD),2人PR[19]。
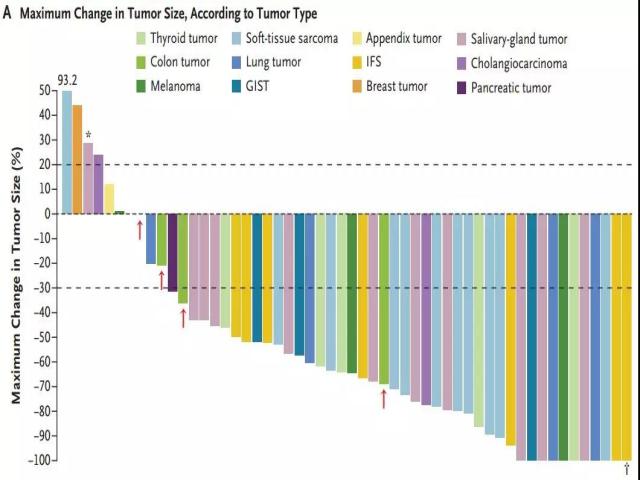
图3:不同类型肿瘤接受LOXO-101治疗后的肿瘤大小变化
NTRK基因融合的发生率极低:基于肿瘤组织的NGS数据显示,肠癌中NTRK基因融合的发生率在国外仅有0.05%-0.31%(3/978)[20,21];在中国人群中的发生率可能稍高,为1.4%[22]。尽管这些特殊类型的基因改变发生率极低,但这类人群从新的靶向药物中获益率极高。
此外,基因融合的患者更有可能是MSI-H[21]或肿瘤突变负荷(TMB)更高[23](但样本量较小,结论可信度下降),NTRK融合者若为MSI-H,应首选免疫治疗还是靶向治疗?这仍需要更多的临床数据。
围手术期治疗
结肠癌新辅助免疫治疗
NICHE研究探索非转移性肠癌术前予以Ipilimumab 1mg/kg d1+纳武利尤单抗 3mg/kg d1 d15的安全性和可行性[24]。结果发现这一策略是安全可行的。dMMR患者均有明显的肿瘤退缩。而pMMR患者的肿瘤退缩不明显。
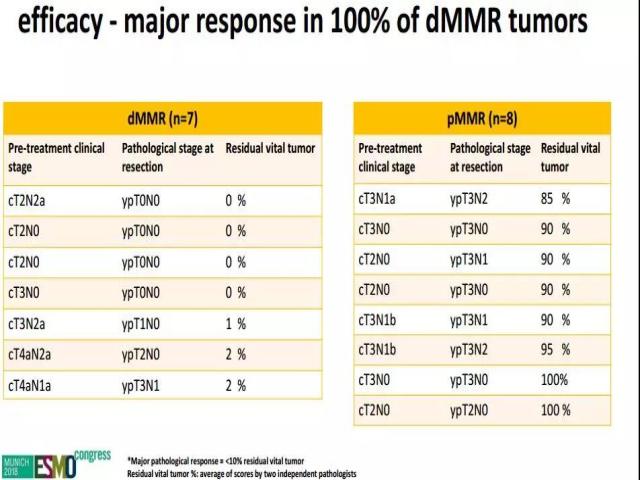
图4:NICHE研究中,dMMR和pMMR患者的缓解情况
dMMR的结肠癌术前经联合免疫治疗后退缩极为明显(0-2%),这为手术困难(如T4b)的患者、重要脏器保留(如需要保肛)的患者带来了希望和新的选择。但是,围手术期免疫治疗是否具有改善生存的意义仍不得而知。I-II期的患者预后本身就很好,可能不需要围手术期治疗;III期患者手术前使用免疫治疗似乎更合理,但需要更多证据支持。
直肠癌辅助治疗
对于接受术前同步放化疗的直肠癌而言,术后治疗应该如何选择?目前推荐意见来自于结肠癌研究的外延,而缺乏直肠癌人群的直接数据。
ADORE研究的人群为经同步放化疗后达到ypII-III期的cT3-4或N+直肠癌,术后予以FOLFOX或5-氟尿嘧啶/亚叶酸钙辅助化疗[25]。结果发现FOLFOX组的6年无病生存率(DFS)优于5-氟尿嘧啶/亚叶酸钙组(68.2% vs 56.8%)(达到主要研究终点),两组的6年OS率无显著差异。在预设亚组分析中,发现奥沙利铂可以提高ypIII期患者的6年DFS率,但无法提高ypII期患者的。
本研究的最大亮点在于根据新辅助化疗后的病理分期来探索辅助化疗方案,提示对于ypII期的患者,似乎术后使用单药化疗是足够的。但对于初始II-III期、ypI期的患者,辅助治疗应如何选择,目前仍未得到回答。
腹膜转移手术切除后腹腔热灌注化疗
累及范围较少的腹膜转移可能也属于“寡转移”范畴,肿瘤减灭术联合腹腔热灌注化疗(HIPEC)优于单纯的静脉化疗。但对于这部分患者,HIPEC是否是必须的?目前不得而知。
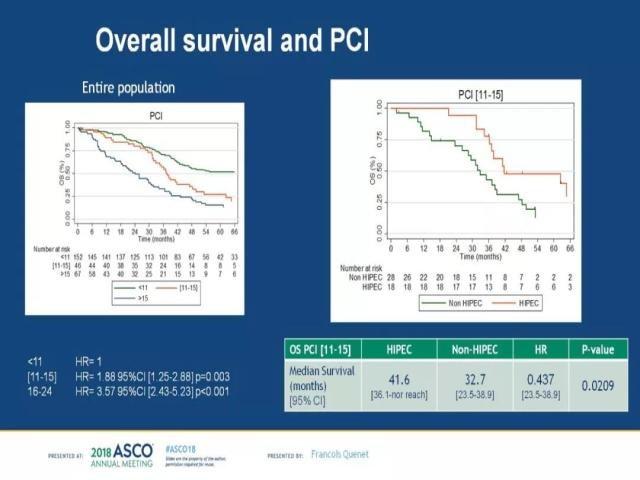
PRODIGE 7研究纳入了仅有腹膜转移的人群,对比肿瘤减灭术+HIPEC和仅行肿瘤减灭术的疗效差别,发现对于总人群两种方式OS相当,但是对于PCI(腹膜肿瘤指数)评分11-15的人群,HIPEC组OS优于单纯减灭术组,而对于PCI<11或>15的人群,两组OS无差别[26]。
这一结论提示:若肿瘤负荷较小,过强的治疗是不必要的。若肿瘤负荷较大(反应肿瘤生物学行为差),单纯加强局部治疗是不够的,加强全身系统治疗能否改善预后仍不得而知。
ctDNA指导治疗
如何更加精准地确定需要辅助治疗的人群始终是难点问题。既往已报道了ctDNA在肝转移术后、局部进展期直肠癌术后以及II期结肠癌术后的作用。
ASCO 2018上又报道了III结肠癌术后ctDNA的持续阳性与较高的复发风险相关,且发现ctDNA的变化可以预测辅助治疗的疗效[27]。
越来越多的证据表明,ctDNA在肿瘤的治疗领域起着重要的作用,TNMB时代已经到来,我们期待更多基于ctDNA进行的临床研究最终能够确定其对于治疗的指导价值。
综合治疗理念的提升
肝和肺是CRC最常见的转移部位。今年《中国结直肠癌肝转移诊断和综合治疗指南》进行了更新[28],同时,我国也发布了全球首个肺转移治疗共识——《结直肠癌肺转移多学科综合治疗专家共识》[29]。这都为我国CRC患者的综合管理带来了新的视野和契机。
专家简介





参考文献
[1]Lenz H-JJ, Van Cutsem E, Limon ML, et al. Durable clinical benefit with nivolumab (NIVO) plus low-dose ipilimumab (IPI) as first-line therapy in microsatellite instability-high/mismatch repair deficient (MSI-H/dMMR) metastatic colorectal cancer (mCRC)[J]. Annals of Oncology,2018,29:LBA18_PR.
[2]Grothey A, Tabernero J, Arnold D, et al. Fluoropyrimidine (FP) + bevacizumab (BEV) + atezolizumab vs FP/BEV in BRAFwt metastatic colorectal cancer (mCRC): Findings from Cohort 2 of MODUL – a multicentre, randomized trial of biomarker-driven maintenance treatment following first-line induction therapy[J]. Annals of Oncology,2018,29:LBA19.
[3]Bendell J, Ciardiello F, Tabernero J, et al. Efficacy and safety results from IMblaze370, a randomised Phase III study comparing atezolizumab+cobimetinib and atezolizumab monotherapy vs regorafenib in chemotherapy-refractory metastatic colorectal cancer[J]. Annals of Oncology,2018,29:LBA004.
[4]Shui L, Wu YS, Lin H, et al. Triplet Chemotherapy (FOLFOXIRI) Plus Bevacizumab Versus Doublet Chemotherapy (FOLFOX/FOLFIRI) Plus Bevacizumab in Conversion Therapy for Metastatic Colorectal Cancer: a Meta-Analysis[J]. Cellular physiology and biochemistry : international journal of experimental cellular physiology, biochemistry, and pharmacology,2018,48:1870-1881.
[5]Cremolini C, Antoniotti C, Lonardi S, et al. TRIBE2: A phase III, randomized strategy study by GONO in the 1st- and 2nd-line treatment of unresectable metastatic colorectal cancer (mCRC) patients (pts)[J]. Annals of Oncology, ,2018,29:LBA20.
[6]Geissler M, Klingler T, Knorrenschild JR, et al. 1st-line mFOLFOXIRI + panitumumab vs FOLFOXIRI treatment of RAS wt mCRC: A randomized phase II VOLFI trial of the AIO (KRK-0109)[J]. Annals of Oncology,2018,29:453PD.
[7]Cremolini C, Antoniotti C, Lonardi S, et al. Primary tumor sidedness and benefit from FOLFOXIRI plus bevacizumab as initial therapy for metastatic colorectal cancer. Retrospective analysis of the TRIBE trial by GONO.[J]. Annals of oncology : official journal of the European Society for Medical Oncology,2018,29:1528–1534.
[8]Aranda E, Garcia-Alfonso P, Benavides M, et al. First-line mFOLFOX plus cetuximab followed by mFOLFOX plus cetuximab or single-agent cetuximab as maintenance therapy in patients with metastatic colorectal cancer: Phase II randomised MACRO2 TTD study[J]. European journal of cancer,2018,101:263-272.
[9]Morano F, Corallo S, Bartolomeo M, Di., et al. Negative hyper-selection of RAS wild-type (wt) metastatic colorectal cancer (mCRC) patients randomized to first-line FOLFOX plus panitumumab (Pan) followed by maintenance therapy with either 5FU/LV plus pan or single-agent pan: Translational analyses of the VALENTINO study[J]. Annals of Oncology,2018,29:LBA22.
[10]Cremolini C, Antoniotti C, Lonardi S, et al. Activity and Safety of Cetuximab Plus Modified FOLFOXIRI Followed by Maintenance With Cetuximab or Bevacizumab for RAS and BRAF Wild-type Metastatic Colorectal Cancer: A Randomized Phase 2 Clinical Trial[J]. JAMA oncology,2018,4:529-536.
[11]Bennouna J, Hiret S, Bertaut A, et al. Continuation of Bevacizumab vs Cetuximab Plus Chemotherapy After First Progression in KRAS Wild-Type Metastatic Colorectal Cancer: The UNICANCER PRODIGE18 Randomized Clinical Trial[J]. JAMA oncology,2018.
[12]Hochster HS, Catalano PJ, O'Dwyer PJ, et al. Randomized trial of irinotecan and cetuximab (IC) versus irinotecan, cetuximab and ramucirumab (ICR) as 2nd line therapy of advanced colorectal cancer (CRC) following oxaliplatin and bevacizumb based therapy: Result of E7208[J]. Journal of Clinical Oncology,2018,36:3504.
[13]Taniguchi H, Yamanaka T, Sakai D, et al. Influence of treatment with prior bevacizumab: A combined analysis of individual patient data from ASPECCT and WJOG6510G trial which compared panitumumab versus cetuximab in patients with wild-type KRAS exon 2 metastatic colorectal cancer[J]. Annals of Oncology,2018,29:454PD.
[14]Shitara K, Yamanaka T, Denda T, et al. Reverce: Randomized phase II study of regorafenib followed by cetuximab versus the reverse sequence for metastatic colorectal cancer patients previously treated with fluoropyrimidine, oxaliplatin, and irinotecan.[J]. Journal of Clinical Oncology 2018,36:557.
[15]Tsuji Y, Shitara K, Yamanaka T, et al. REVERCE: Randomized phase II study of regorafenib followed by cetuximab versus the reverse sequence for metastatic colorectal cancer patients previously treated with fluoropyrimidine, oxaliplatin, and irinotecan-Biomarker analysis.[J]. Journal of Clinical Oncology,2018,36:3510.
[16]Parseghian CM, Loree JM, Morris VK, et al. Anti-EGFR resistant clones decay exponentially after progression: Implications for anti-EGFR rechallenge[J]. Journal of Clinical Oncology,2018,36:3511.
[17]Cremolini C, Rossini D, Dell'Aquila E, et al. Rechallenge for Patients With RAS and BRAF Wild-Type Metastatic Colorectal Cancer With Acquired Resistance to First-line Cetuximab and Irinotecan: A Phase 2 Single-Arm Clinical Trial[J]. JAMA oncology,2018.
[18]Bardelli A, Siravegna G, Sartore-Bianchi A, et al. Plasma HER2 (ERBB2) copy number to predict response to HER2-targeted therapy in metastatic colorectal cancer[J]. Journal of Clinical Oncology,2018,36:3506.
[19]Drilon A, Laetsch TW, Kummar S, et al. Efficacy of Larotrectinib in TRK Fusion-Positive Cancers in Adults and Children[J]. The New England journal of medicine,2018,378:731-739.
[20]Zehir A, Benayed R, Shah RH, et al. Mutational landscape of metastatic cancer revealed from prospective clinical sequencing of 10,000 patients[J]. Nature medicine,2017,23:703-713.
[21]Rankin A, Klempner SJ, Erlich R, et al. Broad Detection of Alterations Predicted to Confer Lack of Benefit From EGFR Antibodies or Sensitivity to Targeted Therapy in Advanced Colorectal Cancer[J]. The oncologist,2016,21:1306-1314.
[22]Ling Q, Li B, Wu X, et al. The landscape of NTRK fusions in Chinese patients with solid tumor[J]. Annals of Oncology,2018,29:75P.
[23]Clifton K, Raymond VM, Dasari A, et al. Actionable fusions in colorectal cancer using a cell-free circulating tumor DNA (ctDNA) assay[J]. Journal of Clinical Oncology,2018,36:3507.
[24]M. Chalabi, L. F. Fanchi, J. G. Van den Berg, et al. Neoadjuvant ipilimumab plus nivolumab in early stage colon cancer[J]. Annals of Oncology,2018,29:LBA37_PR.
[25]Hong YS, Kim SY, Lee JS, et al. Long-term results of the ADORE trial: Adjuvant oxaliplatin, leucovorin, and 5-fluorouracil (FOLFOX) versus 5-fluorouracil and leucovorin (FL) after preoperative chemoradiotherapy and surgery for locally advanced rectal cancer.[J]. Journal of Clinical Oncology,2018,36:3501.
[26]Quenet F, Elias D, Roca L, et al. A UNICANCER phase III trial of hyperthermic intra-peritoneal chemotherapy (HIPEC) for colorectal peritoneal carcinomatosis (PC): PRODIGE 7[J]. Journal of Clinical Oncology,2018,36:3503.
[27]Tie J, Cohen J, Wang Y, et al. Serial circulating tumor DNA (ctDNA) analysis as a prognostic marker and a real-time indicator of adjuvant chemotherapy (CT) efficacy in stage III colon cancer (CC)[J]. Journal of Clinical Oncology,2018,36:3516.
[28]中华医学会外科学分会胃肠外科学组, 中华医学会外科学分会结直肠外科学组, 中国抗癌协会大肠癌专业委员会, et al. 中国结直肠癌肝转移诊断和综合治疗指南(2018版)[J]. 中华消化外科杂志,2018,17:527-539.
[29]中国医师协会外科医师分会多学科综合治疗专业委员会,中国抗癌协会大肠癌专业委员会. 结直肠癌肺转移多学科综合治疗专家共识(2018版)[J]. 肿瘤综合治疗电子杂志,2018,4:1-15.























共0条评论