编译整理:强子
见微知遗传:部分遗传性肾癌的病理特点(一)
见微知遗传:部分遗传性肾癌的病理特点(二)
见微知遗传:部分遗传性肾癌的病理特点(四)
遗传性平滑肌瘤病及肾细胞癌综合征
遗传性平滑肌瘤病及肾细胞癌(hereditary leiomyomatosis and renal cell carcinoma, HLRCC)综合征是一种常染色体显性遗传疾病,因延胡索酸水化酶(fumaratehydratase,FH)基因胚系突变所致,该基因异常使得患者发生皮肤平滑肌瘤及子宫平滑肌瘤的风险增加。据估计,FH突变携带者一生发生肾癌的风险为15%;文献中患者发病年龄平均为41岁。报道中的HLRCC相关肾细胞癌大部分均为高度侵袭性,患者常表现为局部进展期病变或远处转移,且预后较差。不过,随着病理诊断的进展,已有形态学特征为低级别的FH缺陷型肾细胞癌的报道,这表明HLRCC综合征相关肾细胞癌可能比此前认为的临床谱系、形态学谱系要宽泛的多。
与前述VHL综合征或乳头状肾细胞癌病例不同,HLRCC相关肾脏肿瘤多为单侧、单发,因此仅从临床很难与散发性肿瘤鉴别。尽管皮肤平滑肌瘤或子宫平滑肌瘤相比肾脏肿瘤出现的几率要高,但日常临床实践中这类肾外表现或相关病史容易被忽略。因此病理检查在这类患者的诊断、及患者家属相应的管理方面具有重要意义。不过,由于病理诊断中一般并未经遗传学证实,因此建议应用“FH缺陷型肾细胞癌”来形容HLRCC相关肾细胞癌及罕见的体细胞性FH缺陷型肾细胞癌。
1.大体特征
HLRCC相关的肾细胞癌主要为单侧、单发肿瘤。大体特点可多种多样:大部分为实性、均质表现,但有些为囊性,或伴出血、坏死灶。部分肿瘤似发生自囊壁,形成附壁结节。肿瘤周围肾实质一般无显著异常,部分病例偶见囊肿形成。
2.镜下特点
肿瘤结构上包括诸多形态,如乳头状、管状、管状囊性、实性、囊性等,局灶可类似集合管癌或管状囊性癌。也曾有过肉瘤样分化的报道。具体到某一肿瘤,常见多种结构混合。需要指出的是,最近有多单位相关研究指出,伴低分化灶的管状囊性癌中高达70%至80%实际为FH缺陷型肾细胞癌;但目前尚不清楚其中有多少是伴FH胚系突变的真正HLRCC相关肾细胞癌。
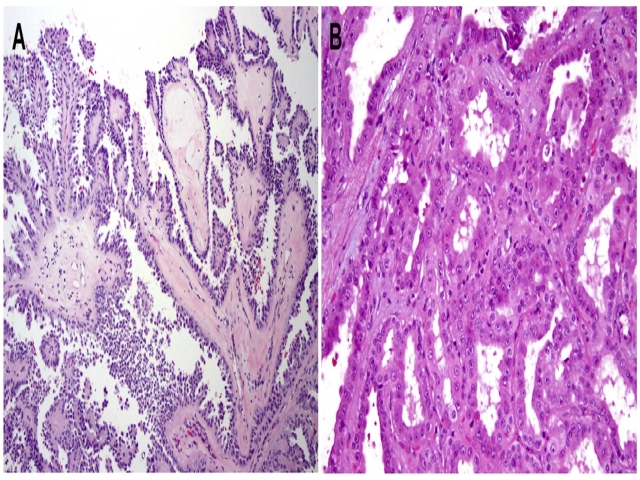
图1. HLRCC相关肾细胞癌的结构表现:乳头状(左)、管状(右)。
细胞学上,HLRCC相关肾细胞癌最具特征性的是由Merino等最初描述的“玫红色”巨细胞病毒包涵体样核仁,周围可见空泡。不过,部分病例中这一特点仅局灶存在。最近描述的FH缺陷型、低级别肾脏肿瘤中,少数病例完全没有这一特点。
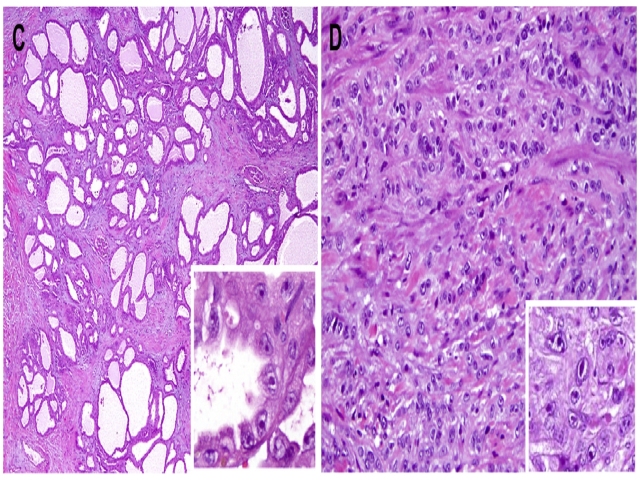
图2. HLRCC相关肾细胞癌的结构表现:管状囊性(左)、实性(右)。其中插图均示特征性的“玫红色”核仁,核旁可见空泡。
免疫组化该肿瘤大部分病例瘤细胞FH表达缺失,但肿瘤内的血管内皮细胞或炎细胞仍偶表达,可作为阳性内对照。需要指出的是,少数经证实的HLRCC肿瘤仍会有FH的弱阳性、甚至强阳性,推测可能是由于有缺陷的FH蛋白仍有着色所致。相反,免疫组化S-(2-succino)-cysteine(2SC)对于FH缺陷型肿瘤中的蛋白异常高度敏感、特异。出现弥漫性细胞核及细胞质着色时,与FH突变之间高度相关。不过,诊断FH缺陷的时候,仅胞质着色而无胞核着色、或仅有复染时着色而呈现“胞核蓝色”的情况,不要判读为2SC阳性。
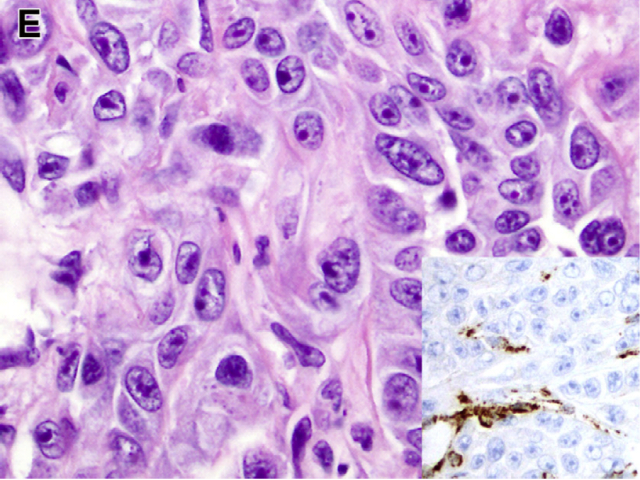
图3. HLRCC相关肾细胞癌中的肉瘤样表现;插图示免疫组化FH不表达,其中内皮细胞、间质及炎症细胞可作为阳性内对照。
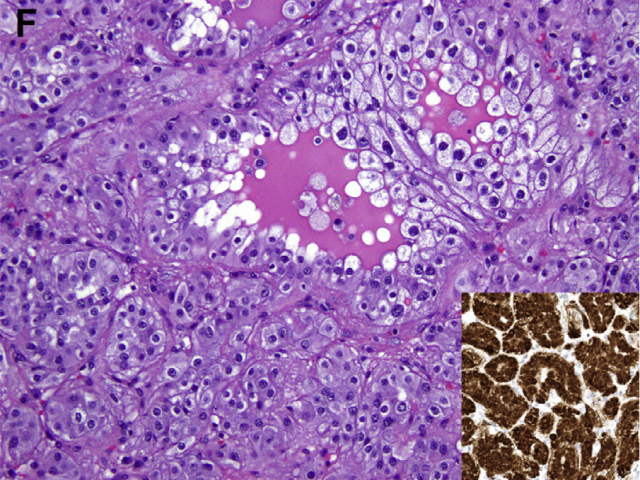
图4. FH缺陷型、低级别肾脏肿瘤中,缺乏显著核仁;插图为免疫组化2SC强阳性,证实FH缺陷。
3.鉴别诊断
HLRCC相关肾细胞癌的鉴别诊断主要有2型乳头状肾细胞癌、集合管癌、管状囊性癌、其他高级别未分类肾细胞癌。HLRCC相关肾细胞癌中显著乳头状结构可能会考虑到2型乳头状肾细胞癌,实际上文献中很多HLRCC相关肿瘤也的确被归为了2型乳头状肾细胞癌。重要的是应意识到,2型乳头状肾细胞癌是形态学及分子水平均有异质性的一组肿瘤。由于HLRCC相关肿瘤相比乳头状肾细胞癌来说,侵袭性更强,因此还是应尽量鉴别开来。2型乳头状肾细胞癌一般境界清楚,常有显著包膜。肿瘤边缘呈浸润性时,应想到其他可能,如HLRCC相关肾细胞癌。HLRCC相关肾细胞癌中具有特征性的细胞核,即使仅局灶存在也对确诊很有帮助。免疫组化2SC及FH可证实FH缺陷型肾细胞癌的诊断。
集合管癌罕见,极具侵袭性,常见于肾髓质。其组织学特点为伴管状及管状乳头状结构的高级别腺癌,具有促纤维性间质。不过,部分集合管癌可以乳头状结构为主。由于集合管癌样生长常见于HLRCC相关肾细胞癌中,因此集合管癌应排除包括HLRCC相关肾细胞癌在内的其他可能后方可诊断。
按照最新版世界卫生组织分类,管状囊性癌应仅限于形态学典型者,即:肿瘤境界清楚,完全由大小不等的管状结构及囊腔构成,囊壁内衬细胞靴钉状,胞质嗜酸性,核仁中等至较大。对于具有管状囊性癌样组织学特点、并有低分化区域的病例,一定要通过辅助检查或分子检测排除FH缺陷型肾细胞癌的可能。
HLRCC相关肾细胞癌中还可见其他组织学特征,如筛状结构、筛孔状的显著空泡、透明细胞特点、肉瘤样分化等,因此需和其他多种肿瘤鉴别,包括肾髓质癌、Xp11或t(6,11)易位性肾细胞癌、高级别透明细胞型肾细胞癌、高级别未分类肾细胞癌。临床特点(如红细胞的镰刀样)及细胞核不表达INI1,支持肾髓质癌的诊断;而TFE3或TFEB易位肿瘤的诊断则需免疫组化或荧光原位杂交检测结果的支持。HLRCC相关肾细胞癌与其他具有非典型特征的高级别肾细胞癌鉴别,则主要依靠免疫组化FH和/或2SC的相关结果。
4.诊断要点
由于HLRCC相关肾细胞癌的临床及病理表现宽泛,因此其确诊主要依靠病理医师遇到临床及病理特点不同寻常病例时考虑到HLRCC相关肾细胞癌的可能,并进一步证实。出现显著核仁、核周空泡,哪怕仅是局灶性,也应注意进行FH和/或2SC的免疫组化检测。最终确诊HLRCC相关肾细胞癌则依靠遗传学检测,证实有FH基因的胚系突变才可以最终明确。
5.预后
文献中报道的HLRCC相关肾细胞癌病例,大部分预后均较差,较小肿瘤也有早期转移的报道。常见转移部位有局部淋巴结、肾上腺、肺、肝、骨。目前,对转移性肿瘤尚无公认的系统治疗方案。针对血管内皮生长因子和/或表皮生长因子受体的抑制剂相关临床试验,以及针对代谢异常的相关临床试验,均正在进行中。一般建议对于这些患者家庭成员、及肾癌患者进行遗传学会诊,但是否进行遗传学检测、以及后续随访等,应具体分析。
点击下载英文文献
参考文献
Yu-ChingPeng, Ying-Bei Chen. Recognizing Hereditary Renal Cancers Through the Microscope: A Pathology Update[J].Surgical pathology clinics,2018,11(4):725-737.
DOI:10.1016/j.path.2018.07.010

















共0条评论