作者:易树华1,2 邹德慧1 Ken He,Young2 邱录贵1
1.中国医学科学院血液病医院;2.美国MD安德森癌症中心
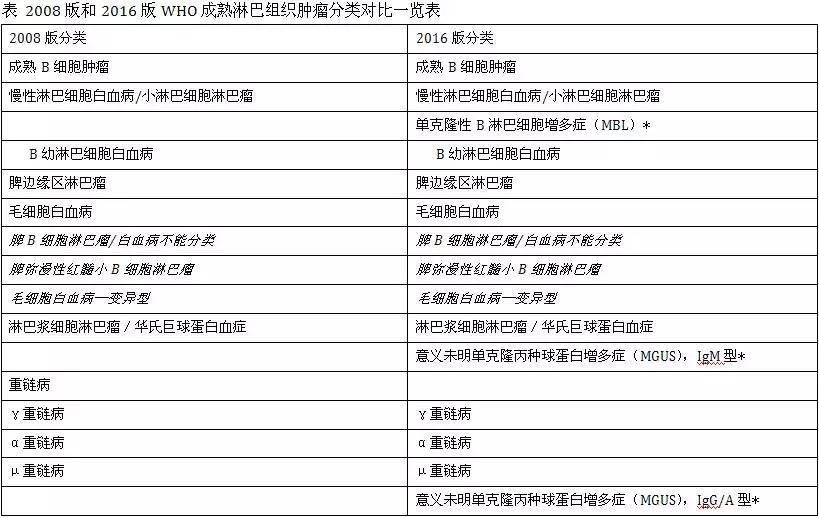
2016版WHO淋巴肿瘤分类(以下简称“2016版”)即将发布,前不久Swerdlow SH等人在《血液》(Blood)杂志在线发表了新分类的修订说明。在此基础上,我们查找了大量相关文献,通过对比2008版对2016版的主要更新进行了如下解读。更为详细的解读将于近期刊登于《中华血液学杂志》。
成熟B细胞肿瘤
慢性淋巴细胞白血病/小细胞淋巴瘤(CLL/SLL)
2008版CLL诊断标准要求外周血B淋巴细胞计数≥5×109/L;在B淋巴细胞<5×109/L时,如存在CLL细胞骨髓浸润所致的血细胞减少,也可诊断CLL。2016版则认为,“如果没有髓外病变,在淋巴细胞<5×109/L时即使存在血细胞减少或疾病相关症状也不诊断CLL”。
单克隆性B淋巴细胞增多症(MBL)
2008版诊断MBL要求外周血B淋巴细胞<5×109/L。2016版对此诊断标准不变,但强调区分低计数型MBL和高计数型MBL,如果外周血克隆性B淋巴细胞<0.5×109/L,则定义为低计数型MBL,此类患者很少进展,一般不需常规随访;如果克隆性B淋巴细胞≥0.5×109/L则为高计数型MBL,这部分患者应该每年常规随访一次。
2016版提出“组织型MBL”的概念,如果SLL/CLL侵犯淋巴结但没有发现“增殖中心”,且CT扫描淋巴结直径<1.5 cm,此时诊断为“组织型MBL”,而不诊断为SLL/CLL。
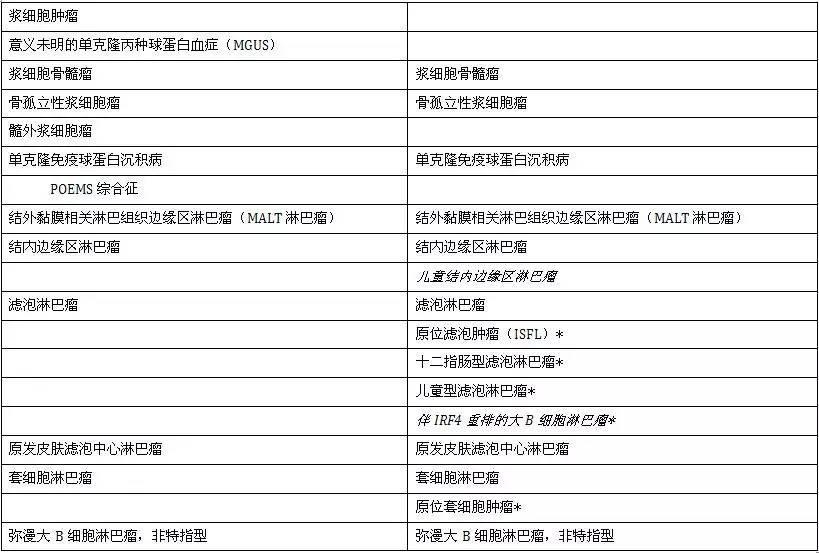
滤泡淋巴瘤(FL)、原位滤泡肿瘤(ISFN)、儿童型滤泡淋巴瘤和其他相关淋巴瘤
2016版在原FL基础上提出2个特殊亚类以及2个独立疾病分类。
1. 两个特殊亚类
原位滤泡肿瘤:ISFN即之前所谓“原位滤泡淋巴瘤”,改为ISFN是为强调其极少发展为真正的FL。组织学上需要与FL部分侵犯淋巴结相鉴别。
十二指肠型FL:指局限于十二指肠黏膜或黏膜下层的低级别FL,不同于其他肠道FL,部分十二指肠FL可自愈,绝大多数不需要治疗。
2. 两个独立分类
儿童型FL:“儿童FL”在2008版中作为FL的暂定亚类存在,缺乏BCL2重排和细胞增殖指数高是其与典型FL鉴别的主要指标。儿童FL也可见于成人,两组病程和预后无差别,均预后良好,故2016版分类统称为“儿童型FL”。但儿童型FL需要与FL-3级鉴别,特别是在成人病例中。
伴IRF4异常的大B细胞淋巴瘤:也是一种好发于儿童和年轻成人的淋巴瘤,在2016版中作为暂定亚类呈现。常常发生于韦氏环和(或)宫颈淋巴结,一般为早期病变。细胞强表达IRF4/MUM1,常同时表达BCL6及伴高增殖指数。BCL2和CD10表达于半数患者,少部分表达CD5。细胞起源上常为生发中心型。大部分病例有IGH/IRF4重排,有时同时有BCL6重排,但缺乏BCL2重排。有些病例没有IRF4重排,但IRF4/MUM1强表达也归入此类。这类淋巴瘤较儿童型FL侵袭性强,但对治疗反应良好。在年长患者中,应注意和CD10﹣/MUM1﹢的FL鉴别,后者常预后不良。
套细胞淋巴瘤(MCL)、白血病型非淋巴结性MCL和原位套细胞肿瘤(ISMCN)
2016版分类中强调将MCL分为两型:经典型MCL和白血病型非淋巴结性MCL(即所谓惰性MCL)。经典型MCL的IGHV基因未突变或少部分突变,同时表达SOX11,常侵犯淋巴结和其他结外组织,伴t(11;14)之外的继发遗传学异常。白血病型非淋巴结性MCL则常为IGHV突变型,不表达SOX11,常侵犯外周血、骨髓和脾脏,临床过程多为惰性,继发遗传学异常较少,但如果出现TP53异常,可表现出非常侵袭的临床病程。
2016版分类中强调了CCND2易位(常与IGK/IGL易位)在cyclin D1/t(11;14)阴性MCL诊断中的作用,大约50%的cyclin D1/t(11;14)阴性MCL存在CCND2易位。
另外,2016分类将原来的“原位套细胞淋巴瘤”改称为“原位套细胞肿瘤”,强调其相对“良性”的疾病特征。ISMCN指Cyclin D1﹢细胞局限于滤泡套区内,并未达到MCL的诊断标准,需要与套区生长模式的“显著性”MCL鉴别,低增殖性的套区生长模式MCL也可表现相对惰性的病程。
毛细胞白血病(HCL)
2008版认为HCL无特征性遗传学异常,2016版分类认为BRAF V600E突变见于几乎所有HCL患者,而不见于变异性HCL和其他小B细胞淋巴肿瘤。少部分使用IGHV 4-34片段的HCL无次突变,但70%伴有MAP2K1突变,MAP2K1突变也见于变异型HCL。
淋巴浆细胞淋巴瘤/华氏巨球蛋白血症(LPL/WM)及其相关性疾病
2016版认为,MYD88 L265P突变在LPL/WM中发生率高达90%,但该突变并不是LPL/WM所特有,MYD88 L265P突变可见于少部分其他小B细胞淋巴瘤、部分IGM型MGU、30%的非生发中心型弥漫大B细胞淋巴瘤、一半以上的原发皮肤弥漫大B细胞淋巴瘤-腿型,以及多数免疫豁免部位DLBCL(睾丸和中枢)。因此,MYD88 L265P突变是LPL/WM诊断的重要参考指标,而非特异性指标。
因为多数IgM型MGUS伴有MYD88 L265P突变,而IgG/IgA型MGUS、浆细胞瘤不伴该突变,目前认为,IgM型MGUS生物学特性与LPL和其他B细胞淋巴瘤类似而不同于浆细胞瘤。因此,2016版分类将MGUS分为两型:IgM型和IgG/A型MGUS。
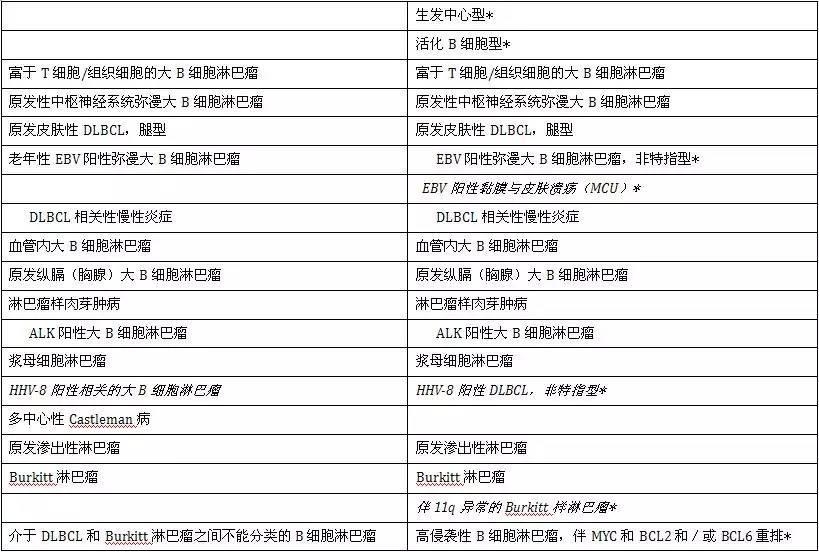
弥漫大B细胞淋巴瘤(DLBCL)
1. 强调细胞起源(COO)分类
2016版分类中要求对DLBCL进行细胞起源分类,即区分为生发中心来源(GCB)、活化B细胞来源(ABC)和少部分不能分类型(非GCB型),可应用基于CD10、BCL6、IRF4/MUM1的Hans法是进行COO分类。
2. 其他临床相关的重要表型、分子或细胞生物学特征
MYC重排见于5%~12%的DLBCL非特指型(NOS),常常与BCL2重排同时发生或少部分与BCL6易位同时发生,即所谓的“双次打击”或“三次打击”淋巴瘤,这部分患者在2016版分类中被作为一个独立的分类呈现,即伴MYC和BCL2和(或)BCL6重排的高侵袭性B细胞淋巴瘤(HGBL)。
MYC蛋白表达在DLBCL NOS中发生率更高,达30%~50%,其中20%~35%与BCL2共同表达。大部分MYC/BCL2蛋白表达的患者并不伴有MYC/BCL2染色体改变,因此被称之为“双表达淋巴瘤(DEL)”。其中MYC阳性的判读界值通常为40%,而BCL2阳性界值报道不一,推荐以>50%阳性细胞为BCL2阳性标准。DEL虽然被多数研究认为是预后差类型,但比HGBL预后要好。
因为抗CD30抗体的出现以及其良好的预期疗效,CD30可能成为DLBCL NOS的潜在治疗靶点,因此,推荐在DLBCL中检测CD30的表达。DLBCL患者的免疫组化检测至少要包括CD20、BCL2、MYC、CD10、BCL6、MUM1和CD30。
EBV﹢DLBCL和EBV﹢黏膜与皮肤溃疡(MCU)
2008版分类中将“老年性EBV﹢DLBCL”作为一个暂定亚类,指发生于年龄>50岁的非免疫缺陷患者,这部分患者预后较EBV阴性DLBCL差。但近年来认为EBV﹢DLBCL在年轻患者中发现的越来越多,其生物学行为与年龄>50岁患者无显著差别。因此,2016版分类则将明确其为一个疾病实体,并将“老年”改为“非特指(NOS)”,强调需要其他合并EBV感染的大B细胞淋巴瘤不归入此类,如淋巴瘤样肉芽肿。
另外,2016分类将EBV﹢黏膜与皮肤溃疡(MCU)从EBV﹢DLBCL中区分出来,作为一个新的暂定分类,因为MCU具有自愈潜能,对传统治疗反应良好。MCU可见于老年或医源性免疫缺陷患者。
Burkitt淋巴瘤(BL)和伴11q异常的Burkitt样淋巴瘤
BL中一个颇具争议的问题即是否存在MYC易位阴性的BL。有研究表明部分形态学类似BL、甚至表型和GEP也与BL类似的淋巴瘤缺乏MYC重排,但却有11q的异常(11q近端获得和端粒缺失)。与经典BL比较,这部分患者具有复杂核型,MYC表达低,表现出一定的形态学多形性,偶尔具有滤泡结构,常常呈结性表现。虽然报道例数有限,由于其临床过程类似于BL,2016分类将作为暂定的疾病整体命名为“伴11q异常的Burkitt样淋巴瘤”。
伴或不伴MYC和BCL2或BCL6重排的高侵袭性B细胞淋巴瘤(HGBL)
在2016版分类中,将所有伴MYC和BCL2和(或)BCL6重排的LBCL归入一个分类,命名为“伴MYC和BCL2和(或)BCL6重排的HGBL”,但需要除外FL和LBL,且形态学表现在诊断中应予以描述评论。此分类多数为2008年版分类中“介于DLBCL和BL之间的不能分类B细胞淋巴瘤”,即BCL-U。2016版中BCL-U不再作为一个暂定命名。那些没有MYC和BCL2和(或)BCL6重排,但形态学介于DLBCL和BL之间淋巴瘤被重新命名为HGBL NOS。
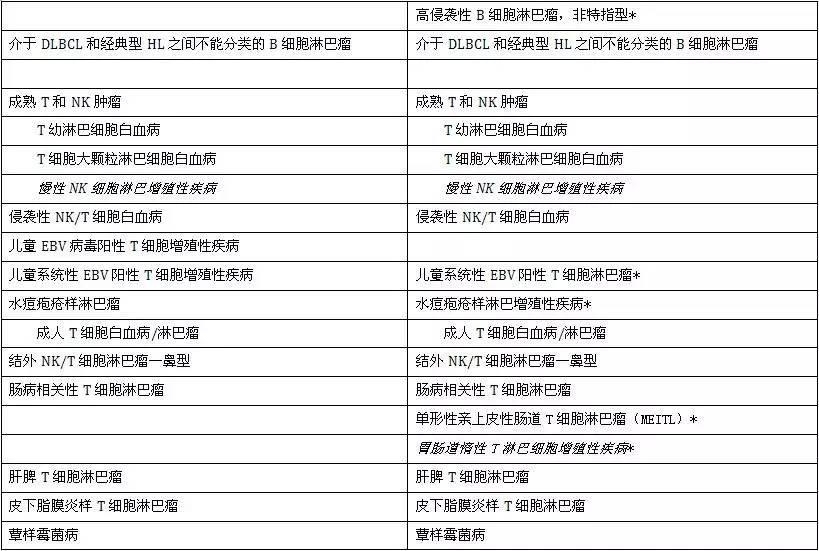
成熟T和NK细胞淋巴肿瘤
结性T细胞淋巴瘤
1. 外周T细胞淋巴瘤,非特指型(PTCL, NOS)、滤泡性T细胞淋巴瘤(FTCL)和伴TFH表型的结性外周T细胞淋巴瘤
原2008版的PTCL NOS中存在一类滤泡变异型,由于单一的形态学表现、相对特征的临床病理特征、细胞遗传学特征以及辅助性T细胞起源(TFH),在2016版中作为一个单独分类暂列,命名为滤泡性T细胞淋巴瘤(FTCL)。
但TFH免疫表型不是FTCL特有,血管免疫母细胞淋巴瘤(AITL)被认为起源于TFH细胞,20%~25%的PTCL,NOS的基因表达谱为TFH特征,部分原发皮肤CD4﹢小或中等大小T细胞淋巴瘤也具有TFH免疫表型特征。2016版分类中将2008版PTCL NOS中具有TFH特征的非FTCL患者另分类为“伴TFH表型的结性外周T细胞淋巴瘤”,作为暂定分类出现。
2. ALK阴性间变大细胞淋巴瘤(ALK-ALCL)和乳腺种植物相关ALCL
ALK-ALCL在2008版中作为暂定亚类存在,2016版分类将其更正为一个独立分类。乳房植入物相关性ALCL是2016版分类中新增的一个ALK阴性ALCL暂定分类,表现为乳房植入物周围渗出相关的纤维囊,淋巴瘤中位发生时间为盐或硅胶种植后10年左右。大多数情况下肿瘤细胞仅局限于肿胀的血清液体中,不侵犯纤维囊,此时一般推荐采取保守的治疗方式,去除填充物和囊。如果肿瘤细胞侵犯纤维囊,则可能出现淋巴结侵犯和系统性播散,可能需要化疗。
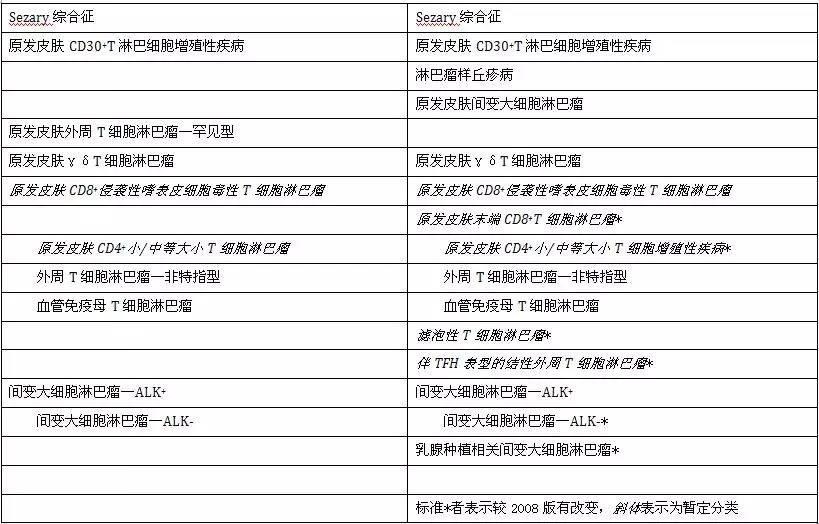
原发皮肤T细胞淋巴瘤
1. 淋巴瘤样丘疹病(LyP):强调临床鉴别
LyP是原发皮肤的CD30阳性淋巴增殖性疾病的一类,2016版在前版基础上中增加了D、E型以及伴6p25染色体重排的LyP。D型组织学上类似于原发皮肤的侵袭性嗜上皮性CD8﹢细胞毒性T细胞淋巴瘤,E型组织学上也类似于侵袭性淋巴瘤,但常可自愈。虽然伴6p25重排的LYP累及的基因位点也为DUSP22-IRF4,组织学与侵袭性的ALK﹣ALCL相似,但却并不发生播散性皮肤病变或皮肤外病变。因此,2016分类强调这三个LyP亚型的临床鉴别非常重要。
2. 原发皮肤末端CD8﹢T细胞淋巴瘤:避免过度治疗
是一个新的暂定分类,专指侵犯耳朵的结节性皮肤损害,组织学为高度侵袭性淋巴瘤表型,但临床表现为惰性,肿瘤细胞为D3﹢CD8﹢CD4-,不符合其他皮肤T细胞淋巴瘤的分类标准,应避免过度治疗。
3. 原发皮肤CD4+小/中等大小T细胞增殖性疾病:“降级”分类
该型在2008版中为暂定类型命名为“原发皮肤CD4﹢小或中等大小T细胞淋巴瘤”,最近认为这类淋巴瘤可能是皮肤对某些不明原因长期刺激的局部克隆性反应,尚不满足肿瘤的诊断标准,因此,在2016版分类中将其命名为原发皮肤CD4﹢小或中等大小T淋巴细胞增殖性疾病。
肠病相关性T细胞淋巴瘤(EATL)和胃肠道惰性T淋巴细胞增殖性疾病
2008版分类中EATL分为两型(Ⅰ和Ⅱ型),其中Ⅰ型细胞形态多样,局限于腹腔,主要见于欧洲北部人种,在2016版直接命名为EATL。2008版分类中Ⅱ型仅占10%~20%,在2016版分类中被暂定为“单形性嗜上皮性肠道T细胞淋巴瘤(MEITL)”,主要发生于腹腔外部位,细胞形态单一,多表达CD8、CD56和MAPK,亚洲人和西班牙人多见。
胃肠道惰性T淋巴细胞增殖性疾病:新的暂定分类,可累及单个或多个胃肠道部位,但呈惰性病程,注意与侵袭性T细胞淋巴瘤鉴别,无症状者可不特殊治疗。
儿童EBV病毒阳性T细胞增殖性疾病
2008版中“儿童系统性EBV阳性T细胞增殖性疾病”在2016版中更名为“儿童系统性EBV+T细胞淋巴瘤”,强调其临床的爆发性、侵袭性临床病程。
2008版中“水痘疱疮样淋巴瘤”在2016版分类中更名为“水痘疱疹样淋巴增殖性疾病”,强调其与慢性活化性EB病毒感染的关系,以及临床过程的多样性,该病即可表现为局限性惰性的皮肤病变,也可出现发热、肝脾淋巴结肿大,伴或不伴皮肤表现,出现系统性症状时常为侵袭性病程。


















共0条评论