1、概述
嫌色细胞胞癌(chromophobe renal cell carcinoma,ChRCC)作为肾细胞癌的一个独立亚型,于1985年首次被报道,是仅次于透明细胞肾细胞癌和乳头状肾细胞癌的第三常见类型,占所有肾细胞癌的5%左右。经典ChRCC由较大而浅染的植物样细胞和较小的嗜酸细胞呈实性巢状排列分布,被纤细血管分隔,肿瘤细胞具有特征性的葡萄干样皱缩的胞核以及核周空晕。ChRCC目前分为经典型和嗜酸细胞亚型还有混合型等,少见组织学类型包括小管状、微囊状、梁状及神经内分泌样和乳头状等结构。色素性微囊性ChRCC在1998年由Michal等人首次报道,当时描述了5例肿瘤细胞排列呈微囊样,肿瘤细胞胞质嗜酸性,伴有色素性钙化及细胞外脂褐素等特征性的ChRCC;2005年该研究小组详细研究了20例色素性微囊性ChRCC的免疫表型和分子遗传学及临床预后特征,荧光原位杂交(FISH)检测结果发现其具有典型的ChRCC遗传分子学特征,进一步证实其为ChRCC的组织学亚型,生物学行为更为惰性,没有远处转移和肉瘤样变。在2016年该究小组又报道10例组织学表现为多房囊性的ChRCC,认为是色素微囊性ChRCC同一谱系的肿瘤类型,从而更拓宽ChRCC的组织学谱系。
微囊性ChRCC的临床表现与普通型ChRCC相似,多为体检无意间发现,少数患者表现为腰痛、肉眼血尿或腹部肿块等三联征,发病年龄为32-83岁,平均年龄为60岁,男性略多见。影像学检查常表现为单侧肾肿块。目前为止国内外文献中仅有不足50例的报道,而国内有3篇文献报道。
2 、病理学特征
大体肿瘤多为单发,界限清楚,但多无完整包膜。切面灰黄灰褐色,常见出血和大小不等的囊腔,多无坏死及中央瘢痕。组织学类似于经典型ChRCC,但结构上以微囊状和管囊状为主,部分区域呈腺瘤样排列,腺腔被覆低柱状排列且核朝向基底部的肿瘤细胞,腔面形成刷状缘。囊肿或小管被覆以嗜酸性瘤细胞为主,少数可见较大植物样细胞,但两种细胞均表现皱缩而不规则的核膜、双核形成,核周空晕等典型ChRCC胞核特征表现。部分微囊腔内可见类似于甲状腺滤泡的胶样物质,其是否为肿瘤细胞分泌所致,目前研究仍不甚清楚。乳头状结构罕见,此外多数色素性微囊性ChRCC可见局灶典型ChRCC的组织学特征,少数肿瘤可完全为多房囊性管囊状结构,但囊肿被覆肿瘤细胞具有典型病理形态学特征。
此外色素性微囊性ChRCC均可见色素沉积,色素可出现在细胞内和细胞外,细胞内色素颗粒类似于肾上腺皮质中常见的脂褐素沉积,而细胞外色素主要出现在微囊性囊肿内,主要为含铁血黄素成片沉积常形成色素池样结构,色素具有神经黑素样特征,研究认为是含铁血黄素混合物,特殊染色Masson-Fontana染色、Ziehl-Neelsen染色和普鲁士蓝染色均显示局灶阳性,其形成可能与包裹神经黑色素和脂褐素的溶酶体异常沉积有关。据文献研究发现钙化、色素沉积及微囊形成可能与肿瘤微环境内的出血所致的退行性变有关。肿瘤间质稀少,可见营养不良性钙化和沙砾体,周围常见坏死和玻璃样变性。特征性的色素沉着及微钙化目前仅见于色素性微囊性ChRCC,故病理医师诊断时应引起注意。综上所述广泛的取材并仔细寻找典型ChRCC的组织学和细胞特点是准确诊断关键,此外免疫组化染色和分子遗传学检测可进一步辅助诊断和鉴别诊断。
免疫组化染色,与普通型ChRCC具有相似的免疫表型特征,肿瘤细胞表达PAX8、CK7、EMA、parvalbumin、抗线粒体抗原和E-cadherin等,文献报道显示在ChRCC中CDl17的特异性为95%,其在色素性微囊性ChRCC中多为局灶阳性,其分布无组织结构特异性,阳性染色多定位于胞膜,部分胞胞膜及胞质均着色;肿瘤细胞不表达Vimentin、CD10、AMACR、TFE3、Melan A、CA9、S-100、Syn等标记物;S-100和HMB45阴性,说明肿瘤组织中的色素不是由黑色素细胞产生;胶样铁特殊染色可为蓝色,超微结构和分子遗传学均显示与典型ChRCC相似,进一步证实其为独特的ChRCC组织学亚型。电镜观察瘤细胞内可见多量大囊泡和丰富的线粒体及深染而致密的色素颗粒,无黑色素小体或神经内分泌颗粒,囊泡直径150-300nm,类似于肾皮质集合管的B型闰细胞。分子遗传学检测存在1,2,6,10,13、17和21号单体染色体缺失。
由于ChRCC 常见胞核形不规则和退行性变的核浓染,因此ISUP/WHO和Fuhrman分级系统并不适用于ChRCC,无法对其临床预后进行区分,新近提出的Paner分级系统根据单位面积内肿瘤的核质比例、是否存在核多形性以及核间变将其分为3级,与患者的临床分期和预后存在明显的相关性。1级:无核拥挤和间变;2级:地图状的核拥挤(低倍镜下存在地图状高核浆比,高倍镜下可见核接触)和存在核多形性(核大小差异3倍以上,可见明显的核染色质不规则);3级:存在胞核间变性(多叶核及瘤巨细胞)或肉瘤样转化。而ChRCC常见的退行性变的核浓染不包括在该分级系统之内。
3 、鉴别诊断
色素性微囊性ChRCC作为特殊形态类型ChRCC,十分罕见,因其组织形态学特殊,且有色素沉着,在临床常被误诊为其他类型肾癌或转移性肿瘤。
(1)管囊状嗜酸细胞腺瘤:在大体、组织形态学及免疫表型特点可类似于色素性微囊性ChRCC,两者均可见出血性囊腔、嗜酸性肿瘤细胞、假乳头状结构、间质钙化、肿瘤细胞表达CD117而不表达Vimentin等。鉴别诊断要点为:管囊状嗜酸细胞腺瘤瘤体中央可有放射状瘢痕,肿瘤细胞常呈实性巢状或腺泡状排列,微囊结构中为红细胞,瘤细胞呈圆形或多角形,胞质内有较多的嗜酸性颗粒,细胞核圆形规则,染色质均匀分布,核仁位于中央,核膜无皱缩,无核周空晕,肿瘤间质细胞少且常伴玻璃样变性。嗜酸细胞腺瘤和ChRCC均被认为来源于集合管的闰细胞,在免疫表型上有一定的相似性,CDl17均可阳性,但嗜酸细胞腺瘤常CK7阴性或弱表达,而ChRCC为CK7强阳性。
(2)管囊状肾细胞癌:罕见,明显好发于男性(男女比为7∶1),大体上囊壁更加菲薄,镜下囊肿被覆肿瘤细胞呈鞋钉样排列,偶尔可见乳头状结构,肿瘤细胞核级别高,核仁显著,囊肿间为纤维性间质,免疫组化染色表达Vimentin、CD10、AMACR和高分子CK等,而较少表达CK7。
(3)XP11.2易位/TFE3基因融合性肾细胞癌:组织形态学较为复杂多样,透明细胞和嗜酸性瘤细胞呈乳头状排列,偶尔可表现为明显的管囊状结构,常见色素沉积和沙砾体钙化,可与色素性微囊性ChRCC相混淆。前者色素为颗粒较为粗大黑色素,免疫组化染色特征性核表达TFE3,FISH检测TFE3易位。
(4)获得性囊性肾病相关性肾细胞癌(ACD-RCC):组织形态学结构多样,肿瘤组织内可见不规则筛孔及乳头状结构,因而可与色素性微囊性ChRCC混淆。ACD-RCC与终末期肾病相关,可伴有长期透析病史,肿瘤细胞内可见特征性有折光性的草酸钙结晶沉积,免疫组化染色常弥漫表达AMACR等。
(5)以小管状结构生长为主的乳头状RCC:肿瘤细胞弥漫表达CK7且间质内常见含铁血黄素沉积和沙砾体形成,因此可与具有乳头状结构的色素性微囊性ChRCC混淆。前者乳头为可见纤维血管轴心的真性乳头,常见泡沫细胞聚集,免疫组化染色弥漫表达AMACR、Vimentin和CD10等,而不表达CD117。
(6)透明细胞肾细胞癌:尤其是嗜酸性变亚型,该肿瘤肿瘤细胞常呈团巢状或腺泡状排列且扩张形成大小不一的囊腔,但腔内无色素细胞,常有坏死;肿瘤细胞胞质透明或呈嗜酸性细颗粒状,结构不规则,核仁明显,无核周空晕,包膜不厚,界限不如嫌色细胞癌清晰,核分裂象多见,也无明显葡萄干样核特征。免疫组化色素性微囊性ChRCC可有CD117等为阳性,胶体铁染色阳性。
(7)转移性恶性黑色素瘤:组织形态学多样,肿瘤细胞常单个或团巢状排列,无筛状或微囊状结构及罗马桥样排列,免疫组化S-100和HMB45阳性有助于二者的鉴别诊断。
4、 临床治疗及预后
ChRCC临床预后较好,生物学行为惰性,5年总体生存率78%-100%,约2%-8%的ChRCC可见肉瘤样转化,从而表现出侵袭性的临床进程。目前多项研究提出的与ChRCC疾病进展相关的临床病理变量包括:病理分期≥pT3期、镜下肿瘤大腺泡状结构、坏死及微血管浸润、Paner核分级≥2级、肉瘤样转化等。而核分裂象计数和瘤细胞构成的类型与肿瘤的预后无关。色素微囊性ChRCC大多数分期和分级较低,无肿瘤性坏死和血管浸润,缺乏明显的大腺泡状结构,目前报道较少,故尚未侵袭性生物学行为的文献报道,亦未见肉瘤样转化。
总之色素微囊性ChRCC是一种少见组织学亚型,组织学上存在异质性,包括微囊/管囊状、假乳头状、腺瘤样结构等,常见色素沉积和钙化,病理形态学和免疫表型特征与普通型ChRCC相似,生物学行为更加惰性,临床预后好。仔细寻找典型的ChRCC特点并辅以免疫组化染色助于该肿瘤诊断和鉴别诊断。
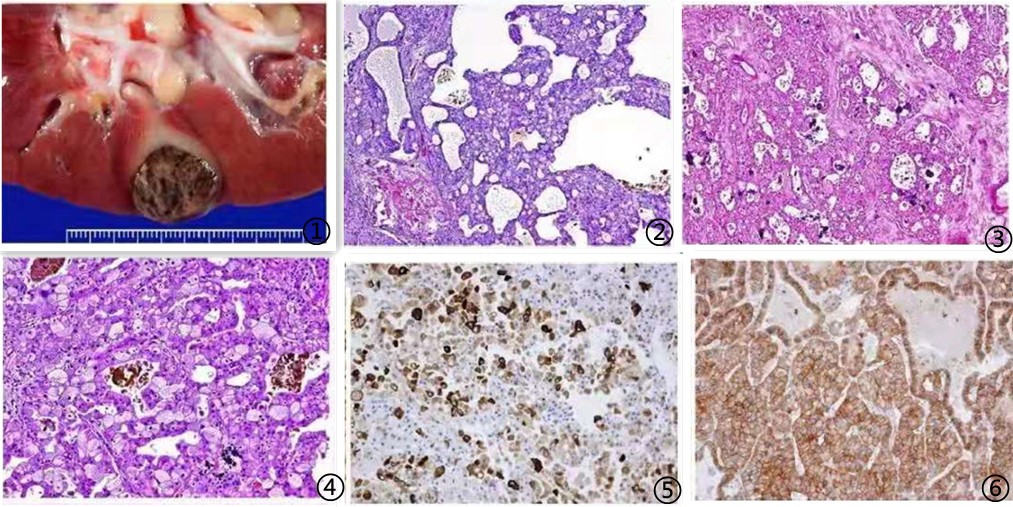
图1 大体肿瘤为单发,界限清楚,无完整包膜,切面见大小不等囊腔,无坏死及中央瘢痕;图2 低倍镜下肿瘤细胞呈微囊状和管囊状为主,局灶可见出血及色素沉着;图3肿瘤细胞间质见钙化及砂砾体;图4 矮柱状肿瘤细胞呈腺瘤样排列,嗜酸性胞质为主,胞核不规则,可见双核和核周空晕,间质内见钙化和细胞内外色素沉积;图5肿瘤细胞EMA呈局灶弱阳性;图6肿瘤细胞CD117弥漫强阳性。
参考文献略;图片来源于网络,如有侵权,联系删除。














共0条评论