[导读] 根据周小鸽老师讲课录音整理(录音整理:王会英)
作者:周小鸽(审阅:周小鸽老师、纪小龙老师)
来源:CPN新兵训练营
1、

1、很高兴在这里跟大家一起交流一下Castleman病,可能对大部分病理医师来说,Castleman病名字很熟悉,但真正遇到这种淋巴组织疾病的机会还是比较少。说到Castleman病,大家就会想到“棒棒糖”、“同心圆”样的滤泡,但实际上Castleman病是一个比较复杂的疾病,我把我们科十几年来遇到的Castleman病病例总结了一下,结合看到的一些文献,跟大家一起分享我对Castleman病的理解和认识。
2、

2、文献和书中对Castleman病的定义不完全一样,有各种各样的说法,看完我们的这些病例,我对Castleman病的理解是这样的:Castleman病(CD)是一组性质未定的淋巴/浆细胞和间质细胞增殖性异源性疾病。这是我对它的理解。为什么把它们弄到一起?因为,虽然在临床上表现各异,但是在病理学上它们比较相似。从疾病性质上看,有的呈良性、交界性、有的与肿瘤关系密切。有文献报道,CD中的淋巴细胞没有克隆性,但是通过雄性激素受体多态性检测间质细胞却有克隆性,甚至有一部分间质细胞具有染色体的核型异常。尽管如此,现在国际上并没有把CD视为肿瘤,但是它有各种各样的临床表现,有一部分CD特别像淋巴瘤,甚至治疗上也按照淋巴瘤进行治疗,如多中心CD;还有一部分单纯切除就可以了,按良性病变对待。所以说CD这个病很复杂,实际上不是一种疾病,而是一组疾病。现在比较公认的说法是三种疾病。
回顾历史,它的名称也是各种各样的,最早叫做巨大淋巴结病,淋巴结可以长的很大;观察形态又发现有些病例血管比较多、有些滤泡比较多,所以又叫做血管滤泡淋巴结增生这么一个良性增生性疾病;还有一些病例形态很像错构瘤,正常淋巴结结构中血管多了、滤泡多了,叫做血管淋巴错构瘤。后来名字叫的越来越多,最后大家认为还是叫做Castleman病最能代表它原始的状态。迄今为止绝大多数Castleman病的病因不太清楚,有些认为与免疫异常有关系、或与感染有关系,现在发现有些Castleman病与HHV8感染有关。如果一定要把这一组疾病进行分类,大概可以分为两个大类(主要看分布):一类是局限性/单中心CD(透明血管型-HV、浆细胞型-PC、混合型);另一类是多中心性(浆细胞型)。随着深入研究,又发现多中心性Castleman病有多种不同的情况,因此又分为了HHV8+ Castleman病,这个常常与HIV感染有关系,有些病例还同时有EB病毒的感染。这类Castleman病在病因学上相对比较清楚;另外还有一些HHV8- Castleman病,病因学尚不清楚的多中心Castleman病称为特发性多中心Castleman病(特发性-iMCD)。
3、

3、临床上,CD分为单中心和单中心CD,二者的临床表现可以差别很大,但在形态学上比较相似,要么透明血管型,要么浆细胞型,或二者皆有的混合型。
单中心CD大多数Castleman病为单中心性,单中心的意思就是指病变发生在一个淋巴结区域(可以是一个淋巴结,也可以是一组淋巴结),但不是多个淋巴结区域。单中心Castleman病从形态学上可以分为三种类型:透明血管型、浆细胞型、混合型(24%)。
(1)透明血管型(CD-HV)占了单中心大多数(67%),其形态学上有很多特征,有些是主要特征、有些是次要特征,如果把次要特征当做主要特征进行诊断,可能就跑偏或者过度诊断或者是漏诊断了。透明血管型CD,首位的主要特征为淋巴结的滤泡增多,绝大多数Castleman病都是这样的,但是要注意的一点是滤泡的多少并不是绝对的,与病变在膈肌的上下有明显关系。在膈肌以上淋巴结内发生的Castleman病,它的滤泡是增多的,如果滤泡减少则很难诊断为Castleman病;在膈肌以下的滤泡比较少、间质增多为主。另外的主要特征是生发中心缩小、套区增宽、间区血管增多。除了主要特征,还有一些次要特征,包含了淋巴窦消失、血管长入/长出生发中心、套细胞呈同心圆、套内多生发中心、浆样树突细胞团(CD123有助于观察)、奇异间质细胞(注意与霍奇金淋巴瘤中大细胞的鉴别)。次要特征可以存在但不是必备的,它可以为诊断提供参考。(2)浆细胞型(CD-PC)相对较少,占9%,它的主要特征同透明血管型:滤泡多、生发中心缩小、套区宽,但滤泡间区浆细胞增多、血管减少。(3)混合型CD为前两者混合而成,同样具有滤泡多、生发中心缩小、套区宽,间区可以是以血管增多为主、或浆细胞增多为主或混合并存。
多中心浆细胞型CD是指在身体多个部位、多个淋巴结区域都有肿大淋巴结,就是我们常说的全身性疾病、系统性疾病,预后较差。它主要以浆细胞样形态表现出来,绝大多数镜下形态同反应性增生相似,只是间质内有大量浆细胞,也有少数病例具有透明血管型的滤泡形态特点。正是有这种滤泡演变,可以看到滤泡间区浆细胞从少到多、滤泡从小到大(甚至同反应性增生的滤泡大小),存在一种谱系的改变。多中心CD形态上没有太多独特的特征,跟免疫相关疾病所致的淋巴结肿大差别不大,所以说多中心CD很难做出一个明确的诊断,必须结合临床才能给出明确的诊断出来。
除此之外,我们还可以看到Castleman病还会伴有T淋巴母细胞增生,这种细胞不是肿瘤性的细胞,但是这种细胞增生成团或成小片,很容易让人当成淋巴母细胞淋巴瘤,从而误诊成恶性肿瘤。相当一部分病例中发现有这样一种现象,如果做TdT染色会发现这一部分细胞TdT+。另外Castleman病还会合并其他淋巴瘤或肿瘤,或者继发出现其他的肿瘤。
4、

4、为什么我在这里要把鉴别诊断拿出来,因为这些疾病(滤泡复旧、套区增生、血管免疫母细胞T细胞淋巴瘤、套细胞淋巴瘤、边缘带淋巴瘤、T淋巴母细胞淋巴瘤)不小心会被当做恶性肿瘤,或者有些恶性肿瘤被当做Castleman病来诊断,所以有很多疾病需要鉴别。
在临床表现和检验方面,单中心CD和多中心CD也是不同的,单中心CD比较简单,可能没有症状,少数一些病例可能有轻微贫血或者稍微有点乏力等轻微症状,只是某个部位、某个淋巴结肿大,但活检结果是个Castleman病。然而,多中心CD基本上都会有一些症状,特别是有B症状,去医院检查发现全身多处淋巴结肿大。检验指标也有很多异常的东西,这个后面有介绍。对于Castleman病治疗,单中心CD做局部切除就可以了,如果是一组淋巴结无法全部切除时再做个局部放疗就可以了。多中心CD就不一样了,因为无法切除干净,所以要进行系统性治疗,有时需要化疗,在NCCN针对淋巴瘤治疗的指南里面就有专门针对Castleman病的化疗方案指南,所以把Castleman病尤其是多中心CD当做淋巴瘤进行治疗。因此,病理医生也应该至少把单中心CD和多中心CD区分出来。多中心CD里面还有多种病因,也应该区分出来,这个后面会讲到。
5、

5、下面我们具体的一一进行详细的介绍。在我们的病例里面,单中心CD年龄跨度还是很大的,从4岁到72岁,平均年龄38岁,中位年龄39岁。透明血管型CD临床一般没有什么症状,偶有发热、乏力。但是浆细胞型CD不同,由于大量浆细胞存在,往往有一些副肿瘤症状,特别是皮肤的改变比较明显。就发病部位来讲,发生在结内的比较多见(占81%),发生在结外的较少(占19%),另外我们发现在结内的CD以膈肌为线,发生在隔上的占69%,发生在隔下的31%。现在CD病因尚不明确,但是治疗效果都很好。
6、

6、刚才我们说过了,关于单中心CD的几个类型,都有其主要特征和次要特征(见P3概述2)
7、

7、从我们的109例病例来看,CD-HV较好发于女性(男:女为1:1.73),发病年龄比单中心CD平均年龄偏低,大多数发生在结内(72%),按横隔来说,大多数发生在隔上(73%)。
8、
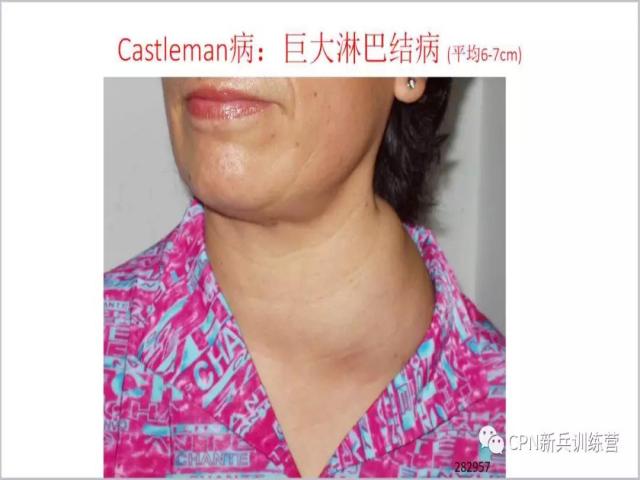
8、Castleman病以前叫做巨大淋巴结病,我们这里有个病例,病人来看病的时候就是这样(如图),脖子上巨大的淋巴结,大体上看就是一个Castleman病,活检证明这个病人是一个单中心的多个的淋巴结肿大。无论几十年前还是现在的文献报道,单中心CD的肿块大小平均为6-7cm,所以还是叫做巨大淋巴结病,虽然有时我们拿到的标本可能是较小的淋巴结,但是病变总体来说还是很大的,约6-7cm。
9、
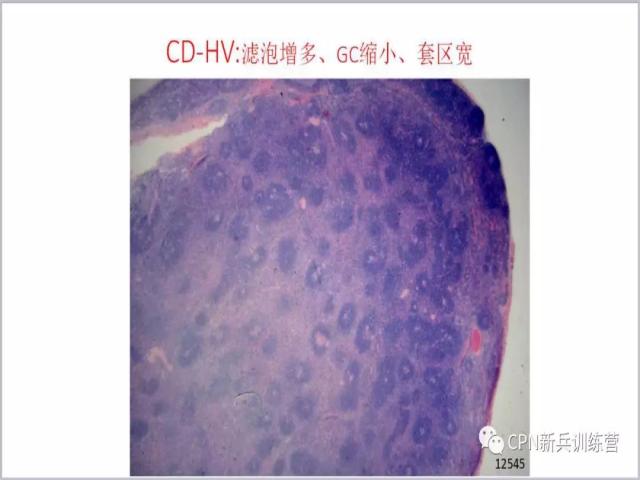
9、从组织学上来看,单中心透明血管型Castleman病最重要的就是滤泡增多,特别是膈肌以上的,如果低倍镜下看到滤泡稀疏,基本上不太考虑Castleman病。另外它的生发中心是缩小的,套区是增宽的,再就是要看滤泡间区,这个图低倍镜下看不太清楚。
10、

10、滤泡增多、生发中心缩小、套区增宽。
11、
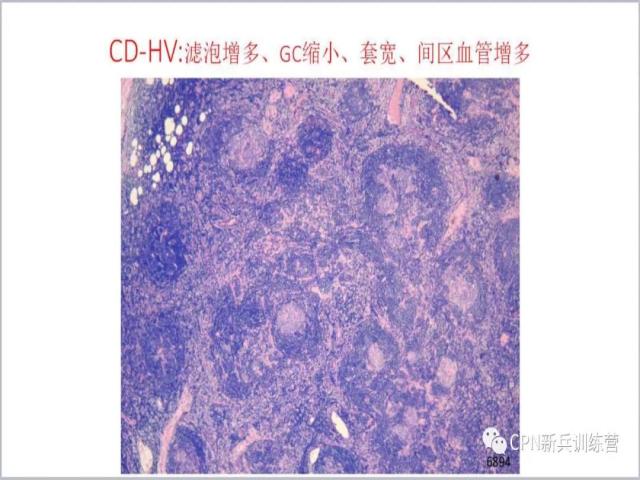
11、上图:滤泡增多、生发中心缩小、套区增宽,间区血管隐约可见。
12、
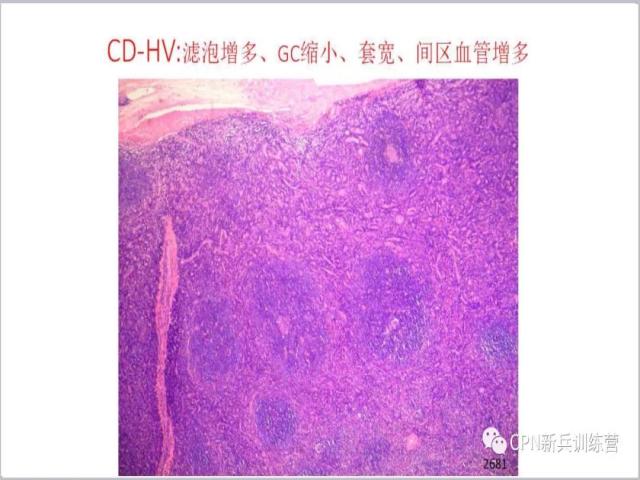
12、上图:滤泡很多,生发中心并不大,这是它的特点,低倍镜下就可以做出判断,间质里面血管明显增多了,甚至间区变宽。
13、
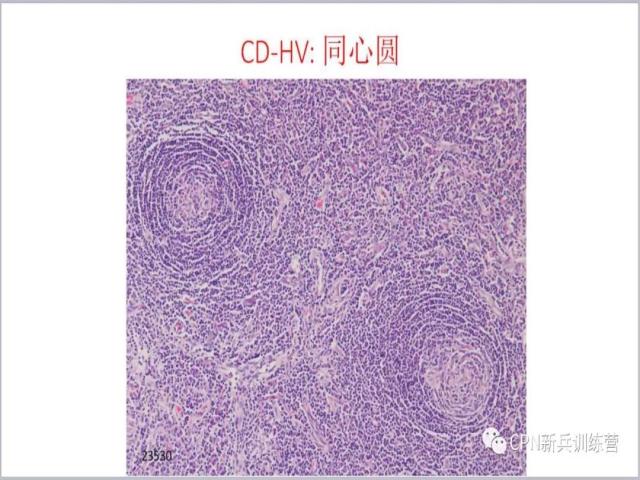
13、如果你在高倍镜下看它的排列,典型的病变可以看到上图这样同心圆样的排列。
14、
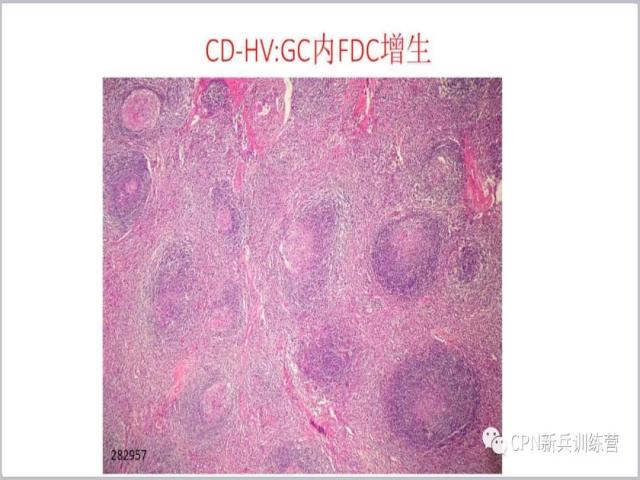
14、可以看到生发中心内的树突细胞的增生,正常淋巴结生发中心里面是大量的中心细胞、中心母细胞,但是现在中心细胞、中心母细胞减少了,生发中心缩小以后树突细胞增生。
15、
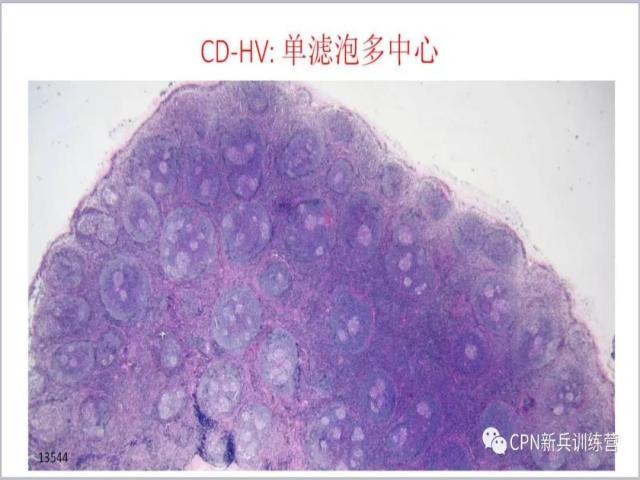
15、一个滤泡里可以看到多个生发中心,有些文献报道说只要一看到这个现象就诊断为Castleman病,但是我们有时在一个淋巴结里看到一个或者少数几个这样的滤泡,我们是没法诊断为Castleman病的,所以说这个现象不是绝对的特征,它可以作为一个次要的形态学标准,可以作为诊断的一个要点来考虑。
16、
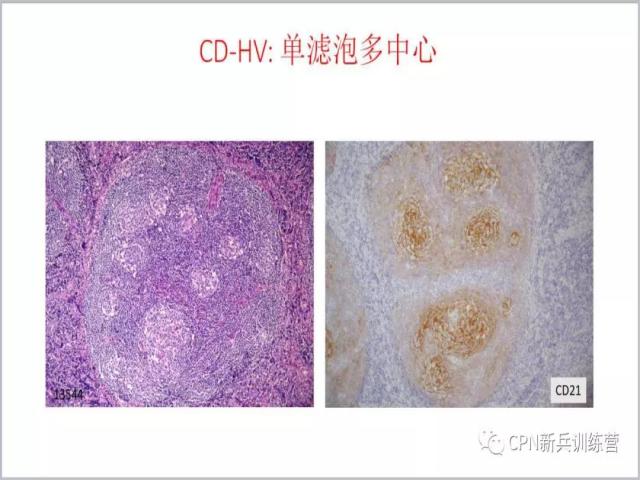
16、这是一个放大的图片,单个滤泡多个生发中心。
17、
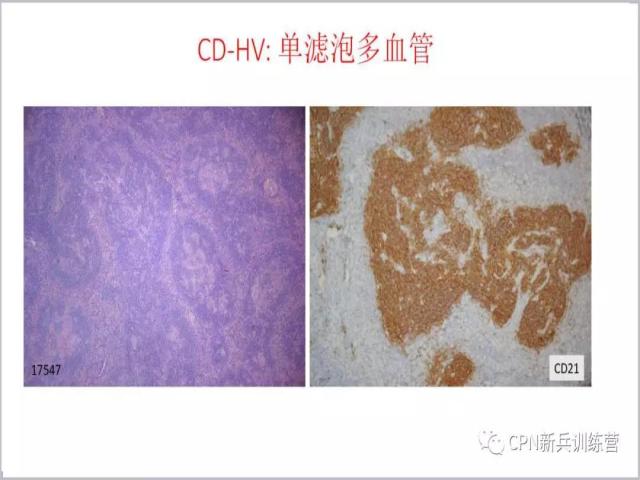
17、 除了间质里面血管增加,单个滤泡里面血管也有增加,CD21可以把FDC树突网勾勒出来,网里面的血管就反衬出来了,滤泡里面有很多血管长进去,这也是它的一个特点。这个可能跟血管免疫母细胞淋巴瘤T细胞淋巴瘤很类似,后面我们会讲怎么鉴别。
18、

18、再来看间质,血管增多是它最特征性的一个特点,这个图我们可以看到间质里面大量的血管增生,在病变的早期,血管是一种高内皮血管,随着时间的延长、病变变老,血管呈现一种谱系的变化,血管慢慢的变薄、变细,基底膜或者间质内出现了玻璃样变,呈现了透明血管型CD的特征。这个类型往往指的是间质内透明血管的改变。
19、
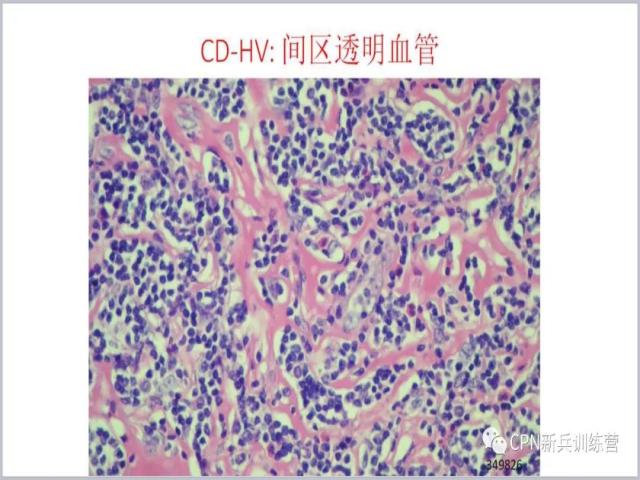
19、随着病变的发展,间质硬化。
20、

20、CD34标记可以看出,间质内血管增多,比反应性增生还要多。
21、

21、CD31标记显示间质内大量血管增生。
22、
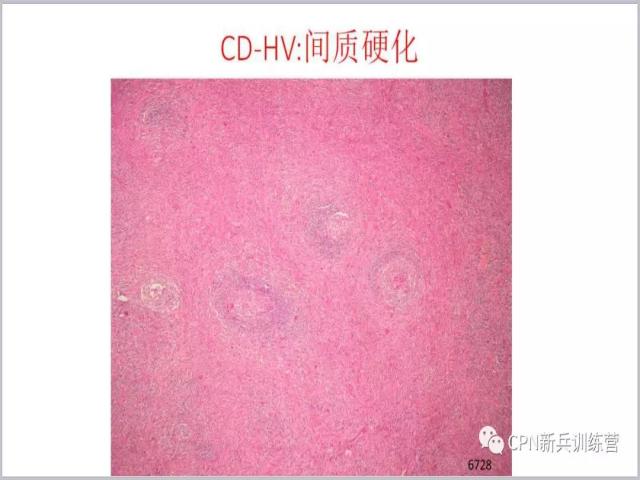
22、甚至有些间质出现了硬化,随着病变的推移,间质硬化会越来越重。
23、

23、还有一部分病例,滤泡并不增多,刚才我们提到,位于膈肌以下的这些淋巴结,并不是以滤泡增生为特征,有些是间质变宽、滤泡减少,有些极端的特殊病例,甚至可能在形态学上一个滤泡都看不到,用CD21染色可能只能看到少数FDC网的痕迹。所以说还有极少数CD完全以弥漫的形式、以间质为主的形式表现出来。在日常工作中,如果没有这样一种认识,可能想不到Castleman病,而是当成一种弥漫性的疾病看待,考虑其他的疾病去了。
24、
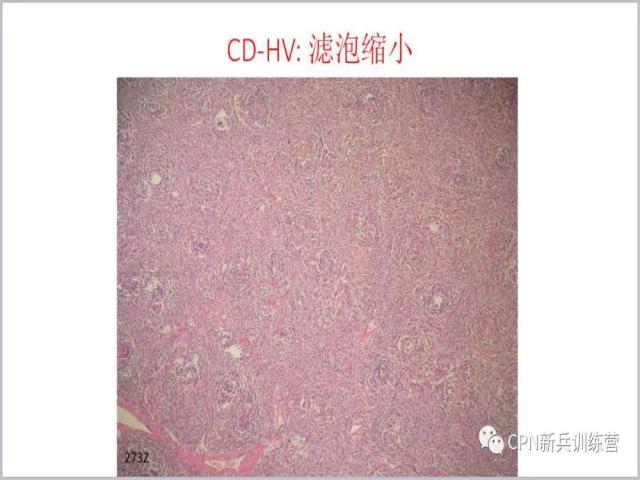
24、病变滤泡变得越来越小,甚至不明显了,跟典型的Castleman病无法联系到一起。
25、
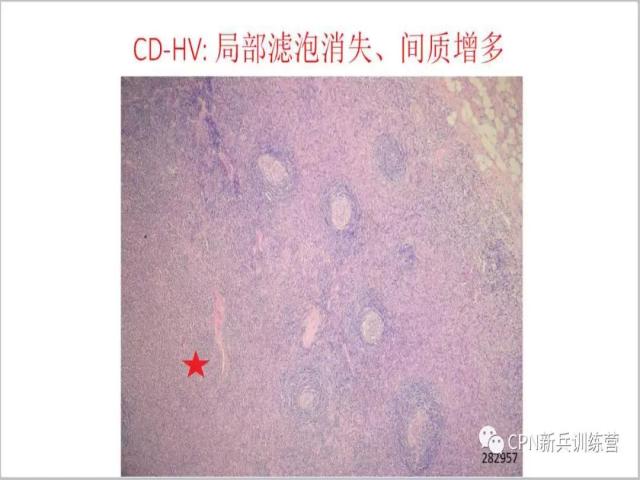
25、右侧部分滤泡还在,而左边这部分间质增多、滤泡消失或者说减少了,所以说病变是在不断的变化的。
26、
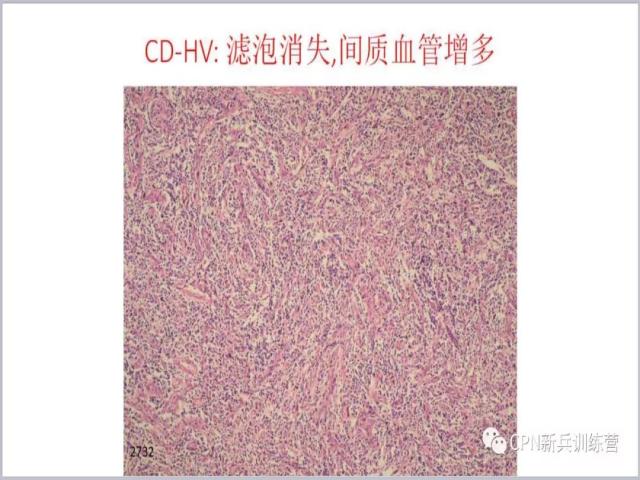
26、滤泡已经消失了,大量的血管间质的增生。
27、
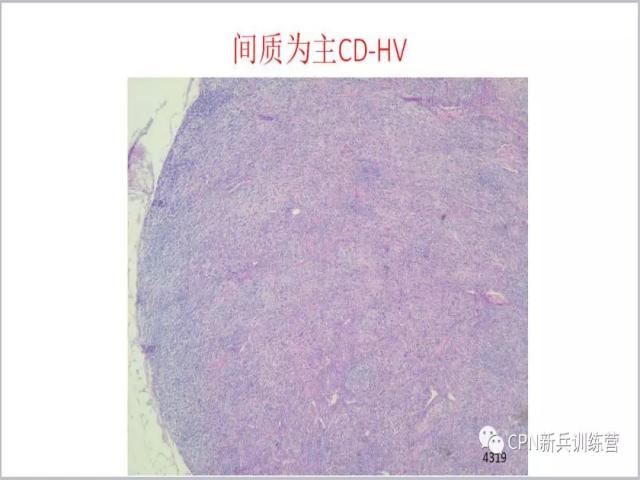
27、以间质为主的透明血管型CD,滤泡消失、看不到了,遇到这样的病例很容易被漏诊,或者误诊成了其他的疾病。因为一看到这个结构,可能往往会认为这个淋巴结结构是破坏掉的,可能是淋巴瘤。但是如果认真去看细胞,你看不到异型的细胞,找不到异型的淋巴细胞或者淋巴瘤其他的证据。
28、

28、左侧图可以看到弥漫性改变的形态学特征,CD21标记还可以看到一些痕迹留下来,有时候滤泡可能比这个还要少、还要小,就这个病例我们可以看到滤泡明显缩小,CD21标记呈现点状的痕迹,间质很多。
29、
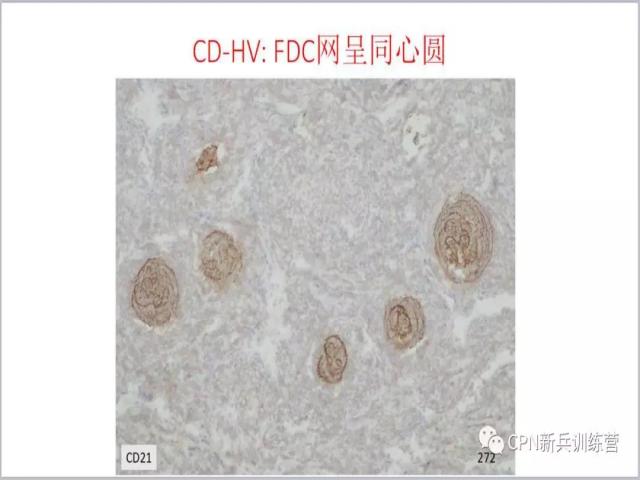
29、典型的同心圆样的FDC网。
30、
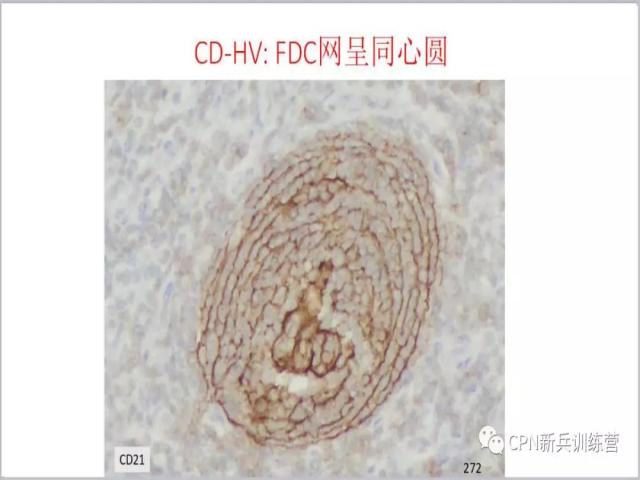
30、典型的同心圆样的FDC网。
31、

31、同心圆内血管长入。
32、
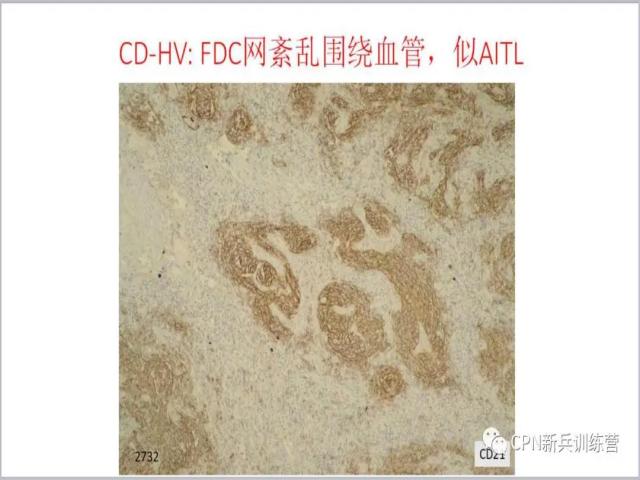
32、同心圆内血管长入很多,这种形态学很容易和血管免疫母细胞性T细胞淋巴瘤混淆。
33、
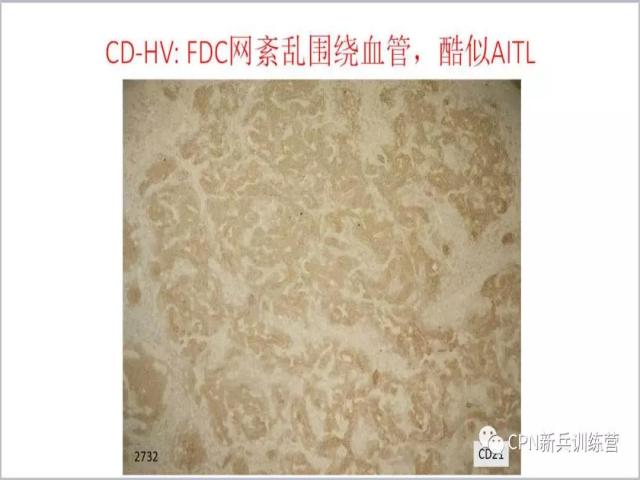
33、此例CD树突细胞大量增生,血管随着一起增生,FDC网不是那么完整的同心圆样,更像一个破碎的FDC网,很容易当作血管免疫母细胞性T细胞淋巴瘤。
34、
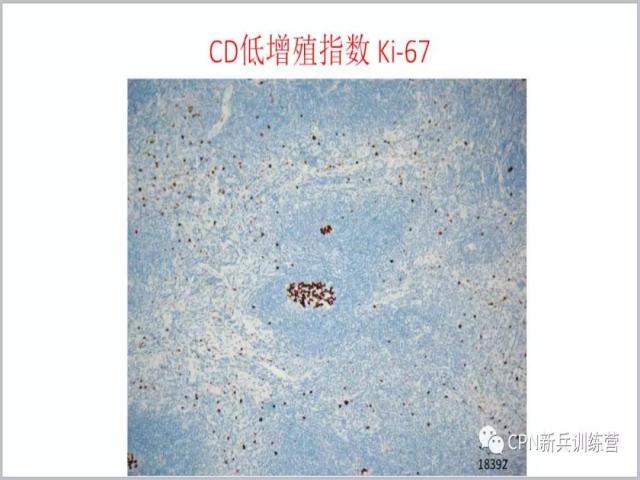
34、Castleman病还有一个特点:虽然滤泡很多(或者是一个弥漫性的病变),但Ki-67标记的核增殖指数不高,除了生发中心增殖指数相对稍高一些,其他区域Ki-67指数很低。反过来说,如果你发现这个病变Ki-67指数很高,或者局部Ki-67很高,就要提高警惕了,这个高的地方是不是有问题的地方。比如说T淋巴母细胞增生的时候,Ki-67增高可能是一个线索,帮助你发现有这部分细胞增生;或者其他一些肿瘤或淋巴瘤累及淋巴结出现了Ki-67的高表达,因此,Ki-67可以帮助我们印证是不是Castleman病。通常诊断Castleman病不需要做免疫组化,但在一些形态不是很明确的时候,最好还是做一些所谓“四项基本原则”(CD3、CD20、Ki-67、CD21)这一类的标记,可能会减少漏诊。
35、

35、这张图是T淋巴母细胞瘤累及到淋巴结吗?如果仔细观察你会发现,它并不是形成一种膨胀性的改变,从细胞走向看不像是主动向外扩张,反而是被挤压了。同时出现Ki-67指数很高且被挤压就很难理解了。这时做个LMO2,如果阳性,提示是T淋母,如果阴性,提示是增生;也可做TCR基因重排看是单克隆还是多克隆,如果多克隆提示增生,单克隆提示可能是T淋母累及淋巴结。
36、
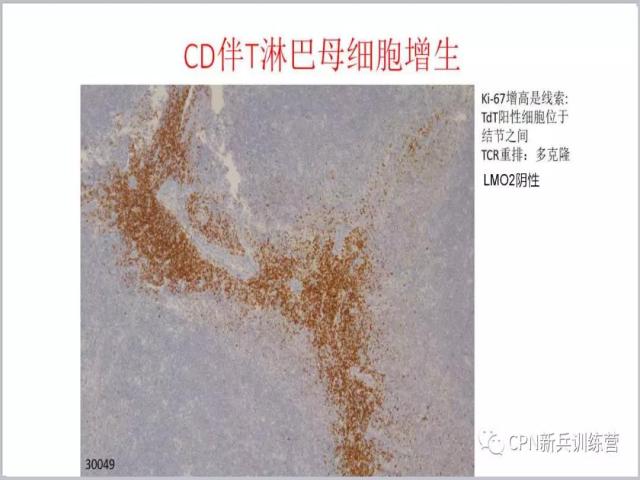
36、周围都是滤泡,T淋巴母细胞在滤泡之间生长,像是被挤压到中间来的。这个形态不像是长的很快的淋巴瘤的形态特征,很难解释它为淋巴瘤。如果看到这个形态特征,要去查一下胸腺有没有问题?看一看有没有克隆性?做一个LMO2看看有没有改变?这种病变在Castleman病人中并不是非常罕见的。
37、

37、下面我们介绍单中心Castleman病另一个亚型——浆细胞型CD,在我们的病例中纯粹的浆细胞型CD不多,只有14例,男性稍多,中位年龄49岁,平均年龄51岁,比透明血管型稍大。绝大多数发生在结内(93%),发生在隔下(57%)相对比隔上(43%)多。从形态特征来说,基本同透明血管型CD的形态特征,唯一不同的是在滤泡间区可见大量浆细胞,这些浆细胞可以是多克隆,也可以是单克隆的。
38、
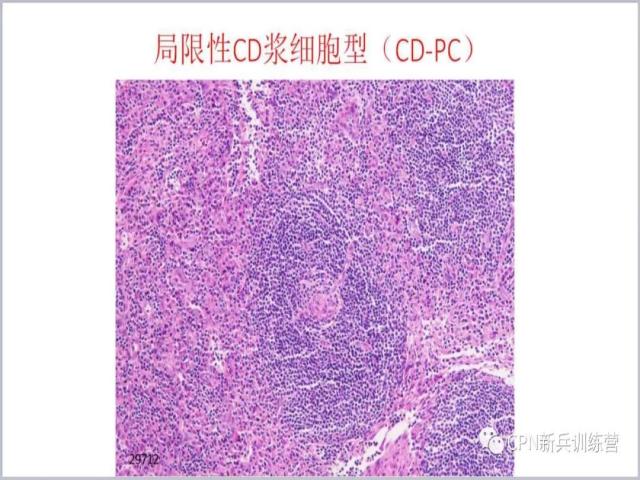
38、我们可以看到它的滤泡和透明血管型CD是一样的,生发中心小、套区宽、血管长入,但是同时可以看到在滤泡间不是大量血管增生,而是大量浆细胞。
39、
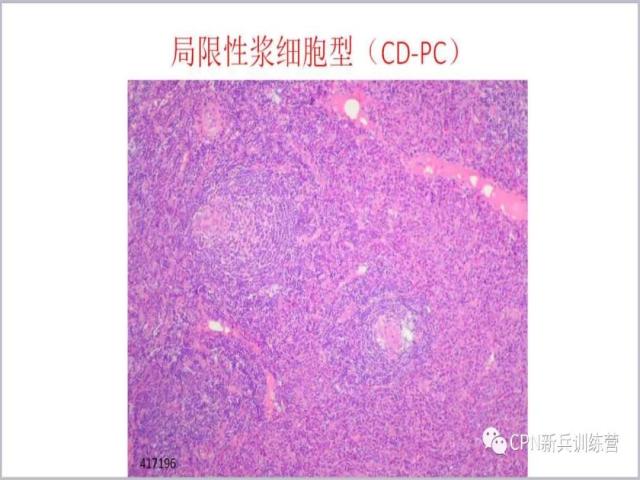
39、滤泡类似透明血管型CD的形态特征,但间区存在大量浆细胞。
40、
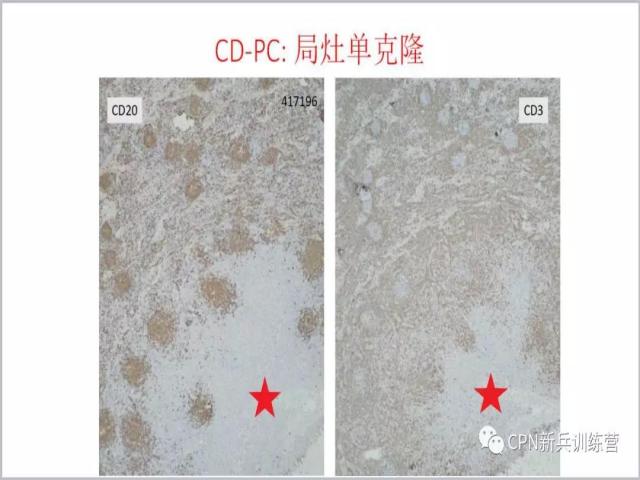
40、在此型Castleman病中有时我们可以看到单克隆的病变,如上图,从滤泡来看这是一个Castleman病,但是在局部我们看到滤泡相对减少。这个区域CD20是阴性的,CD3也是阴性的。这个区域到底是一个什么病变?
41、
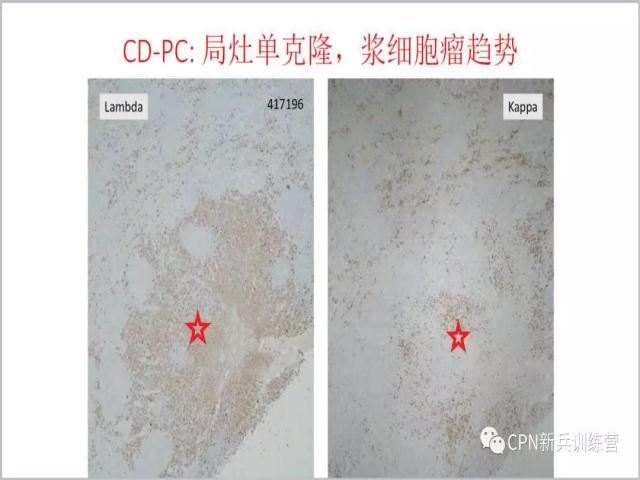
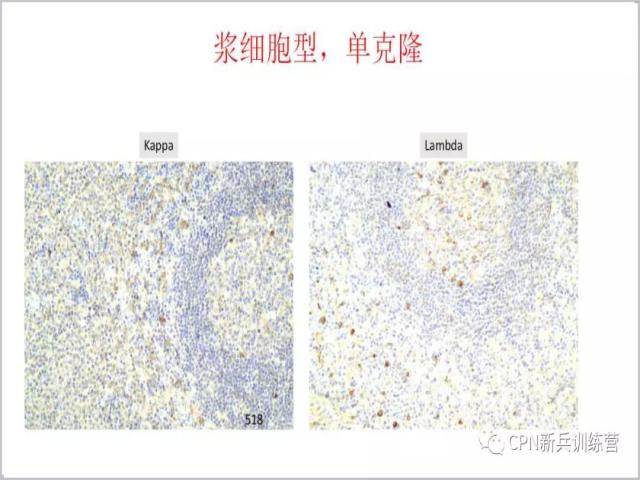
41、再进一步做一些标记,在CD20-、CD3-的区域Lambda+、Kappa少数+,结果是局部出现单克隆的浆细胞改变。这种情况也可以在滤泡之间出现。此例出现在局部,部分滤泡已经被破坏,如果不诊断局部浆细胞瘤的改变,至少也要考虑为具有浆细胞瘤的趋势。是报单克隆增生还是报浆细胞瘤,就是看滤泡的结构有没有被破坏,如果滤泡明显破坏、已形成肿块了,那么就报浆细胞瘤。报告单克隆浆细胞增生伴浆细胞瘤趋势还是浆细胞瘤?仁者见仁智者见智,报告浆细胞增生临床切除病灶就可以了,如果报告浆细胞瘤可能临床要进行下一步治疗(如局部放疗)。对于已经切除只有局部病灶的淋巴结,患者是否就能得到最大获益还未有考证。我的经验是报告“局灶单克隆增生伴浆细胞瘤形成趋势”就可以了,临床按照单中心CD病灶去除就可以了。
42、

42、第三种CD是混合型CD,混合型就是透明血管型和浆细胞型混合,男性稍多于女性,平均年龄45岁,正好介于透明血管型和浆细胞型之间的年龄段,结内较多(79%),横隔上稍多(58%)。形态学上具有透明血管型的滤泡特征,差别就是在间质内既有血管又有浆细胞混合构成,混合可以是均匀混合在一起,也可以是以透明血管为主或者浆细胞为主,但无论怎样在淋巴结内两种成分都可以看到。
43、

43、我们可以看到透明血管型滤泡特征,同时间质内可见透明血管和浆细胞混杂存在。
44、
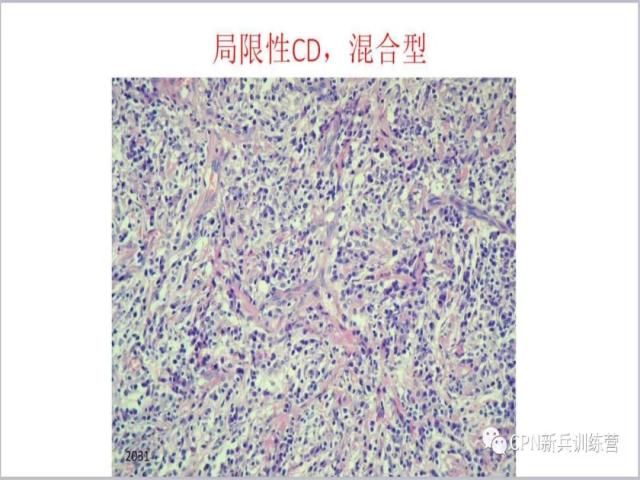
44、上图放大后我们可以看到透明血管很明显,我们首先会想到是不是透明血管型CD,但你仔细看仍可看到间质内有不少浆细胞散在混合在其中,所以这是一例混合型CD。
45、
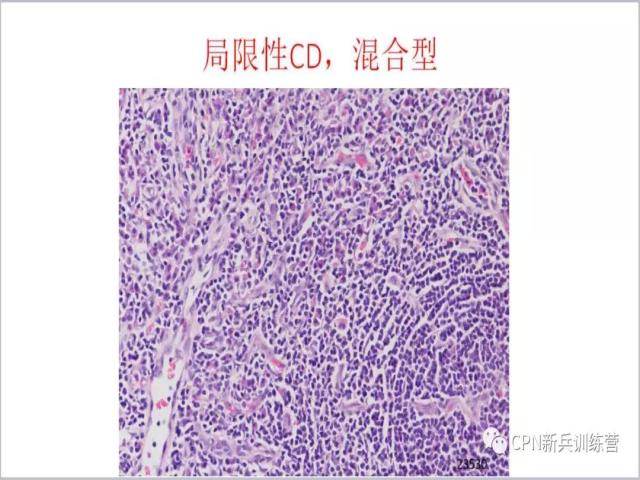
45、我们可以看到,右下角是一个滤泡,在其周边有很多散在的浆细胞,而在左边血管比较明显,也就是说既有血管的增生也有浆细胞的浸润,故此例也可以放到混合型CD。
46、
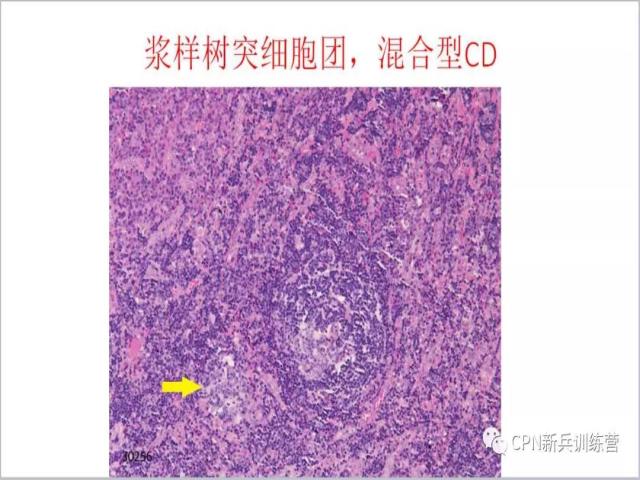
46、Castleman病除了以上三型,实际上还有一种形态特征,叫做浆样树突细胞团。在诊断Castleman病比较纠结的时候,可以仔细去找一下有没有这个特征,找到了是一个支持CD的诊断依据。上图箭头所指的地方,在蓝色背景下看到一巢淡染的细胞团,类似胰腺的胰岛的形态,可以是圆形、不规则或拉长,细胞比较单一,聚集成团。
47、
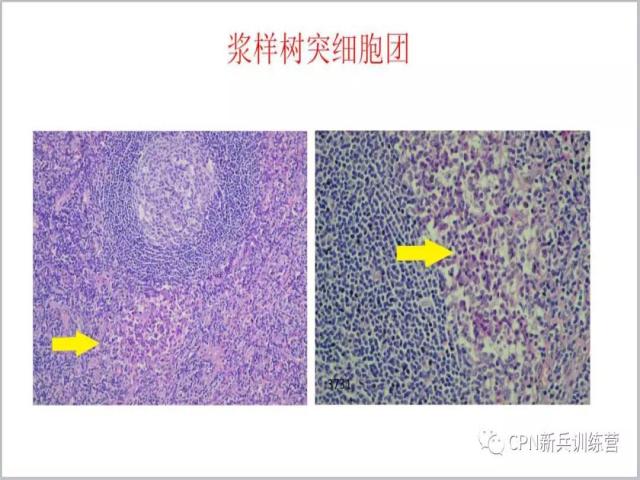
47、放大左图可以看到在滤泡下方有一团浆细胞样胞浆的细胞,就是浆样树突细胞。右图滤泡套区右侧拉长的细胞团也是浆样树突细胞。这类细胞团常常位于滤泡套区外紧邻套区,在我们统计的病例中透明血管型CD有一半可以找到这类细胞团,但在浆细胞型CD中几乎找不到,找到浆样树突细胞团对于诊断Castleman病以及分型有一定的提示作用。
48、
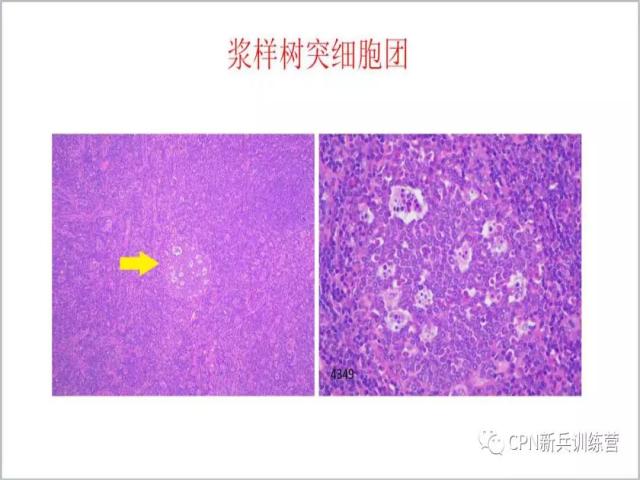
48、右图为左图放大后的图像。我们还可以在细胞团中看到一些凋亡的核碎,奇怪的现象是这一团细胞看上去很活跃,而Ki-67标记显示却只有20-30%这样一个很低的增殖指数。如果想进一步证实可以做CD123标记。
49、

49、另一个可以帮助我们诊断透明血管型CD的线索就是奇异细胞。间质中有的细胞胞体很大,甚至核仁很大,周围可见纤维化、硬化,淋巴细胞和浆细胞存在,似炎性背景。这些大细胞的存在容易被误诊为霍奇金淋巴瘤,但这些大细胞CD30-。其实它们是一些退变的细胞,因为Ki-67显示这类细胞没有增殖活性。
50、
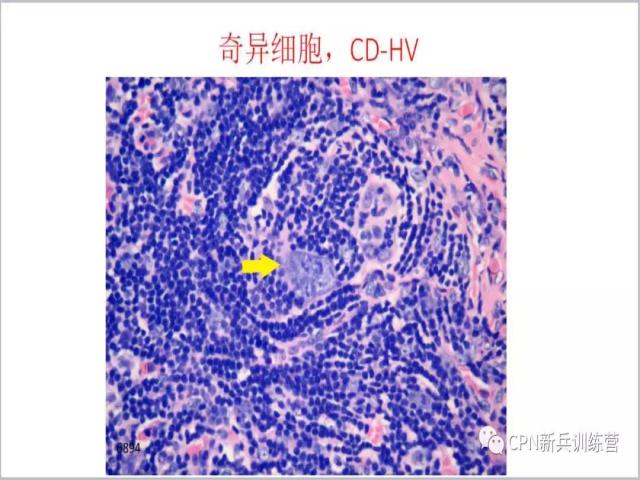
50、看中间的大细胞,可以作为我们诊断Castleman病的一个形态学线索。
51、
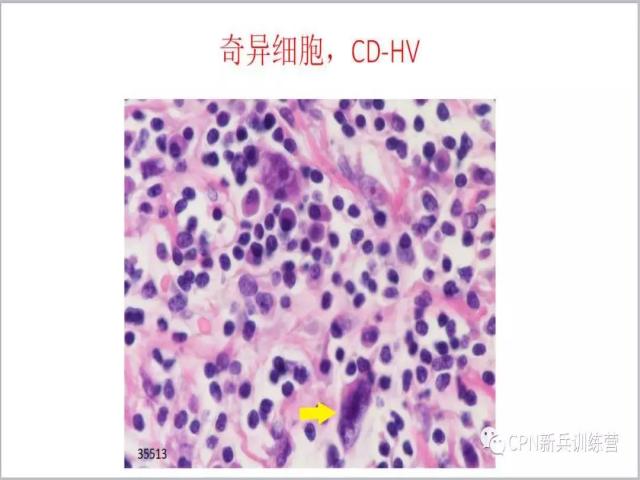
51、木乃伊样大细胞和霍奇金样大细胞。
52、
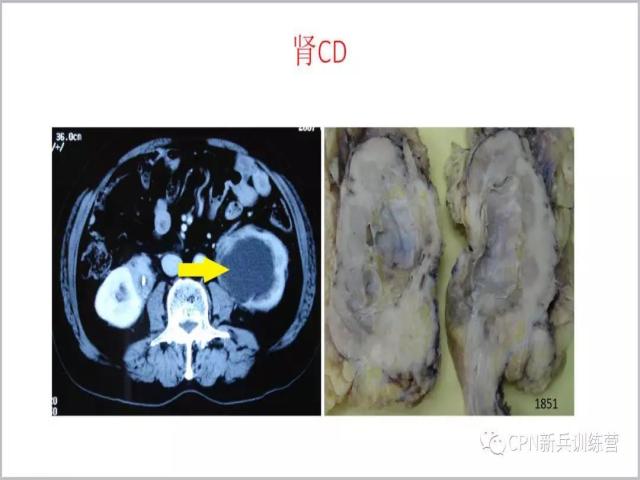
52、Castleman病大多数发生在结内,也有一些发生在结外,发生在结外的时候是一个诊断难点,文献报道,可以发现约1/3的病例发生在结外。这一例是发生在肾脏的Castleman病,这是影像学和大体形态。
53、
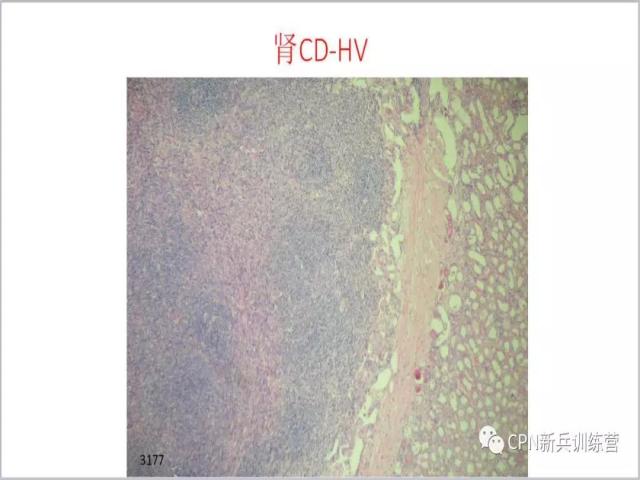
53、HE下我们可以看到,肾组织中可见大量的淋巴样细胞、淋巴滤泡,这些淋巴滤泡有些生发中心不明显,这种病变很容易和黏膜相关淋巴瘤混淆,在黏膜相关淋巴瘤中B细胞是成片分布,而Castleman病B细胞位于滤泡区域,滤泡间区还是T细胞,这是鉴别要点。
54、
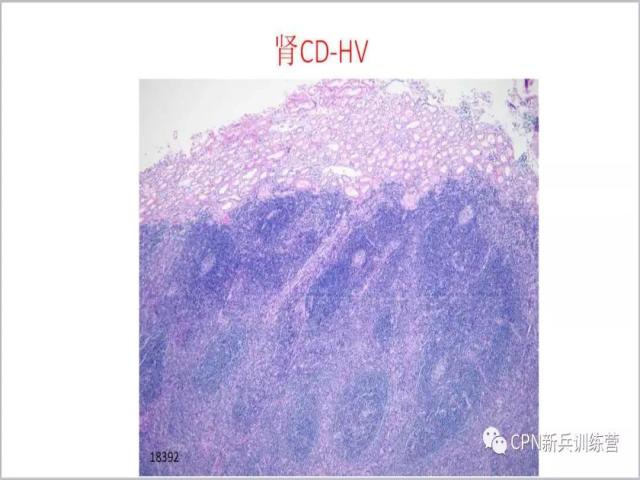
54、可见滤泡生发中心缩小、滤泡间区可以是血管增多也可以是浆细胞改变。
55、
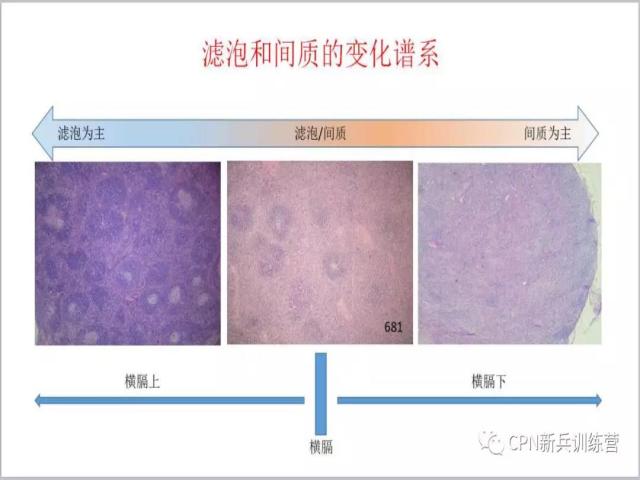
55、我们把前面讲的Castleman病进行归类小结一下,实际上Castleman病包括了滤泡改变、间区间质改变,滤泡和间质的关系我们可以用上图来代替,图示可以看到一个变化的谱系,谱系的一端为位于横隔上的以滤泡增生为主,另一端位于横隔下以间质弥漫增生为主,位于中间的既有滤泡的增生,也有间质的增生。结合临床取材部位(膈肌以上还是膈肌一下)和HE形态学特征对于诊断Castleman病有很大帮助。
56、
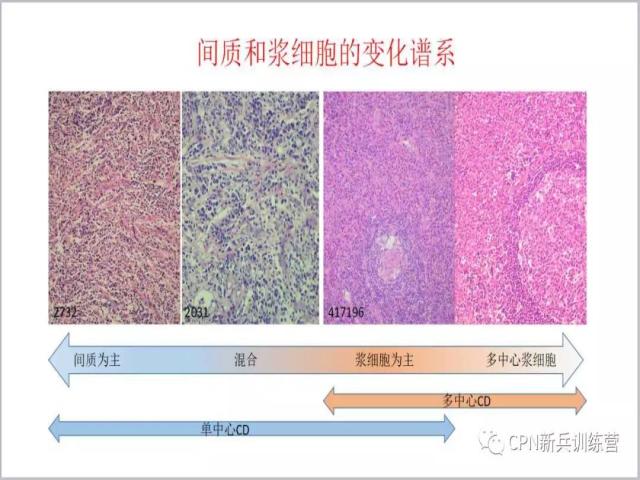
56、我们再看一下间质的改变,也是存在着一个谱系的变化,左边一端为单中心透明血管型Castleman病,向右另一端为浆细胞型Castleman病甚至是多中心Castleman病。多中心Castleman病病变除了间质浆细胞增生变化,滤泡也不同于单中心CD,生发中心缩小不明显甚至不缩小,类似反应性生发中心,此时诊断Castleman病是非常困难的,很容易被误诊为反应性增生的疾病或者自身免疫性疾病等可以引起生发中心增生的疾病。
57、

57、下面我们介绍多中心Castleman病,它的治疗与单中心Castleman病不同。现在国际上把多中心Castleman病分为两个完全不同的疾病,一种是HHV+的Castleman病,一种是HHV8-的Castleman病(也叫特发性-iMCD)。
多中心Castleman病的特点是:多中心(多个部位的),滤泡(呈反应性增生的滤泡、少数可以有透明血管型样的滤泡),间区(浆细胞增多,甚至达到皮质、被膜下窦),不同于典型的单中心Castleman病(其被膜下窦几乎消失)。多中心Castleman病被膜下窦比较明显,不管怎样这些形态学特征都不是特异性的,如果要诊断多中心Castleman病必须结合临床和检验。由于临床病史和检验结果提供的不完善,导致多中心Castleman病的病理诊断率偏低,多年来我们也只是诊断了4例多中心Castleman病,而西方国家的Castleman病大多数为多中心Castleman病。
58、
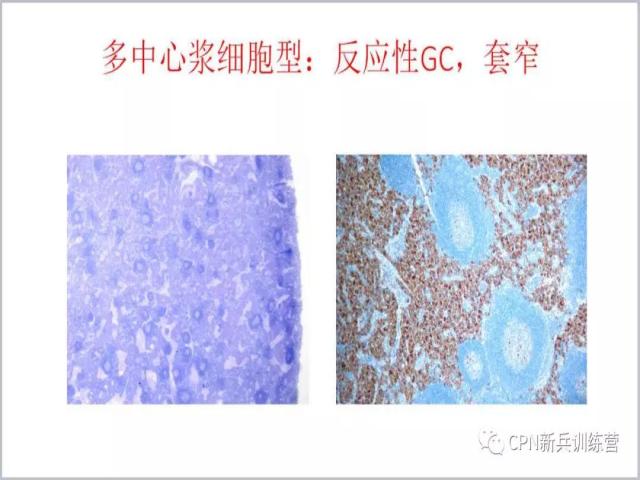
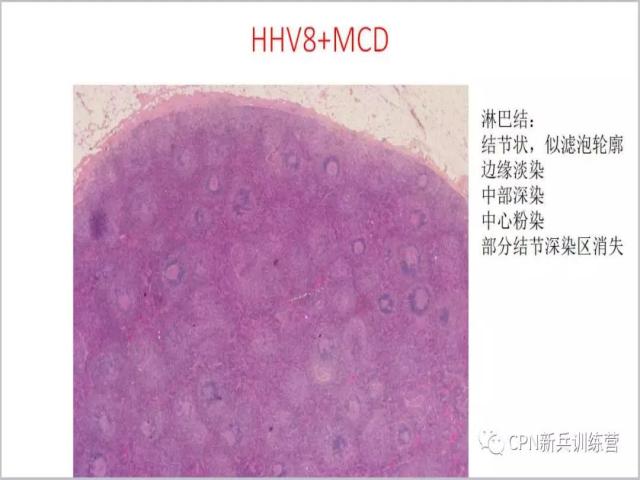
58、多中心Castleman病形态学特征:反应性生发中心,套区较单中心Castleman病窄。
59、
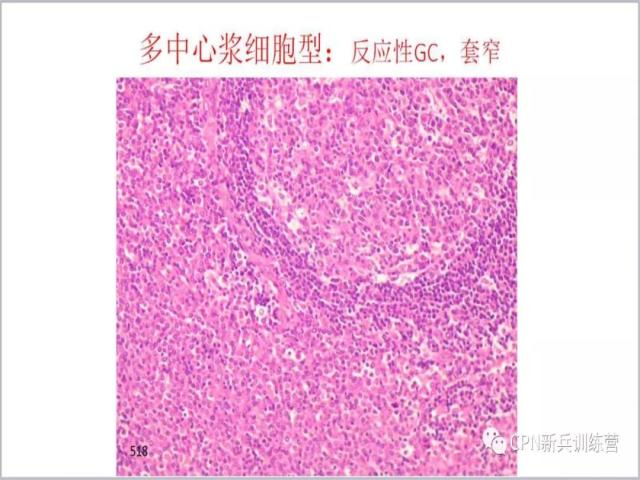
59、反应性生发中心,套区较单中心Castleman病窄。
60、
61、
62、
63、

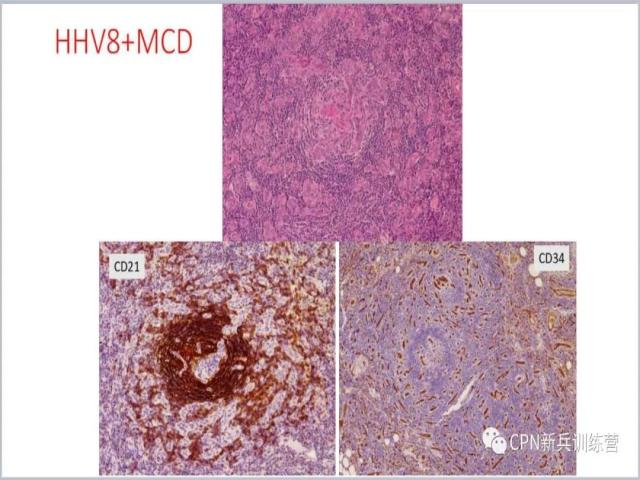
63、如果要诊断多中心Castleman病,首先要做HHV8染色,HHV8阳性的细胞往往是这些大一点的像活化的淋巴母细胞样的细胞,如右图所示阳性的细胞位于套区,而间区、滤泡生发中心偶见。
64、
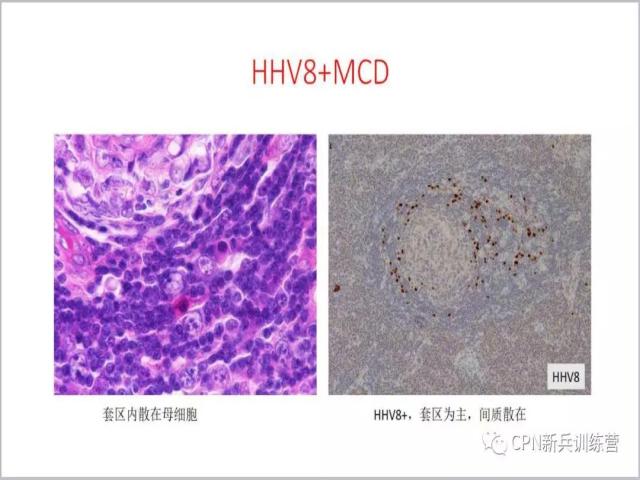
64、随着病变的增多,在套区HHV8阳性细胞也会增多,看到这个现象可以诊断HHV8阳性的Castleman病。
65、

65、为什么要进行HHV8染色进行分类?主要是它们的预后不同。除了HHV8+的MCD外还有一种HHV8-的MCD,我们称之为特发性多中心Castleman病(iMCD),2017年Blood发表了一个国际共识,对HHV8-iMCD诊断提出了一个标准。
66、

66、共识中有两条主要标准:形态学特征(滤泡特征+间区大量浆细胞)和多中心淋巴结肿大(这是个临床特征)。次要标准有11条(见上图),至少要具备2条且2条中必须有一条是检验的指标,也就是说次要标准里2条都是检验指标或者1条检验指标加1条临床指征。具备了2条主要标准+2条次要标准(2+2)就可以诊断多中心Castleman病了。
67、

67、临床皮肤改变可见紫红色樱桃状血管。
68、
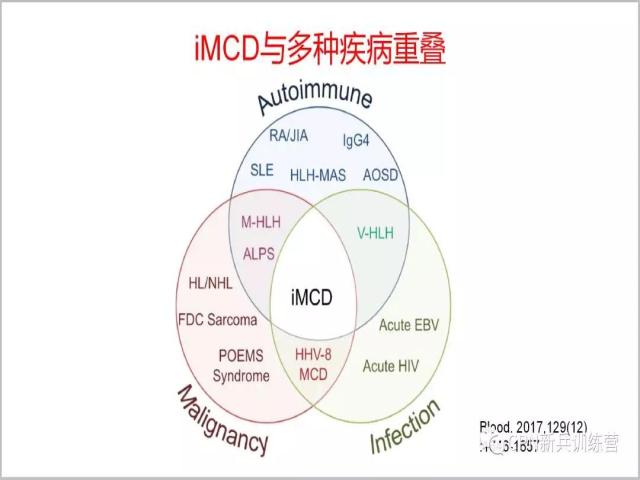
68、多中心Castleman病涉及面比较多,除了以上说的2+2条标准以外,还要除外一些与之相关、相类似改变的其他疾病,主要为自身免疫性疾病(关节炎、IgG4相关疾病、系统性红斑狼疮等)、肿瘤(霍奇金、FDC肿瘤、POFMS综合症)、感染(EB病毒、HIV相关),才可以诊断多中心Castleman病。
69、
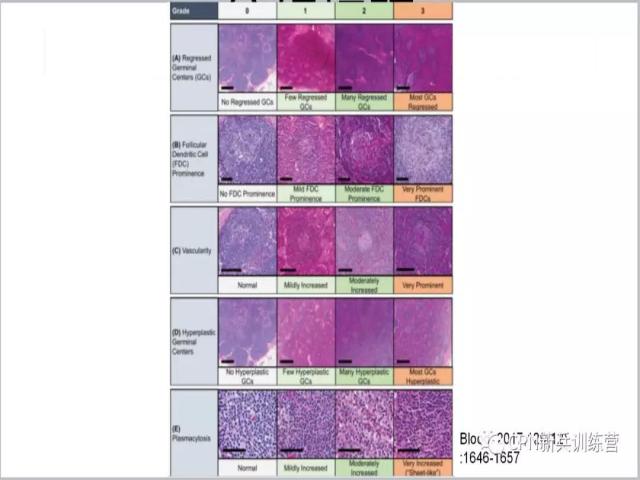
69、这篇文章说Castleman病很多都是有谱系的,上图从上到下依次为滤泡、FDC增生、血管、生发中心、浆细胞等从少/小到多/大的改变,显示不同谱系的细胞在Castleman病中的不同改变,所以我们认为Castleman病不是一种疾病,可能是多种疾病混合在一起的一组疾病。
70、
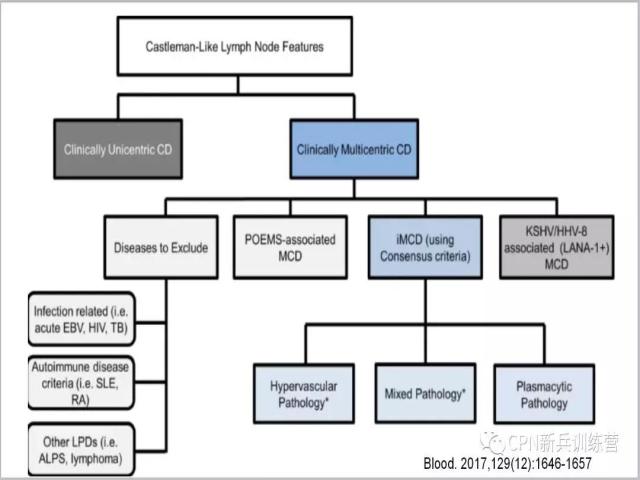
70、在病理学上遇到了Castleman病怎么诊断?如果我们看到了具有Castleman病特征的形态学改变,首先我们要确定这是一个单中心的还是多中心的(问病史),如果是单中心的基本上就是我们讲过的那三种亚型;如果是多中心的要先除外其他的疾病(包括感染性疾病、自身免疫性疾病、肿瘤性疾病等),再做HHV8进行分类。
71、

71、上图清晰显示了Castleman病形态特征改变的谱系。
72、

72、Castleman病诊断四步骤。
73、

73、Castleman病可以合并或继发多种肿瘤,所以说Castleman病可以是良性?交界性、肿瘤性?其实它的性质并不是特别确定的。
74、
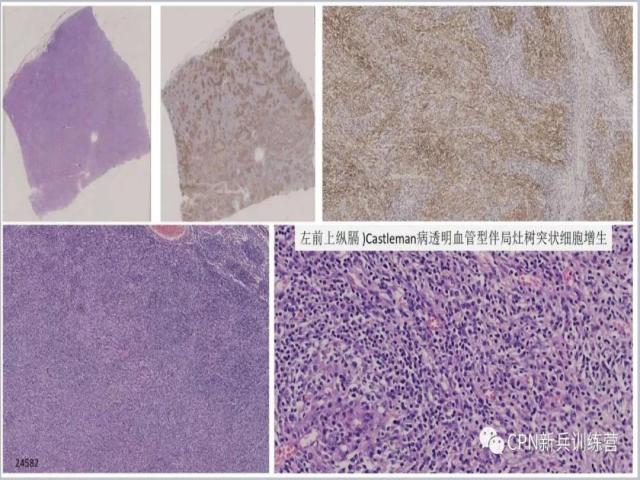
74、这个病例,开始发病时,具有Castleman病的病变特征同时伴有FDC网弥漫增生,随着病变发展,FDC网已经跑出了滤泡的范围,形成了弥漫或局部弥漫的区域,再进一步发展可能就会发生FDC的肿瘤。
75、
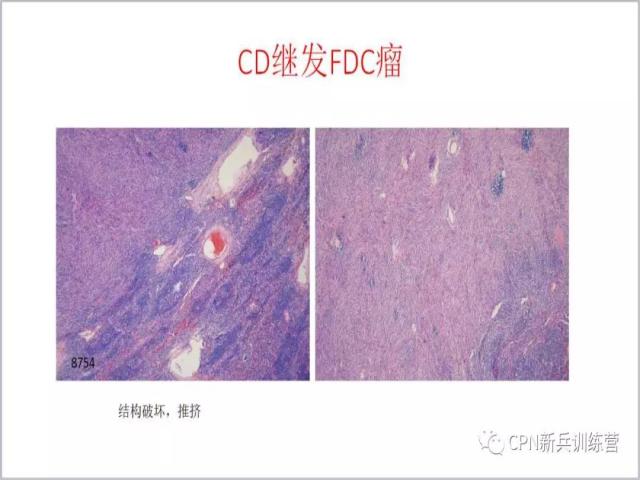
75、这个病例,右下还具有Castleman病特征,中间形成了推挤性的肿块,里面都是一些FDC细胞,原有结构破坏,已经继发成为FDC肿瘤。
76、

76、CD35、CXCL-13标记证实这些都是FDC细胞。
77、
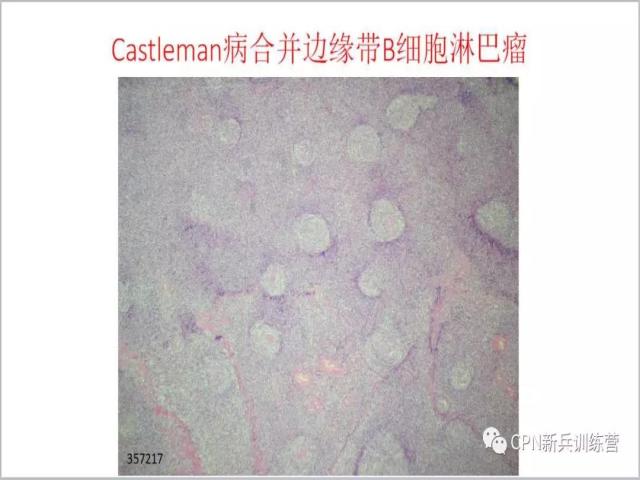
77、另外Castleman病也可以合并边缘带B细胞淋巴瘤,从滤泡特征来看还是Castleman病的滤泡,但是滤泡间区已经不是透明血管型了。
78、
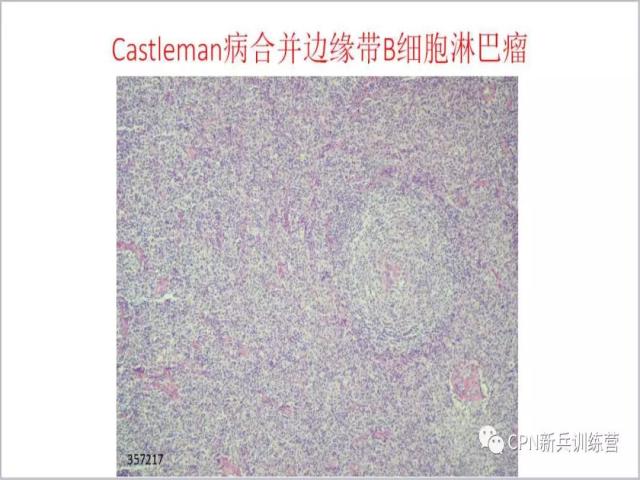
78、放大看。
79、

79、CD20弥漫阳性,表明在局部出现边缘带B细胞淋巴瘤,在另外的区域还是Castleman病形态特征。
80、
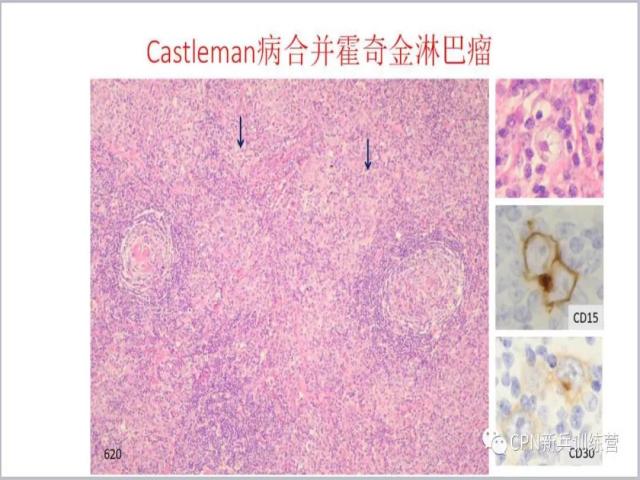
80、Castleman病还可以合并霍奇金淋巴瘤,在Castleman病基础上可以看到一些大细胞,放大看(右图),这些大细胞CD15+、CD30+。
81、
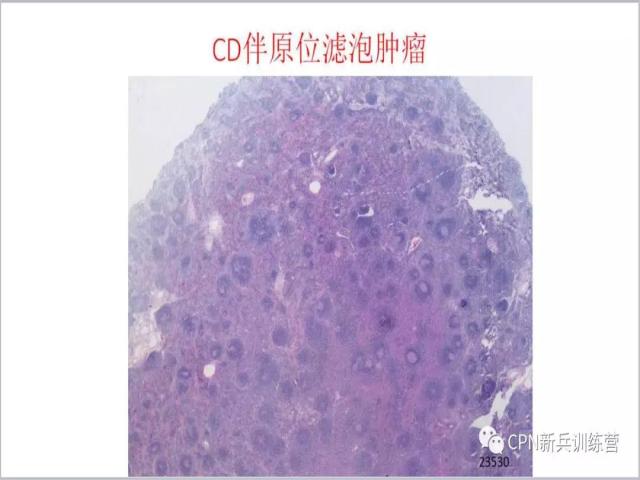
81、可以伴有原位的滤泡肿瘤,看起来是Castleman病,如果进行bcl-2、CD10染色,可以看到。
82、
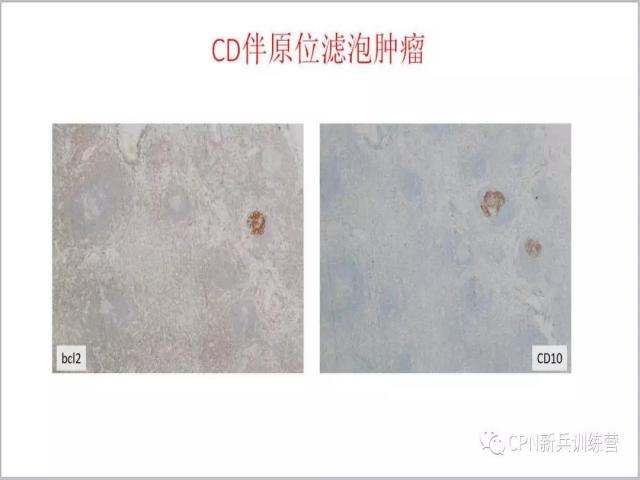
82、大部分生发中心bcl-2、CD10阴性,部分生发中心bcl-2、CD10阳性,这是原位滤泡肿瘤的特征,如果没有进行染色可能就当作Castleman病发报告了。
83、
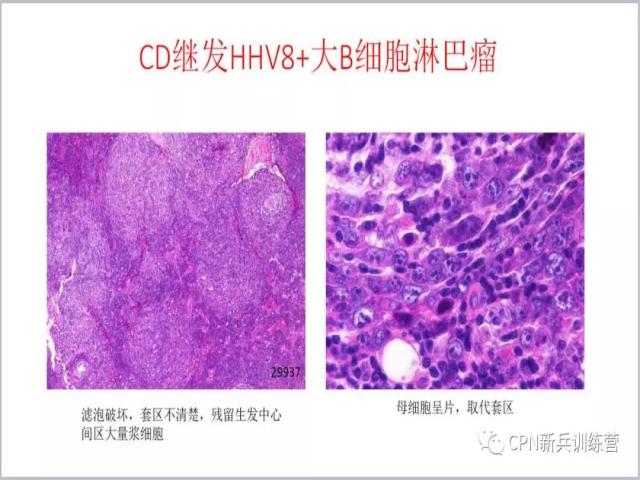
83、还有一部分可以继发HHV8+大B细胞淋巴瘤,我们刚才说了这样的滤泡是HHV8+Castleman病的诊断线索,如果这样的大细胞成片出现在套区,而套区内原有细胞少了,被大细胞取代了,这时就已经发展到了大B细胞淋巴瘤。
84、
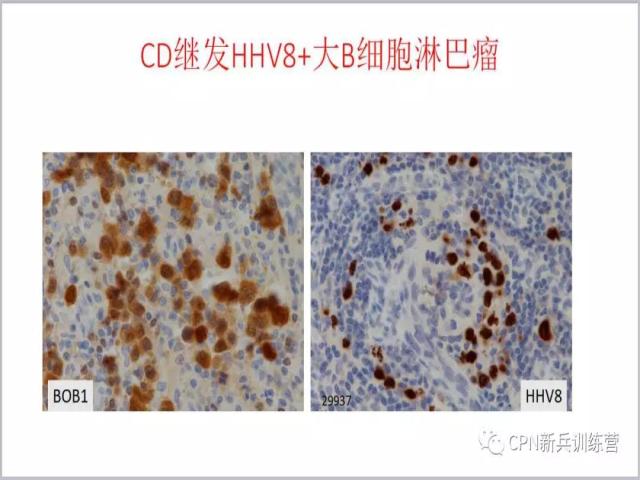
84、大细胞聚集。
85、
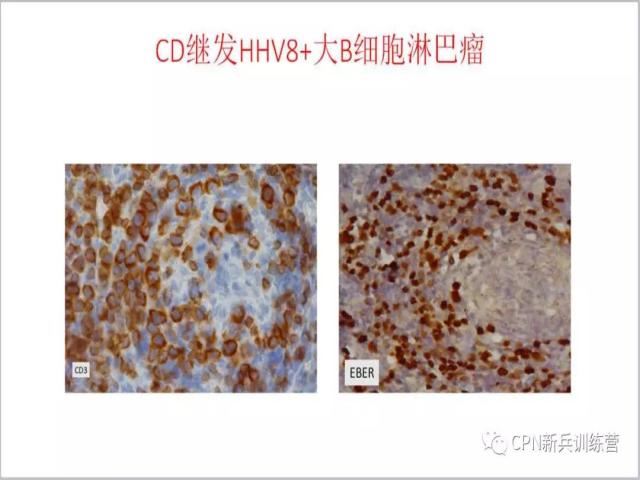
85、值得说明的一点是这些大细胞实际上是B细胞,但不表达CD20,而表达CD3、BOB1、Oct-2、MUM-1这些浆细胞标记,并且EBER+。有人说这是一种浆母细胞的母细胞改变,而不是我们平时所说的真正的、表达CD20的大B细胞淋巴瘤的改变。
86、

86、需要与以上几种进行鉴别诊断。
87、
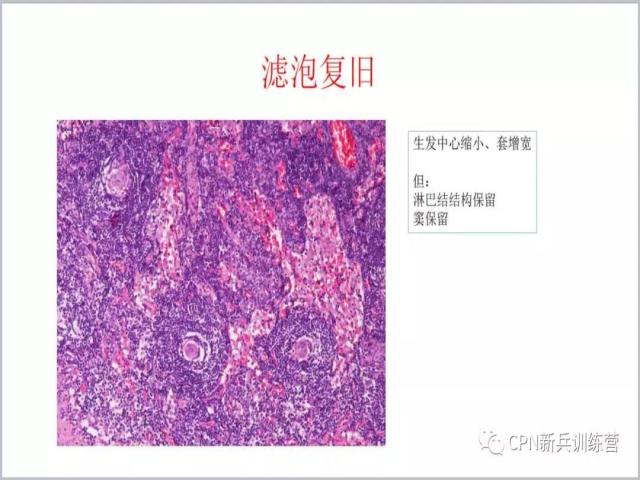
87、如果看到滤泡增多、生发中心缩小,不要都以为它是Castleman病,有时滤泡复旧也可以出现这样的改变,鉴别时有一个重要的特征就是淋巴结结构保留、窦存在。
88、
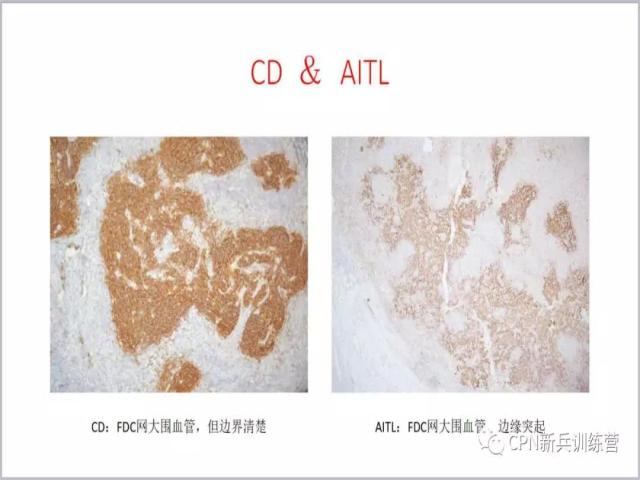
88、与血管免疫母细胞T细胞淋巴瘤(AITL)鉴别:CD病FDC网边界清楚,而AITL的FDC网呈毛刺样向外生长。
89、

89、CD与套细胞淋巴瘤在形态上很难进行鉴别,CyclinD1有助于鉴别。
90、
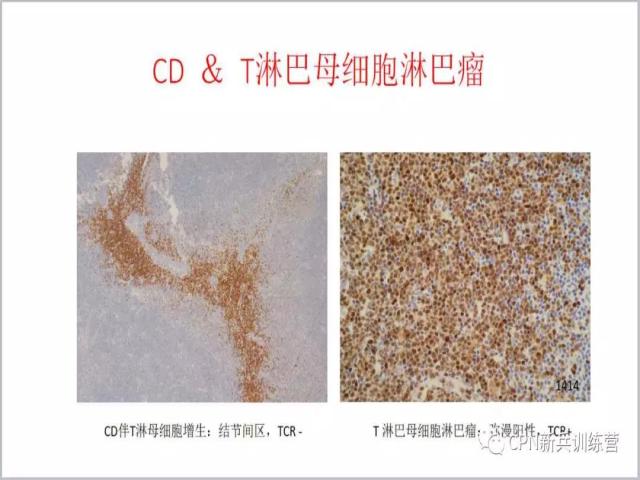
90、CD伴T淋巴母细胞增生和T淋巴母细胞瘤的鉴别:T淋巴母细胞增生时细胞是被挤压呈长条形、不规则的形状,而T淋巴母细胞淋巴瘤细胞是弥漫成片的、因生长较快呈现向外挤压的一种形态。另一个鉴别点是做LMO2和TCR的重排。
91、
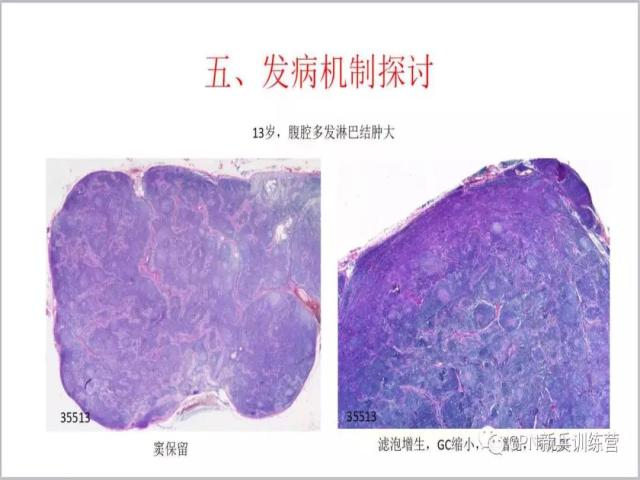
91、我们知道CD有滤泡为主的,有弥漫成片的,还有人说有窦存在的就不是Castleman病,下面我们看一个病例:13岁,腹腔多发淋巴结肿大,取多个淋巴结送检,在有的淋巴结内可以看到窦的存在,另一个淋巴结看到滤泡增生、GC缩小、套区增宽、窦可见。种种线索提示这是一个Castleman病。
92、

92、另外一个淋巴结内生发中心缩小了、套区增宽了,还有一些呈弥漫的、没有滤泡的区域,所以说弥漫的病变开始的时候就是弥漫的,不是破坏或挤压细胞而形成的。这个病例告诉我们Castleman病的不同时期的不同的病变。
93、
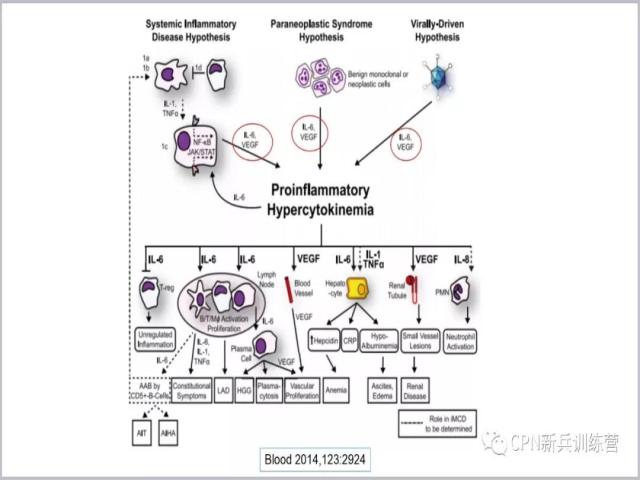
93、那么Castleman病是怎么发生的呢?现在的理论认为,可能与炎症因子、病毒、肿瘤性因素等有关,他们共同的关键特点是都经过了IL-6和血管生成素因子的影响,淋巴结内炎细胞、淋巴细胞、血管的增生都与此有关,出现了我们看到的形态的改变。
94、

94、近两年对Castleman病研究又有了新的进展,其中一个就是应用二代测序发现有些Castleman病有基因的突变。
95、

95、其中一个认识对特发性的多中心Castleman病又有了新的划分,把有独特临床表现的病例又拿出来了,他把它叫做TAFRO综合症(T—血小板减少;A—全身水中;F—发热;R—网状纤维性骨髓纤维化;O—器官肿大),这部分病人预后更差一些。
96、

96、在流行病学方面的研究也有了进展,最近有一篇文章总结分析:单中心CD发病率很低,约百万分之十六;HHV8+MCD变化很大,发病不太清楚;特发性多中心Castleman病发病率约百万分之五,相对来说发病率较少。
97、

97、这篇文章总结了273例Castleman病患者的分型分类比率,这是西方的一篇报道。
98、

98、总结:Castleman病不是单一疾病,至少是两种或以上的疾病;单中心和多中心CD预后不同,一定要区分开;多中心CD要区分出HHV8+和HHV8-,若HHV8+要检测是否有HIV感染,若HHV8-要结合临床区分是否为TAFRO;特发性单中心CD的专家共识诊断标准有两条主要标准和两条次要标准。
99、

















































































































共0条评论